欧洲药品管理局(EMA)开始审查GBT的镰状细胞疗法Oxbryta
2021-01-30 Allan MedSci原创
Oxbryta(voxelotor)旨在治疗12岁及以上的镰状细胞病(SCD)患者的溶血性贫血。
镰状血红蛋白的产生是由β珠蛋白基因的镰状点突变所致,这种血红蛋白的溶解性较正常的胎儿或成人血红蛋白差。镰状细胞病(SCD)包括镰状细胞贫血、镰状β地中海贫血、血红蛋白SC(HbSC)病等。
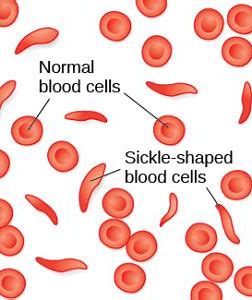
欧洲药品管理局(EMA)已接受了制药公司GBT关于Oxbryta(voxelotor)的销售授权申请。Oxbryta(voxelotor)旨在治疗12岁及以上的镰状细胞病(SCD)患者的溶血性贫血。
Oxbryta是一流的口服疗法,旨在抑制血红蛋白聚合,血红蛋白聚合会导致SCD中红细胞的镰状化和破坏,进而会影响到整个身体的血液和氧气流量,同时减少输送到组织和器官的氧气,这会导致危及生命的并发症。
III期HOPE研究以及II期HOPE-KIDS 1研究的数据均得到了积极结果。在HOPE研究中,Oxbryta(voxelotor)组患者在24周时血红蛋白(Hb)水平显著改善。
EMA已经授予Oxbryta优先药品称号(PRIME)。GBT总裁兼首席执行官Ted Love表示:“镰状细胞病对患者及其家人的生活造成了毁灭性影响,包括严重且威胁生命的并发症,可能导致器官损伤和早逝。尽管有如此巨大的需求,但目前欧洲尚无可以改变疾病进程的疗法”。
原始出处:
http://www.pharmatimes.com/news/ema_begins_review_of_gbts_sickle_cell_treatment_oxbryta_1362312
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#药品管理#
72
#EMA#
59
#欧洲#
68
#欧洲药品管理局#
86
#镰状细胞#
106