2020诺贝尔化学奖再出悬疑:基因编辑技术获奖,华裔科学家张锋错失
2020-10-07 网络 网络
10月7日,2020年诺贝尔奖的最后一个自然科学奖项——化学奖被揭晓,埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和詹妮弗·
10月7日,2020年诺贝尔奖的最后一个自然科学奖项——化学奖被揭晓,埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和詹妮弗·杜德纳(Jennifer Anne Doudna)获得了这一奖项,获奖原因是开发了一种基因组编辑的方法。
在基因编辑技术应用中,张锋几乎是绕不过去的重要人物,他未能因所做的开创性贡献入围诺奖令人生疑,或许将成为近期讨论的一个话题。
当然,诺贝尔奖在过往有很多争议,尤其是涉及到华人方面,有很多错失。例如庄小威教授错失,袁均英教授错失,如今张锋再次错失,令人遗憾!

Emmanuelle Charpentier 和Jennifer A. Doudna 发现了基因技术中最尖端的工具: CRISPR/Cas9基因剪刀。利用这项技术,研究人员可以极其精确地改变动物、植物和微生物的 DNA。这项技术不仅对生命科学产生了革命性的影响,为开创新的癌症疗法做出了贡献,还可能使治愈遗传性疾病的梦想成为现实。
“这种基因工具具有巨大的力量,它将会影响我们所有人。”诺贝尔化学奖委员会 (Nobel Committee for Chemistry) 主席克拉斯古斯塔夫松 (Claes Gustafsson) 表示: “它不仅彻底改变了基础科学,可以创造新型作物,还能开创性新的医疗方法。”
自从 Charpentier 和 Doudna 在2012年发现 CRISPR/Cas9基因剪刀以来,相关的应用呈爆炸式增长。这项工具在基础研究中的许多重要发现中做出了贡献,例如,植物学研究中,植物研究人员已经能够开发抗霉菌、害虫和干旱的作物,而在医学上,新的癌症疗法的临床试验也正在进行中,治愈遗传性疾病的梦想或许在不远的未来实现。这些基因剪刀把生命科学带入了一个新时代,并且在许多方面给人类带来了最大的利益。
有些遗憾的是,对CRISPR-Cas9的发展和应用做出贡献的华裔科学家张锋不在获奖名单中。
CRISPR/Cas9技术
CRISPR/Cas9是继“锌指核酸内切酶(ZFN)”、“类转录激活因子效应物核酸酶(TALEN)”之后出现的第三代“基因组定点编辑技术”。所谓“基因编辑技术”,就是能够让人类对目标基因进行“编辑”,实现对特定DNA片段的敲除、加入的一项技术。
与前两代技术相比,CRISPR/Cas9具有成本低、制作简便、快捷高效的优点,于是它迅速风靡于世界各地的实验室,成为科研、医疗等领域的有效工具。

△CRISPR/Cas9被称作“基因魔剪”(图片来源:诺贝尔官方网站)
CRISPR/Cas9系统的工作原理
那么,这么厉害的技术,是如何操作的呢?
在细菌的基因组上,存在着串联间隔排列的“重复序列”,这些重复序列相对保守,我们称之为CRISPR序列(Clustered Regularly Interspersed Short Palindromic Repeats—成簇的规律间隔的短回文重复序列)。
1.“记录”入侵者档案
其中的“间隔序列”来源于病毒或外源质粒的一小段DNA,是细菌对这些外来入侵者的“记录”。

△CRISPR序列示意图(其中,菱形框表示高度可变的间隔序列,正方形表示相对保守的重复序列)
病毒或外源质粒上,存在“原间隔序列”,“间隔序列”正是与它们互相对应。“原间隔序列”的选取并不是随机的,这些原间隔序列的两端向外延伸的几个碱基往往都很保守,我们称为PAM(Protospacer adjacent motifs-原间隔序列临近基序)。
当病毒或外源质粒DNA首次入侵到细菌体内时,细菌会对外源DNA潜在的PAM序列进行扫描识别,将临近PAM的序列作为候选的“原间隔序列”,将其整合到细菌基因组上CRISPR序列中的两个“重复序列”之间。这就是“间隔序列”产生的过程。
2、打击二次入侵者
当外源质粒或病毒再次入侵宿主菌时,会诱导CRISPR序列的表达。同时,在CRISPR序列附近还有一组保守的蛋白编码基因,称为Cas基因。CRISPR序列的转录产物CRISPR RNA和Cas基因的表达产物等一起合作,通过对PAM序列的识别,以及“间隔序列”与外源DNA的碱基互补配对,来找到外源DNA上的靶序列,并对其切割,降解外源DNA。这也就实现了对病毒或外源质粒再次入侵的免疫应答。
正是基于细菌的这种后天免疫防御机制,CRISPR/Cas9技术应运而生,从而使科学家们利用RNA引导Cas9核酸酶实现对多种细胞基因组的特定位点进行修饰。
CRISPR/Cas9技术在基因敲除中的实现过程
如下图所示,在待敲除基因的上下游各设计一条向导RNA(向导RNA1,向导RNA2),将其与含有Cas9蛋白编码基因的质粒一同转入细胞中,向导RNA通过碱基互补配对可以靶向PAM附近的目标序列,Cas9蛋白会使该基因上下游的DNA双链断裂。
对于DNA双链的断裂这一生物事件,生物体自身存在着DNA损伤修复的应答机制,会将断裂上下游两端的序列连接起来,从而实现了细胞中目标基因的敲除。
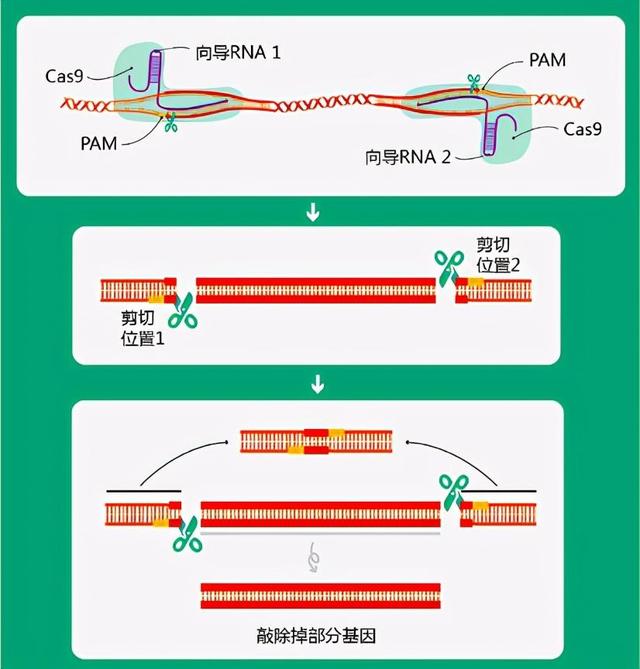
△CRISPR/Cas9技术敲除掉部分基因原理图(绘图肖媛)
而DNA片断的插入或定点突变的实现,只需在此基础上为细胞提供一个修复的模板质粒,这样细胞就会按照提供的模板在修复过程中引入片段插入或定点突变,对受精卵细胞进行基因编辑,并将其导入代孕母体中,可以实现基因编辑动物模型的构建。
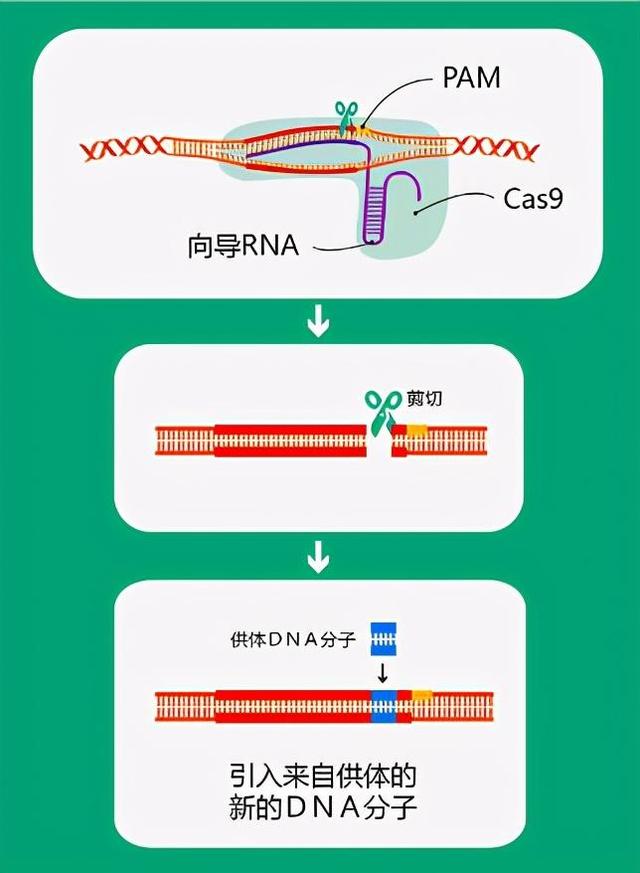
△CRISPR/Cas9技术插入新基因原理图(绘图肖媛)
CRISPR/Cas9技术的应用
利用基因编辑技术CRISPR/Cas9,科学家们做出了许多成果。比如,北京希诺谷生物科技有限公司用此技术培育出比格犬“龙龙”,它成为我国首例完全自主培育的体细胞克隆犬,也是世界首例基因编辑克隆犬。

△世界首例基因编辑克隆犬“龙龙”(图片来源科技日报)
除此以外,来自美国、中国、丹麦研究机构的科学家凭借此技术成功克隆出世界上第一批不携带活性内源性逆转录病毒(PERVs)的猪,克隆猪将来可以满足人类器官移植的需要。
随着对CRISPR系统认识的加深,实验设计的优化改造,我们相信CRISPR/Cas9以及其衍生技术终究会带来一场科学史上的巨大变革。期待在不久的将来,CRISPR/Cas9所带来的巨大转变必将能够惠泽万家。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#获奖#
44
#华裔#
48
#诺贝尔化学奖#
34
#基因编辑技术#
53
关注好久了
135