Stem Cell Rep:aPKC-CBP信号通路参与调节中风后神经血管的重塑和功能恢复!
2018-01-30 MedSci MedSci原创
科学家的研究表明非典型的蛋白激酶C(atypical protein kinase C,aPKC)介导在CREB-结合蛋白中S436的磷酸化,它在发育和老年大脑中调节神经前体细胞的分化。中风后的神经血管重塑过程中aPKC介导CREB结合蛋白磷酸化。
中风是全球重要的公共卫生负担,约有40%的中风病人会出现永久性的神经障碍。目前临床急需新型的脑中风后干预手段。越来越多的研究证据表明,损伤部位的多能性神经前体细胞不仅仅来自于侧脑室室管膜下区(lateral ventricle subventricular zone,SVZ),局部的非神经细胞也能重编程为多能性神经前体细胞。
周细胞在毛细血管中围绕内皮细胞,并且这些细胞能够在损伤后重编程为组织特异性的干细胞,它是一个极具吸引力的细胞资源。在中风相关的脑损伤中,周细胞重编程为多功能神经前体细胞必需经历间质-内皮转换过程。另外,由于细胞重编程的可塑性,周细胞能稳定新产生的微血管壁以及维持血脑屏障,因此对中风后血管重塑十分重要。
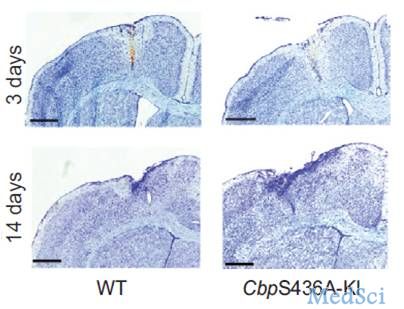
科学家的研究表明非典型的蛋白激酶C(atypical protein kinase C,aPKC)介导在CREB-结合蛋白中S436的磷酸化,它在发育和老年大脑中调节神经前体细胞的分化。中风后的神经血管重塑过程中aPKC介导CREB结合蛋白磷酸化。应用aPKC-CBP信号通路缺陷的敲入基因鼠(CbpS436A),科学家展示了破坏aPKC-CBP信号通路后,在小鼠局灶性缺血性中风模型中会增加缺血激活的周细胞(ischemia-activated pericytes,i-pericytes)重编程为神经前体细胞的效率。而细胞重编程效率的提升使CbpS436A小鼠在中风后局灶来源的神经前体细胞群体出现一过性的增加,同时表现出i-pericytes数量的减少,而这会导致血管重塑过程受损,从而妨碍在中风慢性期的运动恢复。
总之,这个研究表明aPKC-CBP信号通路在调节局灶性缺血性中风后神经血管重塑以及功能修复过程中的重要作用。
原文出处:Gouveia A, Seegobin M, Kannangara T S, et al. The aPKC-CBP Pathway Regulates Post-stroke Neurovascular Remodeling and Functional Recovery[J]. Stem Cell Reports, 2017, 9(6): 1735-1744.DOI: 10.1016/j.stemcr.2017.10.021
本文由梅斯医学(MedSci)原创编译整理,转载需授权!
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Cell#
42
#aPKC-CBP#
35
#stem cell#
39
#CBP#
40
#CEL#
32