一场关于结直肠癌肝转移治疗后复发的“圆桌对话”
2019-01-29 阿拉蕾 中国医学论坛报
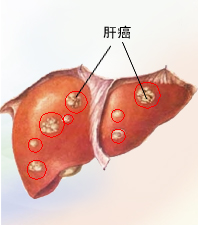
肝脏是结直肠癌转移最主要的靶器官,结直肠癌肝转移(CRLM)患者通过以手术为主的综合治疗能够获得长期生存甚至治愈。但是,CRLM治疗后复发是临床上面临的难点,也是影响患者预后的主要原因。
肝脏是结直肠癌转移最主要的靶器官,结直肠癌肝转移(CRLM)患者通过以手术为主的综合治疗能够获得长期生存甚至治愈。但是,CRLM治疗后复发是临床上面临的难点,也是影响患者预后的主要原因。
针对上述问题,让我们看浙江大学医学院附属第二医院王建伟教授,浙江大学医学院附属邵逸夫医院宋章法教授以及浙江省肿瘤医院鞠海星教授如何解答。



左图:王建伟教授 中图:宋章法教授 右图:鞠海星教授
王建伟教授:浙江大学医学院附属第二医院肿瘤外科主任医师,博士研究生导师,中国抗癌协会大肠癌专业委员会肝转移学组委员,中国肿瘤防治联盟浙江省联盟结直肠专业委员会副主任委员,中国医师协会结直肠肿瘤分会肝转移专业委员会委员
宋章法教授:浙江大学医学院附属邵逸夫医院肛肠外科副主任医师,医学博士,博士研究生导师,浙江省生物医学治疗重点实验室副主任,中国医师协会外科学分会肛肠外科分会委员
鞠海星教授:浙江省肿瘤医院结直肠外科科室副主任,主任医师,硕士研究生导师,中国抗癌协会大肠癌专业委员会青年委员,中国医师协会结直肠肿瘤分会外科专业委员会委员
无疾病证据(NED)概念
能够接受肝转移灶切除的患者数量有限,而初始不可切除的患者,其预后不理想。2016年,欧洲肿瘤内科学会(ESMO)指南提出NED概念,即病理学、影像学、分子生物学等检查未发现肿瘤存在证据。除了根治性手术(RO切除),也可以通过射频消融、立体定向体部放疗(SBRT)等治疗实现NED。初始不可切除患者经过转化治疗在用过局部治疗达到NED后能够获得生存获益。然而,NED治疗后复发率高仍是临床上面临的难点。关注复发必须要从复发部位分布和复发时间两个维度来分析。
复发部位
从目前数据来看,约有80%的患者会出现CRLM切除术后复发,即便是R0切除,手术切除的部位复发率也有约4%。针对初始肝转移灶不可切除的患者,通过其他非手术治疗手段(如射频/化疗达到CR)达到NED,也存在一定的局部复发率,通过文献回顾可以看到射频消融部位复发率约为10%,而对于化疗过程中消失的病灶复发率约为14%。
从复发部位来看,最常见的为肝内转移和肺转移,单纯一个部位的复发约占75%,两个部位的复发约占20%。如果是单个部位出现治疗后复发,预后较好。出现单个肝内复发患者的中位总生存期(OS)约为2年,单个肺内复发患者的OS约为3年。从目前的数据来看,初始经过手术切除转移灶的患者如果出现复发,其复发灶数量多在2个以内(约90%)。因此,在能够达到NED的各种治疗手段中,手术治疗仍处于核心地位。
复发时间
CRLM切除术后复发率较高,大部分患者为2年内出现复发,越早出现复发,预后越差。但是,目前对于早期复发的时间定义还不是十分明确。近期,Adam教授团队的一项回顾性临床研究共纳入987例结直肠癌肝转移术后患者,其中670例出现复发,复发率约为70%,并把不同的复发时间点作为cut-off值去评估复发时间对预后的影响。研究结果显示,术后8个月内出现复发的患者,其5年生存率约为18.5%,而8个月以上出现复发的患者,5年生存率约为53.4%。因此,术后8个月是否出现复发是评估预后的重要指标。
通过分析影响CRLM切除术后早期复发的因素,发现主要包括5点:年龄≤57岁;术前进行过大于一线的化疗;在最后一次化疗后出现进展;肝转移灶>3个;癌胚抗原(CEA)>60 ng/ml 。对于这些具有这些早期复发高危因素的患者,我们应当加强术后监测。
早期复发后治疗的预后影响因素
CRLM早期复发后治疗的预后影响因素主要包括:原发灶淋巴结阳性、CEA>50 ng/ml、以及是否再次进行手术治疗。既往的观念认为,术后出现复发的患者预后较差,再次进行手术的效果也不理想。但是也有临床研究结果显示,再次进行手术治疗患者的5年生存率可达38.8%。因此,针对早期复发的患者,我们仍然可以选择手术治疗。
此外,是否使用靶向药物也是独立的预后影响因素。合理使用有效的靶向治疗药物(如快速缩瘤的西妥昔单抗),能够帮助CRLM术后早期复发患者取得更为理想的疾病控制,从而提高再次手术的疗效。
非手术治疗手段的地位
从复发部位来看,合并有肝外转移的比例高于单纯肝内转移,这提示我们,对于希望达到NED的患者,临床医生是否应该进行积极的全程全身治疗,从而有效降低NED后出现快速肝外或全身转移的情况。近年来的数据显示,经过化疗等全身治疗也能够达到较为理想的NED状态(pCR率接近8%-30%) 。因此,针对肝转移灶数目较多的患者,积极的给予全身治疗能够进一步提高患者的生存获益。
消失的肝转移灶
近年来,有个新的定义叫肝转移灶化疗后“消失”(DLM),它究竟能带给我们何种启示,业内尚有争议。针对不同的患者,我们有不同的治疗目标。如果是初始可切除的患者,尽可能避免新辅助化疗让病灶消失,因为R0切除后的复发率最低;如果病灶数目较多,例如大病灶伴有多个小病灶,那么化疗的目的是通过缩瘤转化为可切除,同时会让部分小病灶消失。此外,如果病灶在化疗后消失,这也提示我们肿瘤对化疗敏感,生物学行为较好,生存预后较为理想,我们需要给予这部分患者积极的治疗。
评估肝转移灶是否消失的方法有很多种,肝脏增强MRI是术前评估的精准手段,术中超声也能够帮助我们进一步鉴别,如果发现术前评估未显示的残余病灶,直接进行手术处理。这里需要区分两个概念,一为“病灶消失”,是指经过化疗,术前及术中均未能发现病灶;一为“病灶错失”,是指化疗后病灶显着缩小,术中超声可能无法准确定位而造成遗漏。
总结
从RO切除到NED,这种肝转移治疗目标的改变体现了诊疗理念的进步。针对CRLM治疗后复发的患者,我们需要综合评估复发部位、复发时间、病灶数量等因素,制定个体化的治疗策略,结合手术、化疗、靶向药物、射频消融等各种治疗手段,提高患者的预后。
作者:阿拉蕾
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#转移治疗#
67
#肝转移#
48
#结直肠#
62
好
107
学习了,谢谢分享
96