PLOS ONE:研究揭示帕金森病相关突触核蛋白的迁移特性
2013-05-02 PLOS ONE dxy
α-突触核蛋白迁移特性 一种已知的在帕金森病的发展中具有关键作用的蛋白可以像病毒一样进入细胞和造成损害。这种蛋白叫做α-突触核蛋白。研究显示,一旦进入一神经元后,α-突触核蛋白就会离开溶酶体这个细胞的消化车间。这与流感病毒在感染中进入细胞的过程很相似。这项发现最终能导致新治疗方法的产生来延缓帕金森病的发病或者是阻断、减缓其进程,研究者说。这项由病毒学家Edward Campbell博士和他的同事
一种已知的在帕金森病的发展中具有关键作用的蛋白可以像病毒一样进入细胞和造成损害。这种蛋白叫做α-突触核蛋白。研究显示,一旦进入一神经元后,α-突触核蛋白就会离开溶酶体这个细胞的消化车间。这与流感病毒在感染中进入细胞的过程很相似。这项发现最终能导致新治疗方法的产生来延缓帕金森病的发病或者是阻断、减缓其进程,研究者说。这项由病毒学家Edward Campbell博士和他的同事完成的研究发表在2013,4,25号的PLOS ONE 杂志上。
α-突触核蛋白在正常的健康神经元中行使一定的功能。但是在帕金森病患者,这种蛋白变坏了,集聚成块导致大脑负责运动控制区域的神经元的死亡。之前的研究显示这些蛋白集聚后能进入细胞并造成伤害。Campbell和他的同事弄明白了α-突触核蛋白是如何逃出溶酶体的,这些小分子的结构共同作为细胞的消化系统。这些气泡状结构(也叫做囊泡)的破裂释放的酶对其它的细胞是有害的。“溶酶体酶类的释放可被细胞作为‘危险信号’感觉到,因此相似的溶酶体破坏经常由入侵的病毒或者细菌引起,”Chris Wiethoff,这个研究的合作者说。“溶酶体经常被描述为‘自杀包’因为当它们被病毒或细菌诱导破裂时,它们诱导的氧化应激经常导致受感染细胞的死亡。”
在病毒或细菌感染中,这种感染细胞的死亡整体来说对感染者是一件好事。但是在帕金森病中,相同的保护机制可能会导致神经元的死亡,增加α-突触核蛋白在大脑细胞之间的扩散,Campbell 说。“这可以解释帕金森病的自然进程。更多受到影响的细胞导致大脑中更多毒性α-突触核蛋白蛋白的扩散集聚,”Campbell 说。“这和病毒感染扩散所发生的现象是非常相似的。”
Campbell强调这些研究需要继续研究并在别的帕金森病模型中得到确认。“利用培养的细胞模型,我们有了一些令人激动的发现。然而,我们需要去了解溶酶体破裂在帕金森病动物模型中是如何影响疾病进程的,最终,需要了解帕金森病影响的人类大脑。我们能干扰α-突触核蛋白在这些情况下让溶酶体破坏的能力吗?这会对疾病的进程有积极的影响吗?这些是我们下一步很激动的要去问的问题。”Jeffrey H.Kordower,医学博士,神经病学的教授,神经外科教授和拉什大学医学中心脑修复研究中心的主任,说这项研究“是研究结果已经开始影响帕金森病领域的一群研究者的一项很重要的发现。这篇文章加深了有关alpha-synuclein 蛋白的理解,帕金森病的主要诱因,能从一个细胞转入另一细胞。这篇文章完美地解决了这种转移背后的机制。这个发现将会影响最近几年帕金森病的研究方向。”
与帕金森相关的拓展阅读:
- AAN 2013:帕金森病精神症状治疗新药Pimavanserin效果良好
- NEJM:脑刺激配合药物治疗早期帕金森更优
- NEJM:下丘脑刺激有助于改善早期帕金森症状
- 帕金森可在细胞间传播
- AAN2013:唾液腺活检或有助于帕金森病诊断
- Neurology:帕金森病患者α-突触核蛋白自身抗体水平较低 更多信息请点击:有关帕金森更多资讯

Alpha-Synuclein Induces Lysosomal Rupture and Cathepsin Dependent Reactive Oxygen Species Following Endocytosis
Abstract
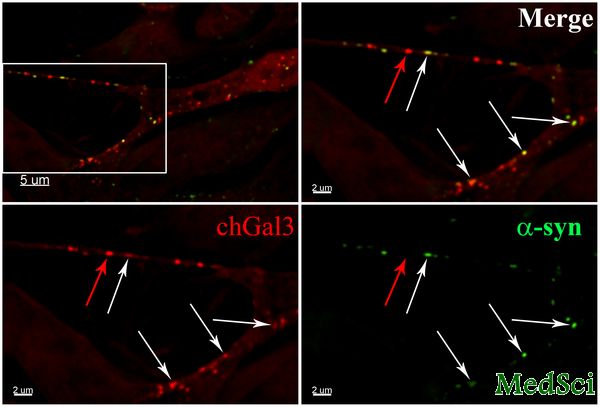
α-synuclein dysregulation is a critical aspect of Parkinson's disease pathology. Recent studies have observed that α-synuclein aggregates are cytotoxic to cells in culture and that this toxicity can be spread between cells. However, the molecular mechanisms governing this cytotoxicity and spread are poorly characterized. Recent studies of viruses and bacteria, which achieve their cytoplasmic entry by rupturing intracellular vesicles, have utilized the redistribution of galectin proteins as a tool to measure vesicle rupture by these organisms. Using this approach, we demonstrate that α-synuclein aggregates can induce the rupture of lysosomes following their endocytosis in neuronal cell lines. This rupture can be induced by the addition of α-synuclein aggregates directly into cells as well as by cell-to-cell transfer of α-synuclein. We also observe that lysosomal rupture by α-synuclein induces a cathepsin B dependent increase in reactive oxygen species (ROS) in target cells. Finally, we observe that α-synuclein aggregates can induce inflammasome activation in THP-1 cells. Lysosomal rupture is known to induce mitochondrial dysfunction and inflammation, both of which are well established aspects of Parkinson's disease, thus connecting these aspects of Parkinson's disease to the propagation of α-synuclein pathology in cells.
作者:PLOS ONE
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#迁移#
66
#Plos one#
56
#核蛋白#
64
#突触#
62