大脑是如何“老化”的?《柳叶刀》子刊:运动能力下降比认知衰退早10年!
2024-08-25 医学新视点 医学新视点
发表于The Lancet Healthy Longevity的一项研究结果表明,在老年人中,整体认知能力和运动功能(步态功能和手部力量)呈衰退趋势。
既往研究表明,阿尔茨海默病(AD)的病理累积过程可能持续多年,在早期阶段尚未表现出认知能力受损,但病理变化已经悄然发生。此外AD及相关痴呆症的病理状态不仅可能导致认知障碍,还可能对老年人的步态和手部力量产生影响。然而,现有研究还缺乏充足的证据,通过随时间变化的轨迹(即“纵向轨迹”)来说明运动功能衰退和认知能力衰退的先后变化情况。
发表于The Lancet Healthy Longevity的一项研究结果表明,在老年人中,整体认知能力和运动功能(步态功能和手部力量)呈衰退趋势。而且,步态功能和手部力量衰退比认知能力衰退早了长达10年。手部力量衰退可能有助于识别AD风险;步态功能衰退可能是早期血管性认知障碍的生物标志物,而不是AD的临床前生物标志物。
此外,大多数认知能力衰退是由大脑病理引起的,而运动能力衰退并不完全由年龄和大脑病理引起,单凭步态衰退不足以预测痴呆症风险。

截图来源:The Lancet Healthy Longevity
该队列研究使用了三项衰老慢性病队列研究中的老年人数据,旨在描述老年人认知能力和运动功能随着时间推移的衰退轨迹,并探讨其与AD及相关痴呆症病理的关联。
所有三项队列研究的纳入标准为:入组时≧65岁,无临床诊断的痴呆症,这些参与者同意在死后捐献大脑进行痴呆症病理学评估,且同意对认知能力和运动功能(步态功能和手部力量)进行至少三次年度评估。研究团队基于19项神经心理测试对参与者进行整体认知能力评估,通过握力和捏力评估手部力量,并基于行走2.44 m并转身360°的步数和时间来进行步态评分。
具有认知能力和运动测量数据的1303例参与者被纳入分析,他们的平均死亡年龄为90.3岁,其中905例(69%)为女性,398例(31%)为男性。在中位时间为9年的随访中发现:
-
参与者的认知能力、步态功能和手部力量的平均值均有所下降。
-
平均而言,步态功能和手部力量衰退早于认知能力衰退。参与者的认知能力在死亡前25-15年间大致保持稳定,此后开始衰退,并在死亡前5年加速衰退。相比之下,步态功能和手部力量在整个研究期间呈持续衰退趋势。
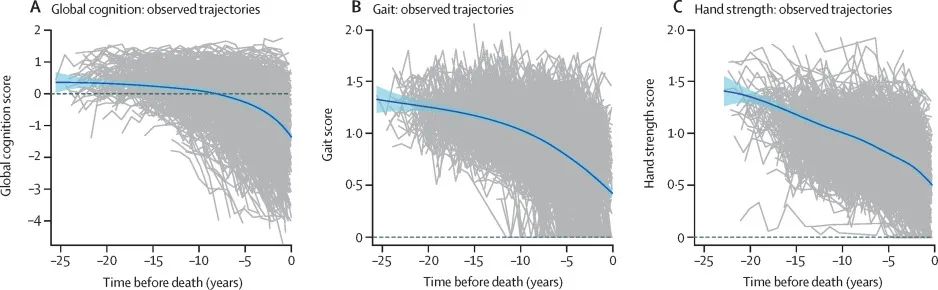
▲参与者的认知能力(A)和运动功能(B:步态功能;C:手部力量)衰退轨迹(图片来源:参考资料[1])
进一步分析AD及相关痴呆症的10种病理特征变化发现:AD及相关痴呆症的各项病理表现与认知能力和运动功能衰退的关联不同,关联的起始时间也有所不同。
-
只有tau缠结(与认知能力损害相关的异常蛋白积累)、帕金森病病理和大面积脑梗塞这三种病理与认知能力、步态功能和手部力量这三大表现的衰退都有关,而脑淀粉样血管病变与上述任何一种变化均无关联。
-
相比步态功能衰退,手部力量与各项病理表现的关联程度更紧密。与步态功能衰退相关的仅上述3种病理表现,与手部力量衰退相关的病理表现还有其他3种,包括海马硬化、TDP-43和小动脉硬化。
-
tau缠结与认知能力衰退的关联早于其与步态功能和手部力量衰退的关联。具体来说,tau缠结在死亡前11年中都与认知能力衰退有关,其与手部力量衰退的关联始于死亡前3.57年,和与步态功能衰退的关联始于死亡前3.49年。
-
大面积脑梗塞与步态功能衰退的关联始于死亡前9.25年(P<0.0001),早于其与认知能力和手部力量衰退的关联,其与后两者的关联分别始于死亡前6.65年(P=0.0005)和2.66年(P=0.024)。
-
帕金森病病理与认知能力衰退的关联较早出现(始于死亡前7.93年),而与步态功能衰退(始于死亡前4.60年)或手部力量衰退(始于死亡前5.80年)的关联则更晚出现。
在四项敏感性分析中也得到了类似的结果。
研究团队还分析了死亡年龄与认知能力和运动功能衰退之间的关联。结果显示:
剔除AD及相关痴呆症病理的影响后,年龄与认知能力衰退的关联大大减弱。这些发现表明,在老年人中观察到的大部分认知能力衰退归因于AD及相关痴呆症病理变化,包括海马硬化、TDP-43、帕金森病病理、大面积脑梗塞、微梗塞和动脉粥样硬化。
然而,即便剔除AD及相关痴呆症病理的影响后,年龄与运动功能衰退的关联依然存在,尤其是步态功能衰退的幅度比手部力量下降更明显。这意味着,运动功能衰退尤其是步态功能衰退不仅仅与年龄和脑部病理有关,仅凭步态功能衰退还不足以预测AD及相关痴呆症的各种不良健康结局或类型。这也符合目前的医学认识,因为与认知相关的潜在神经通路几乎全部包含在大脑内,而运动功能相关的潜在通路则不仅涉及大脑,还涉及脑干、脊髓、周围神经和肌肉。
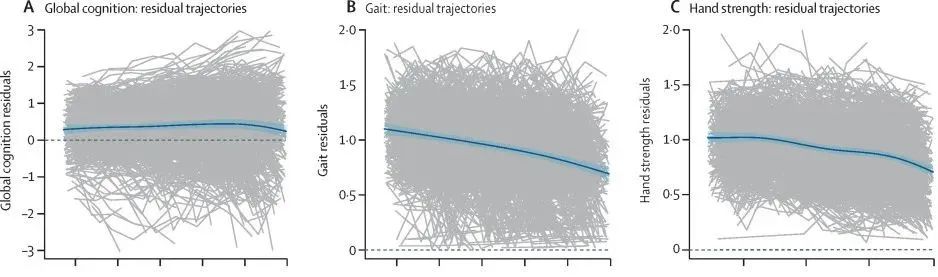
▲剔除AD及相关痴呆症病理关联后,年龄与认知衰退的关联减弱(A),年龄与步态功能衰退(B)和手部力量下降(C)的关联仍然明显,步态功能衰退的幅度更明显(图片来源:参考资料[1])
总体而言,研究结果表明,在老年人中,运动功能的平均衰退早于认知能力衰退。大脑大面积梗死而非tau缠结与“步态功能衰退早于认知能力衰退”这一现象相关。这表明有必要进一步研究步态受损是否可以作为临床前期血管性认知障碍的临床标志,还需要观察与步态功能衰退相关的其他影响因素,如肥胖、肌肉骨骼疾病(包括背部、臀部和膝盖的骨关节炎)和其他合并症,以及脑外运动通路的病理学与步态衰退的关系。
该研究的同期评论文章指出,该研究为运动功能衰退与痴呆症的神经病理基础间的关联提供了有趣的洞见,增加了关于步态、血管健康和痴呆症之间关系的证据,并有助于未来的研究更好地理解已积累的观察性证据。
参考资料
[1] Oveisgharan S, Wang T, et al., (2024). The time course of motor and cognitive decline in older adults and their associations with brain pathologies: a multicohort study. Lancet Healthy Longev. doi: 10.1016/S2666-7568(24)00033-3.
[2] Emma Nichols, Jennifer S Rabin. (2024). Declining motor and cognitive functioning and the role of gait in dementia. Lancet Healthy Longev. DOI: 10.1016/S2666-7568(24)00049-7
作者:医学新视点
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#阿尔茨海默病# #运动能力# #认知衰退#
38