Invest Ophthalmol Vis Sci:Caspase-2介导钝性眼部损伤后特定部位的视网膜神经节细胞死亡
2018-09-12 MedSci MedSci原创
英国伯明翰大学炎症与衰老研究所神经科学与眼科学研究团队的Thomas CN、Thompson AM和McCance E等人近日在Invest Ophthalmol Vis Sci杂志上发表了一项重要研究,他们在大鼠钝性眼外伤模型中,研究caspase-2对视网膜神经节细胞和光感受器死亡的作用。
英国伯明翰大学炎症与衰老研究所神经科学与眼科学研究团队的Thomas CN、Thompson AM和McCance E等人近日在Invest Ophthalmol Vis Sci杂志上发表了一项重要研究,他们在大鼠钝性眼外伤模型中,研究caspase-2对视网膜神经节细胞和光感受器死亡的作用。
眼外伤在平民和军人中很常见。闭合的全眼球钝性眼外伤导致光感受器外节段(视网膜视网膜)的急性破坏和视网膜神经节细胞(RGC)死亡(创伤性视神经病[TON]),两者都永久性地损害视力。Caspase-2依赖性细胞死亡是一个重要的途径,并且在RGC变性模型中得到证实。

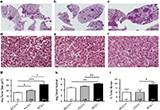
他们在雌性Lister-hooded大鼠中诱导双侧眼窝闭合球形钝性眼外伤,并通过Western印迹和免疫组织化学眼睛caspase-2作用和功能定位。通过向玻璃体内注射胱天蛋白酶-2小干扰RNA(siCASP2)敲除视网膜caspase-2。在视网膜切片中,通过BRN3A阳性细胞计数来评估RGC的存活情况、通过外核层(ONL)的厚度来评估光感受器的存活情况。通过视网膜电图(ERG)来评估视网膜功能。
结果发现,损伤后5、24和48小时,在视网膜中检测到裂解的半胱天冬酶-2水平升高,并且定位于RGC而不是光感受器。小干扰RNA介导的caspase-2敲低实验表明,小干扰RNA具有保护RGC的作用,但不在损伤部位的中心。此外,在损伤后2周,敲低caspase-2增加了ERG明视阴性反应(PhNR)的幅度。然而,siCASP2对光感受器没有保护作用,这表明该模型中的光感受器变性不是由caspase-2介导的。
因此,他们认为,Caspase-2可以一定比例介导RGC死亡,但在钝性眼外伤中不能介导光感受器的死亡。因此,玻璃体内递送的siCASP2可用于有效治疗RGC的死亡以预防创伤性视神经病。
原文出处:
Thomas, C.N., et al., Caspase-2 Mediates Site-Specific Retinal Ganglion Cell Death After Blunt Ocular Injury. Invest Ophthalmol Vis Sci, 2018. 59(11): p. 4453-4462.
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言




#视网膜神经#
47
#caspase-2#
46
#眼部#
36
#视网膜神经节细胞#
48
#EST#
35