一、病史简介
男性,51岁,上海人,2016-09-21收入中山医院感染病科
主诉:反复咳嗽、咳痰4余年,加重半年。
现病史:
患者2012年起无明显诱因下反复咳嗽、咳痰,偶有咯血,至外院就诊,具体诊疗过程不详,考虑“支气管扩张症”。
2012年、2014年外院体检查胸部CT示右侧肺部阴影(CT报告单和片子均遗失),未进一步诊治。近半年来诉咳嗽、咳痰症状加重,痰量中等,呈黄脓痰,无痰中带血,无发热、盗汗,无胸闷、胸痛。
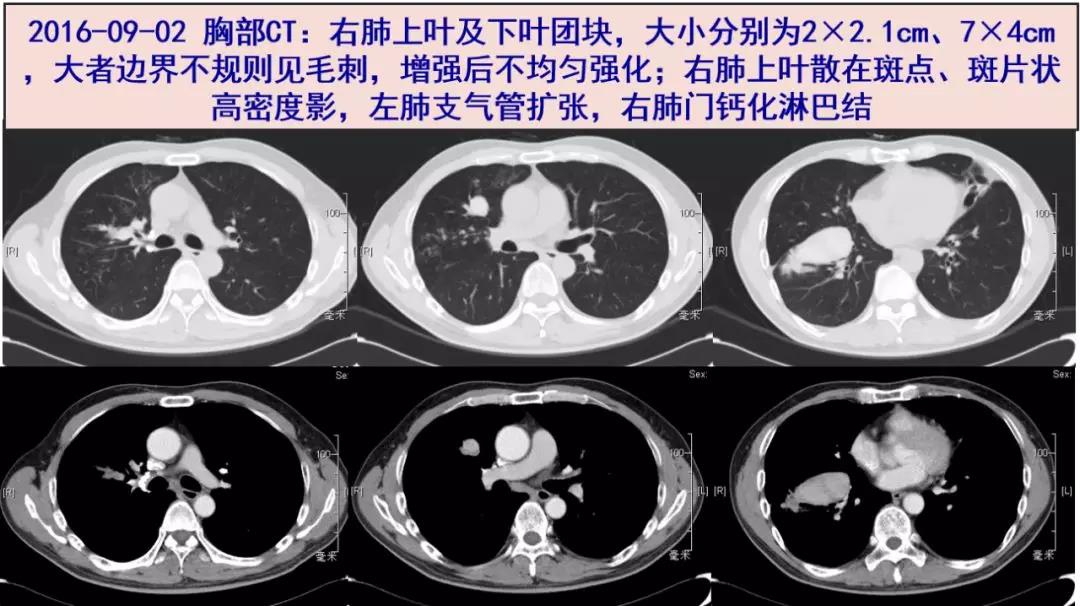
2016-09-02 至我院就诊,胸部CT:右肺上叶及下叶占位,大小分别为2×2.1cm、7×4cm,大者边界不规则见毛刺,增强后不均匀强化;右肺上叶散在斑点、斑片状高密度影,左肺支气管扩张,右肺门钙化淋巴结。血WBC 8.36x10^9/L,ESR 4mm/h,CRP 0.5mg/L,CEA 6.1ng/mL,IgE 76 IU/ml。G试验459.9,T-SPOT.A/B 16/1,隐球菌荚膜抗原阴性。痰细菌和真菌培养:均阴性。予以口服左氧氟沙星0.5g qd*2周,症状无缓解。
二、入院检查(2016-09-21)
【体格检查】
T 37℃,P 80 bpm,R 20 次/分,BP 130/80mmHg;
双肺呼吸音清,双肺可闻及细湿罗音。心律齐,未及杂音。腹平软,无压痛或反跳痛,双下肢无水肿。
【实验室检查】
血常规:WBC 10.77X10^9/L,N 66.1%,L 23.3%,Eos% 5.8%, Hb 140g/L,Plt 253X10^9/L;
炎症标志物:hs-CRP 0.7mg/L,ESR 3mm/H,PCT 0.03ng/mL;
血气分析:PaO2 86mmHg,PaCO2 41mmHg, SpO2 96%;
肝肾功能:ALT/AST 25/18U/L,Alb 46g/L,Scr 76umol/L;
自身抗体:均阴性;
肿瘤标志物:癌胚抗原 6.2ng/mL,余均阴性;
特定蛋白:IgG 19.16g/L,IgE 82 IU/Ml, IgA 2.86 g/L,IgM 2.00g/L;
T-SPOT A/B:23/2;血隐球菌荚膜抗原:阴性;1-3-β-D葡聚糖 :>1000 EU/ml;
痰涂片找细菌、真菌、抗酸杆菌:阴性。
【辅助检查】
09-22 心电图:正常
三、临床分析
病史特点:中年男性,反复咳嗽、咳痰4余年,加重半年,查白细胞轻度升高,血沉及CRP正常,CEA及G试验升高。原有支扩史,入院前3周胸部CT发现:右肺下叶团块4*7cm,右上肺结节2*2.1cm及散在斑点斑片影。疾病诊断和鉴别诊断考虑如下:
肺部肿瘤:患者中年男性,有咳嗽咳痰呼吸道症状4年,曾有痰血史。2012年和2014年外院胸部CT报告有右侧肺部阴影,但CT片子和报告单遗失。本次胸部CT发现右下肺较大团块病灶4*7cm,右上肺结节灶,查血炎症标记物(ESR和CRP)正常,而CEA升高,需考虑肺部肿瘤可能性,右下肺肿块系肺原发肿瘤,右上肺结节可能为转移性肿瘤,可行支气管镜肺活检以明确诊断。
肺结核:患者有咳嗽、咳痰4年,胸部CT示除了右下叶团块影以外,右肺上叶散在斑点、斑片和结节等多形态病灶,伴右肺门钙化淋巴结,T-SPOT两次阳性(分别为16/1和23/2),虽然无低热、盗汗,且血沉及CRP正常,仍需要考虑结核病可能,尤其是右上肺病灶,可行支气管镜检查肺活检和肺泡灌洗做组织病理和微生物学检查。
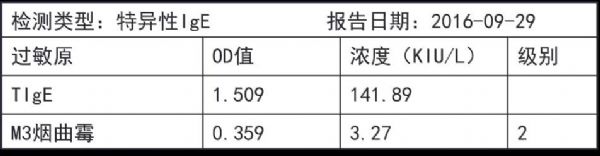
肺曲霉菌病:患者CT显示的右肺下叶团块影,密度高,边界清晰,除了肺部肿瘤外,尚需考虑痰栓形成的可能,常见原因为过敏性支气管肺曲霉病(ABPA),本病通常表现为外周血嗜酸性粒细胞升高、血IgE升高、炎症标记物(包括ESR和CRP)升高,但本例除外周血嗜酸性粒细胞升高外,其余正常。可行烟曲霉特异性抗体和支气管镜检查等明确或排除诊断。
肺细菌性感染:如铜绿假单胞菌,既往有支扩病史,反复出现咳嗽、咳痰,呈黄脓痰,血白细胞略有升高,但炎症标志物正常,痰细菌涂片及培养阴性,暂不考虑。
四、进一步检查、诊治过程和治疗反应
2016-09-23 行支气管镜检查,左侧各叶段支气管管腔通畅,黏膜光滑;右侧支气管:右上叶前段一亚段、右下叶前基底段黏膜稍肿胀,管腔内大量黄色黏性分泌物,未见新生物;

09-23 根据气管镜检查结果(管腔内见痰栓),结合血嗜酸性粒细胞升高,考虑ABPA,予以静滴甲强龙40mg qd,辅以护胃、补钙等治疗;
09-24 BALF及肺组织涂片找细菌、真菌及抗酸杆菌:阴性;咳痰(09-22送检)真菌培养:曲霉属1+;
09-26 支气管镜病理(右上叶前段)肺组织病理:坏死性肉芽肿;复查WBC 12.64X10^9/L,N 65.4%,血Eos下降至 0.01X10^9/L,血沉及CRP正常;
09-27 考虑ABPA合并肺曲霉菌感染可能,加用伊曲康唑注射液:起始剂量0.2g q12h*2d,维持剂量0.2g qd,静滴甲强龙减至30mg qd;
09-28 BALF 细菌培养阴性,真菌培养:曲霉属1+;肺组织细菌、真菌培养阴性;
10-03 复查ALT 221 U/L,AST 56 U/L,考虑药物性肝损,停伊曲康唑,改用卡泊芬净50mg qd(首剂70mg),同时保肝治疗;
10-04 诉咳嗽、咳痰较前明显好转,甲强龙改为口服美卓乐32mg qd;
10-07 美卓乐减量至28mg qd;随访肝酶仍进行性升高(ALT 632U/L,AST 149U/L) ,10-07停用卡泊芬净;
10-10 复查胸部CT:右肺上叶结节和下叶肿块消失,显示为扩张的支气管,右上肺斑点斑片影也较前(2016-09-02)明显吸收,左肺舌段支扩伴炎症;
10-19 复查肝酶好转后出院,出院予口服美卓乐28mg qd。
出院后随访
2016-11-03 美卓乐减量至24mgqd;
2016-11-24 美卓乐20mgqd,后每2周减量1片。
2017-02-27 患者复查胸部CT:两肺局部支扩伴慢性炎症,较前相仿,偶有咳嗽、咳痰,予以停用激素。
五、最后诊断与诊断依据
最后诊断:
肺曲霉病:过敏性支气管肺曲霉病(ABPA)合并侵袭性肺曲霉病
诊断依据:
患者中年男性,慢性病程,反复咳嗽、咳痰4余年,加重半年,胸部CT示右肺上叶结节和下叶团块影,外周血嗜酸性粒细胞升高,虽然炎症标记物(血沉及CRP)和IgE正常,但支气管镜检查见右上叶前段一亚段、右下叶前基底段黏膜稍肿胀,管腔内大量黄色黏性分泌物,提示痰栓存在。痰和支气管肺泡灌洗液均培养出曲菌。短时间(2周)使用糖皮质激素,复查胸部CT示原来的右肺上叶结节和下叶肿块影消失,显示显着扩张的支气管,据此过敏性支气管肺曲霉病的诊断可以明确。同时,胸部CT示右上叶有斑点和斑片影,局部肺活检病理报告为坏死性肉芽肿,六胺银染色(+),并见个别菌丝,故合并肺曲霉感染的诊断也可以建立。
六、经验与体会
过敏性支气管肺曲霉病(allergic bronchopulmonaryaspergillosis, ABPA)是机体对定植于气道的曲霉产生的一种复杂超敏反应,常见于哮喘及囊性纤维化患者。典型的ABPA临床特征以哮喘症状为主,且反复发作,支气管阻塞、炎症和黏液嵌塞的反复发作可导致支气管扩张、纤维化和呼吸功能受损。
ABPA通常综合临床表现、影像学和免疫学指标来诊断。影像学上,中央型支气管扩张是ABPA的常见特征,主要累及肺上叶及中叶,还可发现黏液栓的证据,如第二级至第四级支气管黏液嵌塞导致的“牙膏样阴影”或支气管内渗出液伴支气管壁增厚导致的“指套征”阴影(显示为从肺门向外延伸的2-3cm长、5-8mm宽的分枝管状放射密度)。本例表现不甚典型,尤其是右下肺的痰栓,影像学显示为7*4cm的类肿块,门诊曾被怀疑为肺部肿瘤;同时患者既往无哮喘病史,炎症标记物(ESR、CRP)和IgE不高。入院后行支气管镜检查见右侧支气管腔内大量黄色黏性分泌物,结合外周血嗜酸性细胞升高,基本确定ABPA,即开始糖皮质激素治疗。后续痰及支气管肺泡灌洗液培养出曲霉,以及2周后复查胸部Ct提示原先的“肿块”病灶在痰栓排出后显示显着扩张的支气管,进一步证实ABPA的诊断。
ABPA的治疗旨在控制急性炎症的发作和减少进行性肺损伤。对于ABPA急性或反复发作的患者,推荐采用全身性糖皮质激素治疗,初始剂量为泼尼松0.5mg/(kg·d),并在3-6个月期间缓慢减量至停药。该患者应用静脉和口服糖皮质激素治疗后症状及影像学明显改善,黏液栓排出后可见支气管扩张的征象。ABPA激素调整根据血清IgE水平情况逐渐减量,但该患者IgE正常,故主要通过复查胸部影像学检查进行监测糖皮质激素的临床疗效。有研究显示,联合伊曲康唑治疗,可以减少ABPA的复发。
该患者粘液栓周围有斑点斑片影,TBLB病理示坏死性肉芽肿,特染见个别菌丝,六胺银(+),故考虑合并气道侵袭性肺曲霉病。相对于血管侵袭性肺曲霉病,气道侵袭性肺曲霉病,病情较轻。本例使用伊曲康唑6天,因为进行性肝功能受损,换用卡泊芬净治疗5天,感染病灶获得控制。出院后单用糖皮质激素,未继续用抗曲霉治疗,肺部炎症病灶也基本吸收,后续门诊随访显示病灶稳定。
作者:骆煜、金文婷等
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录






#内科治疗#
85
#肿块#
73