Cell Death Dis:LncRNA kcnq1ot1通过介导miR-452-3p/HDAC3/ABCA1通路促进脂质的积累并促进动脉粥样硬化
2020-12-26 MedSci原创 MedSci原创
动脉粥样硬化作为大多数心血管疾病(如心肌梗塞和中风等)的病理基础,其主要特征表现为动脉内膜中过多的脂质沉积。在动脉粥样硬化过程中,内循环中的单核细胞迁移进入内膜下层,并分化为巨噬细胞,这些巨噬细胞通过
动脉粥样硬化作为大多数心血管疾病(如心肌梗塞和中风等)的病理基础,其主要特征表现为动脉内膜中过多的脂质沉积。在动脉粥样硬化过程中,内循环中的单核细胞迁移进入内膜下层,并分化为巨噬细胞,这些巨噬细胞通过摄取大量修饰的脂蛋白形成泡沫细胞,这也是早期动脉粥样硬化病变的一大标志。
ABCA1(ATP结合盒转运蛋白A1)作为一种跨膜蛋白,其介导的胆固醇外排被认为是胆固醇逆向转运(RCT)的第一步以及限速步骤,过量的外周胆固醇通过该步骤被HDL转运至肝脏,最终排泄到胆汁以及粪便中。既往研究显示,在apoE-/-小鼠中上调ABCA1的表达可以促进RCT并减少动脉粥样硬化斑块的面积。因此,更好地了解ABCA1调控的分子机制对于开发新的动脉粥样硬化治疗策略至关重要。
长非编码RNA(lncRNA)是一类长度超过200个核苷酸的RNA,其通过影响染色质修饰、转录或转录后加工,在基因表达的调控中起着至关重要的作用。越来越多的证据表明,lncRNA的异常表达与脂质代谢紊乱和动脉粥样硬化相关。kcnq1ot1(Kcnq1重叠转录本1)是kcnq1基因座中的一个印记反义lncRNA,研究显示其可能是心血管疾病的一个潜在诱因,然而其在动脉粥样硬化中的作用仍然未知。
Kcnq1ot1加重apoE-/-小鼠的动脉粥样硬化
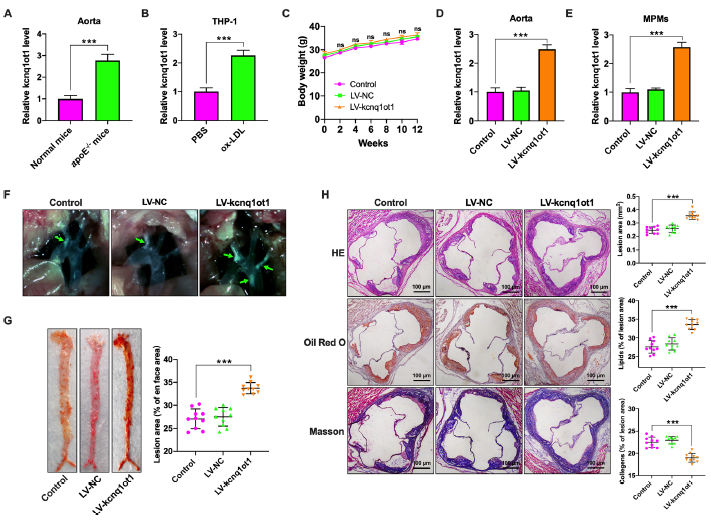
这项研究旨在探讨kcnq1ot1对动脉粥样硬化形成的影响以及潜在的分子机制。研究人员发现,在患有动脉粥样硬化的小鼠主动脉以及脂质相关巨噬细胞中,kcnq1ot1的表达水平显著升高。慢病毒介导的kcnq1ot1过表达能够显著增加以西方饮食喂养的apoE-/-小鼠的动脉粥样硬化斑块的面积,并降低了血浆HDL-C水平和RCT效率。
kcnq1ot1的上调伴随着miR-452-3p和ABCA1的表达水平的降低,但小鼠主动脉和THP-1巨噬细胞中HDAC3的表达水平升高。进一步研究显示,过表达kcnq1ot1能够抑制胆固醇的外排,并促进了THP-1巨噬细胞中脂质的积累。而对应的,敲低kcnq1ot1可防止apoE-/-小鼠的动脉粥样硬化并抑制THP-1巨噬细胞中脂质的积累。
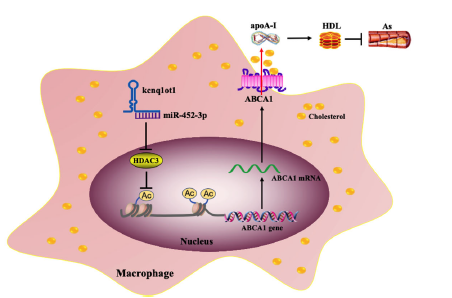
kcnq1ot1促动脉粥样硬化作用的示意图
机制研究显示,kcnq1ot1能够通过竞争性结合miR-452-3p来提高HDAC3的表达水平,并进而抑制ABCA1的表达以及胆固醇的外排。
综上,该研究结果表明,kcnq1ot1通过介导miR-452-3p/HDAC3/ABCA1通路促进巨噬细胞中脂质的积累,并加速动脉粥样硬化的发生发展。
原始出处:
Yu, XH., Deng, WY., Chen, JJ. et al. LncRNA kcnq1ot1 promotes lipid accumulation and accelerates atherosclerosis via functioning as a ceRNA through the miR-452-3p/HDAC3/ABCA1 axis. Cell Death Dis 11, 1043 (09 December 2020).
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#CRN#
86
#Dis#
67
#CEL#
69
#KCNQ1OT1#
86
#miR#
0