Human Reproduction:孕前基因组医学的现状和未来展望
2020-11-18 MedSci原创 MedSci原创
对不孕症患者的全基因组测序(GS)将使针对不孕症表型的全基因组关联研究成为可能,如卵巢早衰、非整倍体风险增加、卵母细胞完全不成熟或囊胚发育失败等,从而促进真正生殖精准医学的发展。

近日,Human Reproduction上新发表了一篇文章综合介绍了孕前基因组学的应用。在这篇文章中,研究者回顾了孕前基因组分析的现有知识和潜在发展,旨在检测生殖和个人健康风险(隐性遗传疾病和医学上可操作的次要发现),预测特定的生殖结果,特别是在试管受精的背景下,生殖遗传风险评估扩大到一般人群和试管受精夫妇,将有助于确定在怀孕前携带隐性突变和亚致死条件的情况。这一办法将增加夫妇的生育自主权,特别是在可以利用植入前基因检测来避免不良条件传播的情况下。此外,对不孕症患者的全基因组测序(GS)将使针对不孕症表型的全基因组关联研究成为可能,如卵巢早衰、非整倍体风险增加、卵母细胞完全不成熟或囊胚发育失败等,从而促进真正生殖精准医学的发展。
如今,基因组检测可以通过孕前载体筛选(PCS)、植入前基因检测(PGT)或怀孕期间的传统产前检测(即羊膜穿刺术和绒毛膜绒毛取样)来准确评估夫妇的生殖风险。从那些已知家庭中存在严重遗传疾病的夫妇无法获得分子诊断来支持生殖管理开始,用于隐性遗传疾病的个人计算机在生殖风险评估方面向前迈出了显著的一步。由于孕前基因检测和随后知情的计划生育,严重的单基因疾病如囊性纤维化(CF)和β-地中海贫血的发生率降低了47%至90%。
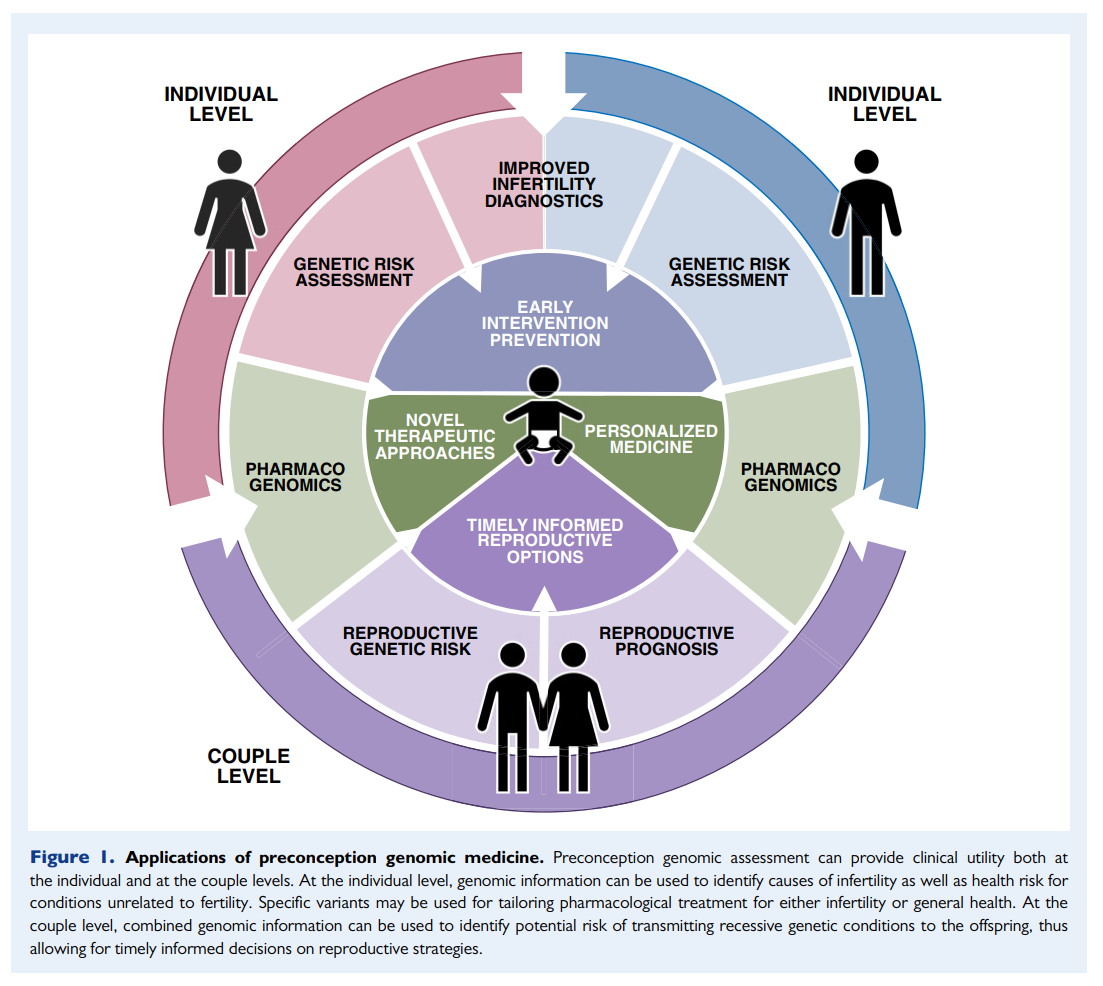
孕前基因医学的应用
影响卵母细胞受精和胚胎发育基本过程的基因突变都是研究不孕症的潜在候选基因。体外受精(IVF)和第二代“试管婴儿”(ICSI)的广泛应用使得研究者有可能在这些过程中发现细微的表型变化(即卵母细胞完全成熟失败、胚胎发育完全停滞),并研究不孕症的遗传原因,否则这些因素将被掩盖。
最近发现的基因缺陷的另一个更广泛的含义是它们可能与卵巢早衰(POI)有关。超过一半的已知单基因原因(19/35)已经被报道为POI的原因,或者敲除小鼠模型表明男性和女性不育。有趣的是,这些基因中绝大多数都参与了减数分裂过程。一个新的结论是,基因咨询不仅应该包括非梗阻性无精子症(NOA)患者的男性亲属,也应该包括女性亲属。
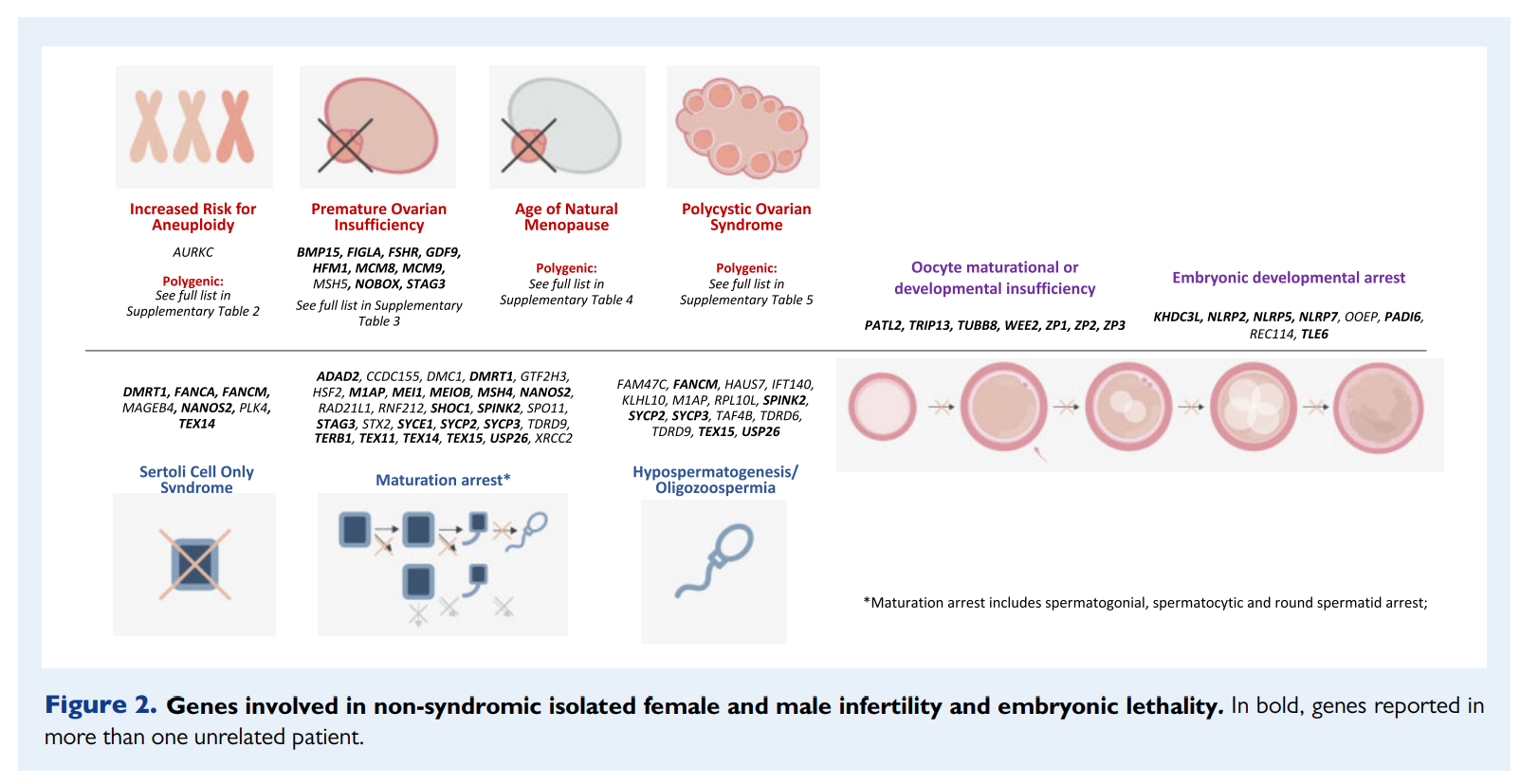
基因参与非综合征孤立的男女不育和胚胎致死率
实现普遍的临床应用和研究转基因的后续益处的道路遇到了一些体制和社会障碍。这些挑战涉及多个方面,不仅包括技术和基础设施方面的缺陷,还包括教育、后勤、经济和社会方面的限制,这些限制需要大量资源和广泛实施。
为了创建有意义的数据存储库,以便更新和进一步分析基因组和医学信息,需要对进行基因分型的患者进行跟踪。出于这个原因, 目前的主要医疗点(即家庭医生)将需要及时与一个集中的电子医疗记录数据库集成,在该数据库中,从GS获得的初始基因组信息与健康状况进展之间的相关性可以持续监测。关键的是,如果法律、道德和社会权利不能与技术基础设施同步发展,这种情况可能会影响基因组方法的合法性,并降低其公众接受度。因此,需要做出重要的努力来开发一个框架,既能保持病人的隐私,又能以有效的方式共享数据。
参考文献:Antonio Capalbo, Maurizio Poli, Antoni Riera-Escamilla, Vallari Shukla, Miya Kudo Høffding, Csilla Krausz, Eva R Hoffmann, Carlos Simon, Preconception genome medicine: current state and future perspectives to improve infertility diagnosis and reproductive and health outcomes based on individual genomic data, Human Reproduction Update, , dmaa044, https://doi.org/10.1093/humupd/dmaa044
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#human#
64
#孕前#
67
#reproduction#
60
#PRO#
58
需要做出重要的努力来开发一个框架,既能保持病人的隐私,又能以有效的方式共享数据。
92