【衡道丨笔记】精准医学时代胃癌外科治疗的挑战和思考——从标准化到个体化
2024-05-05 衡道病理 衡道病理
“复旦大学附属中山医院病理科32周年系列公开课”的课程中,张恒老师为大家带来了精准医学时代胃癌外科治疗的挑战和思考——从标准化到个体化的内容。摘要如下:
精准医学
精准医学:
将遗传学信息用于个体疾病的诊断或治疗;其发展依赖于测序技术的革新、大数据分析技术的出现及相关分子生物学技术的发展(蛋白组、代谢组等)。
精准医学背景下的胃癌外科的机遇与挑战
因期施治,践行精准治疗理念
-
胃癌的微创治疗;
-
进展期局部可切除胃癌的围术期治疗;
-
晚期胃癌的转化治疗:
-
分子诊断与基因分型。
理念为先,精确选择手术范围
-
扩大根治、标准根治、缩小根治。
重视病生,围术期精细化管理
-
外科预康复、全程营养管理。
挑战与机遇之一:内镜微创 VS 腔镜微创
内镜外科:
JCOG0607
治愈性切除(Curative Rep,CR)
1、肠型腺癌
2、pT1a不限大小/pT1b(SM1)≤3cm
3、UL(-)不限大小/UL(+)≤3cm
4、垂直切缘(-)
5、血管脉管浸润(-)
JCOG1009/1010
研究设计:
-
入组标准:cT1aN0M0,含低分化成分(por,sig),<2cm,UL(-);
-
主要研究终点:5-year OS for UD-EGC
Results:
-
根据入组所有病例年龄和性别计算5年期望生存期(expected 5y-OS)为94.9%,考虑5%的置信区间,因此将生存期阈值设定为89.9%;
-
275例UD-EGC中(中位随访69.9个月),5y-OS:99.3%(97.1%-99.8%),5y-RFS: 98.9%,达到研究终点;
-
ESD可成为UD-EGC(cT1a)病人的标准治疗之一。
内镜微创治疗的指征逐渐扩大
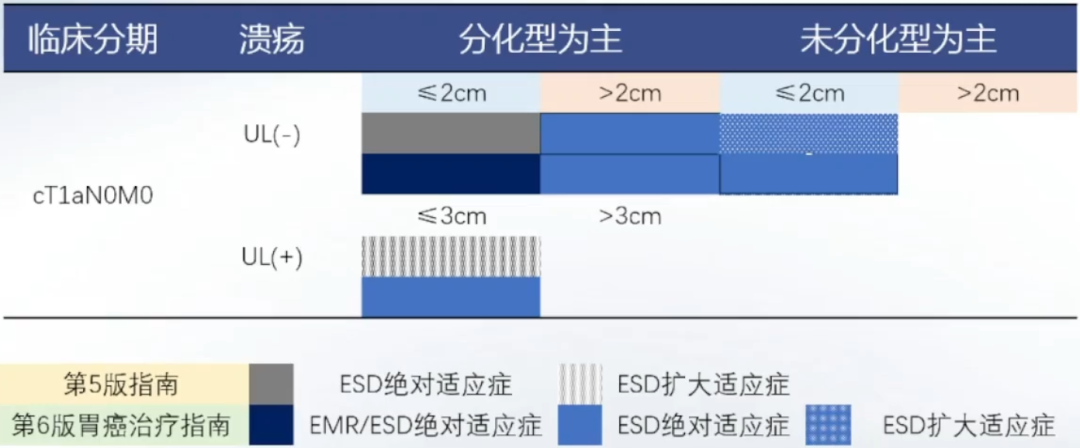
病理诊断新需求
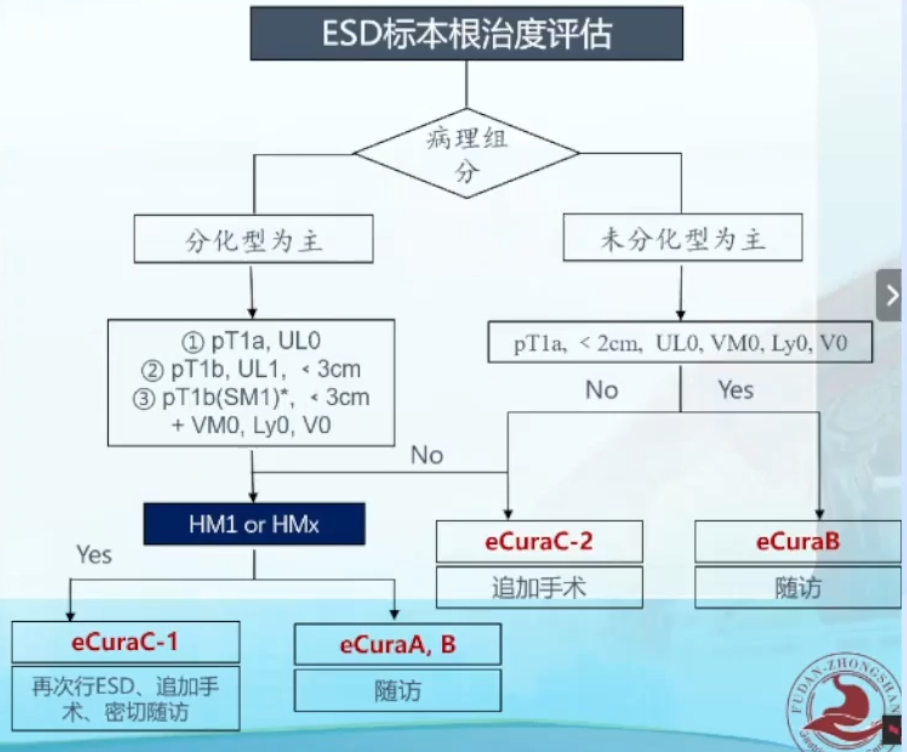
腔镜外科
腔镜微创治疗的循证医学证据
优势:
-
解剖精细
-
快速康复
-
出血少
-
切口小
-
更美观
挑战与机遇之二:功能保留手术
早期胃癌手术新趋向个体化
在保证根治性切除的前提下,缩小手术范围,合理选择重建方式,尽可能保留胃的功能(幽门,残胃容量,胃酸及内因子分泌),以提高患者营养状态及生活质量;
保留功能的胃切除术(function-preserving gastrectomy,FPG
(一)近端胃切除术(proximal gastrectomy,PG)
对于发生在胃上部1/3的EGC,沿胃网膜右动脉淋巴结(No.4d组)、胃右动脉根部淋巴结(No.5组)及幽门下淋巴结(N0.6组)很少发生转移,没有必要对这些淋巴结进行常规清扫。
第5版《日本胃癌治疗指南》推荐:近端胃切除和全胃切除均可作为胃上部1/3的EGC的可选择术式。
(二)保留幽门的胃切除术(pylorus-preserving gastrectomy,PPG)
病灶下缘距幽门超过5cm的EGC,胃右动脉根部淋巴结及幽门下动脉淋巴结(No.6i组)转移非常罕见,有助于对右胃动脉第一个分支及幽门下动脉的保留而不影响幽门部的血供。
PPG作为胃中部1/3的EGC可选术式。
(三)胃局部切除术(local gastrectomy,LG)
腹腔镜-胃镜联合手术治疗(laparoscopic andendoscopic cooperative,LECS)

对于有淋巴结转移的患者,无法达到根治肿瘤的目的。
挑战与机遇之三:扩大手术 VS 综合治疗
外科医生的努力:扩大手术范围?
扩大根治术不能提高进展期胃病远期疗效,且增加术后并发症风险!
策略的演变:围术期综合治疗
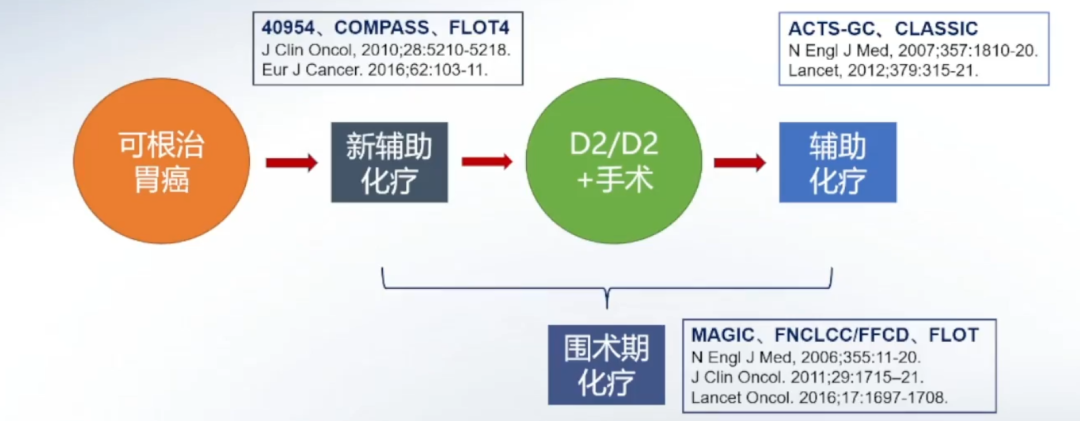
病理诊断新要求
基于术前活检标本的分子诊断:
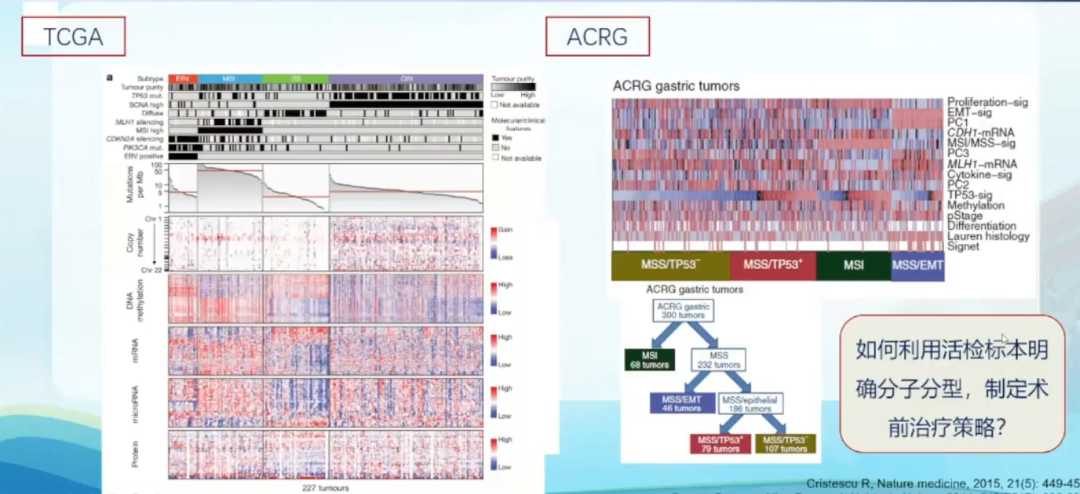
免疫治疗
Neo-planet:新辅助放化疗联合PD-1抗体治疗
局部进展期近端胃癌术前新辅助放化疗联合免疫治疗的前瞻性单中心单臂研究

pCR率33.3%;2年PFS 66.9%;OS 76.1%。
作者:衡道病理
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#胃癌# #外科治疗#
77