Science Signal:Rac1不依赖PI3K和GTPase介导MET驱动的锚定非依赖性细胞生长
2020-06-24 MedSci原创 MedSci原创
锚定非依赖性增殖和细胞迁移对肿瘤生长和转移扩散均至关重要。这些行为都是由生长因子受体信号驱动,一般是激酶PI3K及其下游效应器。但近期研究人员发现,在培养的细胞和移植瘤小鼠中,并非如此……
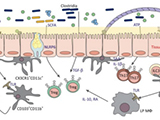
在癌症中,常见受体酪氨酸激酶(PTKs)过表达或突变,PTKs参与驱动肿瘤的生长和转移。在现代的PTK信号模型(包括MET)中,下游磷脂酰肌醇3-激酶 (PI3K) 介导细胞增殖和细胞迁移,而小鸟苷三磷酸酶(GTPase)Rac1介导细胞迁移。
但在培养的NIH3T3和胶质母细胞瘤细胞中,Hervieu等人发现I型PI3K介导致瘤MET诱导的细胞迁移,但不影响锚定非依赖性的生长。相反,Rac1通过不同的方式调控这两个过程。
作为PI3K的下游时,Rac1通过其GTPase活性介导细胞的迁移,而不依赖PI3K时,Rac1通过适配器的功能以GTPase依赖性方式介导锚定非依赖的细胞生长。
通过其RKR模体,Rac1和激酶mTOR形成一个复合物,以促进其向质膜的易位,而其活性则促进培养细胞的锚定非依赖性的生长。用雷帕霉素抑制mTOR可抑制小鼠皮下MET突变的细胞移植物的生长,也可抑制抗MET抑制剂的细胞的生长。
这些发现揭示了Rac1在介导PI3K非依赖的MET-mTOR途径中的GTPase非依赖性的作用,并提出了或可克服癌症患者对RTK抑制剂耐药的替代或联合策略。
原始出处:
Alexia Hervieu,et al. A PI3K- and GTPase-independent Rac1-mTOR mechanism mediates MET-driven anchorage-independent cell growth but not migration. Science Signaling 23 Jun 2020:Vol. 13, Issue 637, eaba8627. DOI: 10.1126/scisignal.aba8627
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Signal#
91
#tPA#
65
#Sign#
78
#GTPase#
70
#MET#
74