SCIENCE 和 SCI TRANSL MED:第一期刊齐发文——迷途的巨噬细胞终于被科学家拯救,成为癌症免疫治疗悍将
2017-05-15 佚名 奇点网
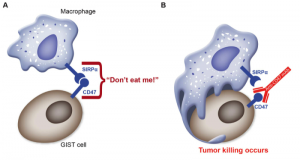
巨噬细胞,作为固有免疫的重要组成部分,通常扮演抵御病原体入侵的“排头兵”和激活适应性免疫的“通信兵”。但是,在肿瘤环境中,它却禁不住肿瘤细胞释放的一些信号分子的“诱惑”,变成了“叛军”:它不仅阻止T细胞等攻击肿瘤细胞,还会分泌生长因子滋养肿瘤细胞,促进肿瘤血管的生成,导致肿瘤细胞转移扩散。据统计,巨噬细胞可占肿瘤总重量的一半!



作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#Transl#
37
#TRA#
32
#SCIE#
33
#Med#
73
学习了分享了
57