Nat Med:基于DNA甲基化技术在真实世界人群中实现宫颈癌的精准筛查
2024-06-24 测序中国 测序中国
研究发现,将WID-qCIN与HPV16和/或HPV18相结合可以检测到93.4%的宫颈上皮内瘤变3级和100%的侵袭性宫颈癌。
宫颈癌是全球女性第四大常见癌症。如果获得早期诊断并及时治疗,宫颈癌是可以治愈的,因此筛查就显得尤为重要。宫颈癌筛查包括人乳头瘤病毒(HPV)检测,如果结果是阳性,则需要进行进一步的细胞学分型。基于细胞学的宫颈筛查需要复杂的基础设施、专业人员和较短的筛查间隔。鉴于细胞学方法的种种缺点和限制,更佳的分诊方法仍是一个未满足的需求。
DNA甲基化(DNA methylation)标志物在癌症诊断、治疗选择及预后评估中的重要性日益凸显。在20年前,科学家们就完成了DNA甲基化检测宫颈(前)癌的概念验证。从那时起,几种基于DNA甲基化的标志物被开发了出来,并在不同的环境中得到了应用。此前,奥地利欧洲转化肿瘤预防和筛查研究所的研究团队及合作者开发了 WID-qCIN 检测,以评估人类基因三个区域的DNA甲基化:DPP6、RALYL和GSX1。
近日,该团队对WID-qCIN检测进行了进一步优化,并将其应用于来自一个真实人群队列的HPV阳性女性,评估了WID-qCIN检测结合HPV16/18基因分型与细胞学分类HPV阳性女性的预测性能。研究发现,将WID-qCIN与HPV16和/或HPV18相结合可以检测到93.4%的宫颈上皮内瘤变3级和100%的侵袭性宫颈癌。WID-qCIN/HPV16/18相结合可以预测69.4%的2级或更严重宫颈上皮内瘤变(CIN2+),细胞学预测仅为18.2%。在6年内,细胞学分诊需要4.1次阴道镜转诊才能检测到一例2级或更严重的宫颈上皮内瘤变,而WID-qCIN/HPV16/18仅需要2.4次阴道镜转诊。以上结果支持了WID-qCIN/HPV16/18方法可以作为HPV阳性女性的更优分诊策略。该成果发表在Nature Medicine上,文章题为“Cervical cancer screening using DNA methylation triage in a real-world population”的文章。

文章发表在Nature Medicine
在2017年1月至3月期间,参加宫颈癌筛查的女性真实队列共包括28,017名患者,年龄≥30岁,共有2377名HPV检测呈阳性的女性进行了细胞学评估。其中711例为细胞学阳性(意义不明或更糟的非典型鳞状细胞,ASC-US+),然后转诊进行阴道镜检查和组织学评估。在前12个月内获得活检的定义为流行病例(306例CIN2+,其中11例为宫颈癌)(图1)。12个月后获得活检的定义为偶发病例(271例CIN2+,其中11例为宫颈癌;第13-72个月期间报告了随访筛查或阴道镜检查数据的流行CIN2+病例被排除在发病率分析之外)。无CIN2+的女性平均随访时间为40.3个月(范围0.3~71.4个月)。
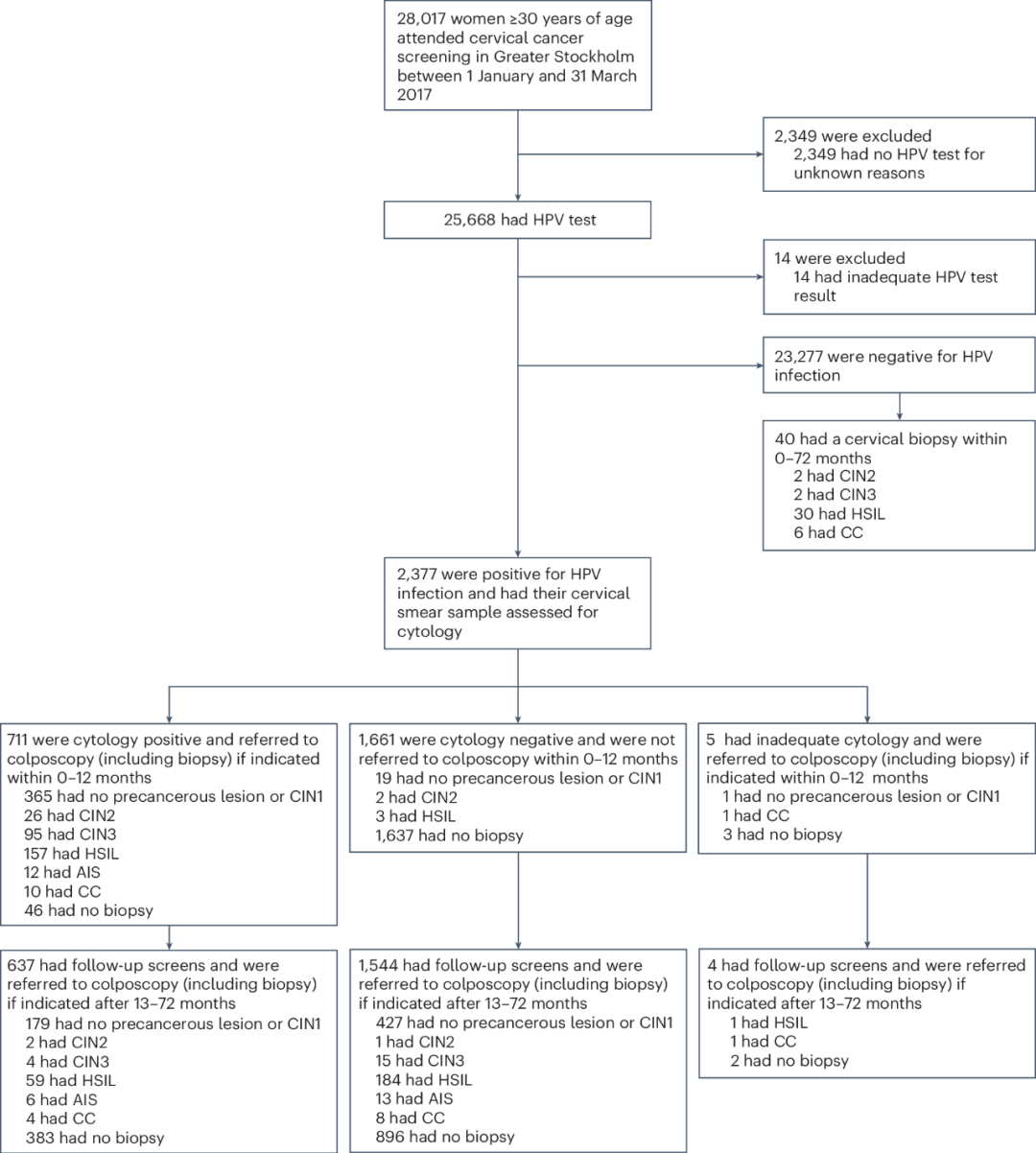
图1. 研究队列人群。
1 流行疾病的检测
根据定义,细胞学检查对组织病理学定义的流行CIN2+病例的敏感性非常高,为98.4%,因为队列中只有细胞学检测阳性的女性会被转诊进行阴道镜检查,从而进行组织病理学活检。虽然HPV16/18基因分型检测到了大约一半的CIN2+病例(53.3%),但单独的WID-qCIN检测(77.0%)或WID-qCIN检测与HPV16/18基因分型相结合(85.9%)的敏感性显著更高(P<0.01)。此外,单独的HPV16/18检测会错过>40%的CIN3病例(敏感性58.9%),单独的WID-qCIN检测(85.7%)或WID-qCIN/HPV16/18(93.4%)的敏感性在CIN3检测中显著更高(P<0.01)。所有宫颈癌均可以通过HPV16/18或WID-qCIN/HPV16/18检测到。单独的WID-qCIN可以检测到10/11例宫颈癌。
细胞学检查(80.1%)、HPV16/18(76.3%)和WID-qCIN(76.9%)的特异性 (≤CIN1)相当。与单独 HPV16/18(P < 0.01)或单独WID-qCIN检测(P < 0.01)相比,WID-qCIN/HPV16/18 的特异性显著较低(60.7%)。WID-qCIN检测与组织学结果之间的关联进一步证实了WID-qCIN检测指示疾病进展的能力。
2 预测宫颈癌发病率
根据基线检测结果,细胞学检查、HPV16/18、WID-qCIN和WID-qCIN/HPV16/18对CIN2+病例的预测分别为18.2%(风险比0.96)、45.6%(风险比2.72)、46.3%(风险比3.01)和69.4%(风险比3.55)(图2)。细胞学检查仅能预测20.0%的宫颈癌病例(即样本采集后12个月以上检测到癌症),而HPV16/18或WID-qCIN分别可以预测54.5%和40.0%的宫颈癌病例。大多数因基线细胞学检测阳性而确定的CIN2+病例是在0–12个月内检测到的,而不是在13–72个月内。此外,基线时细胞学阴性的女性可能在第二轮筛查时(约3年时)检测呈阳性,但在分析中仍被归类为细胞学阴性,所以这两条曲线在3年后不久交叉。
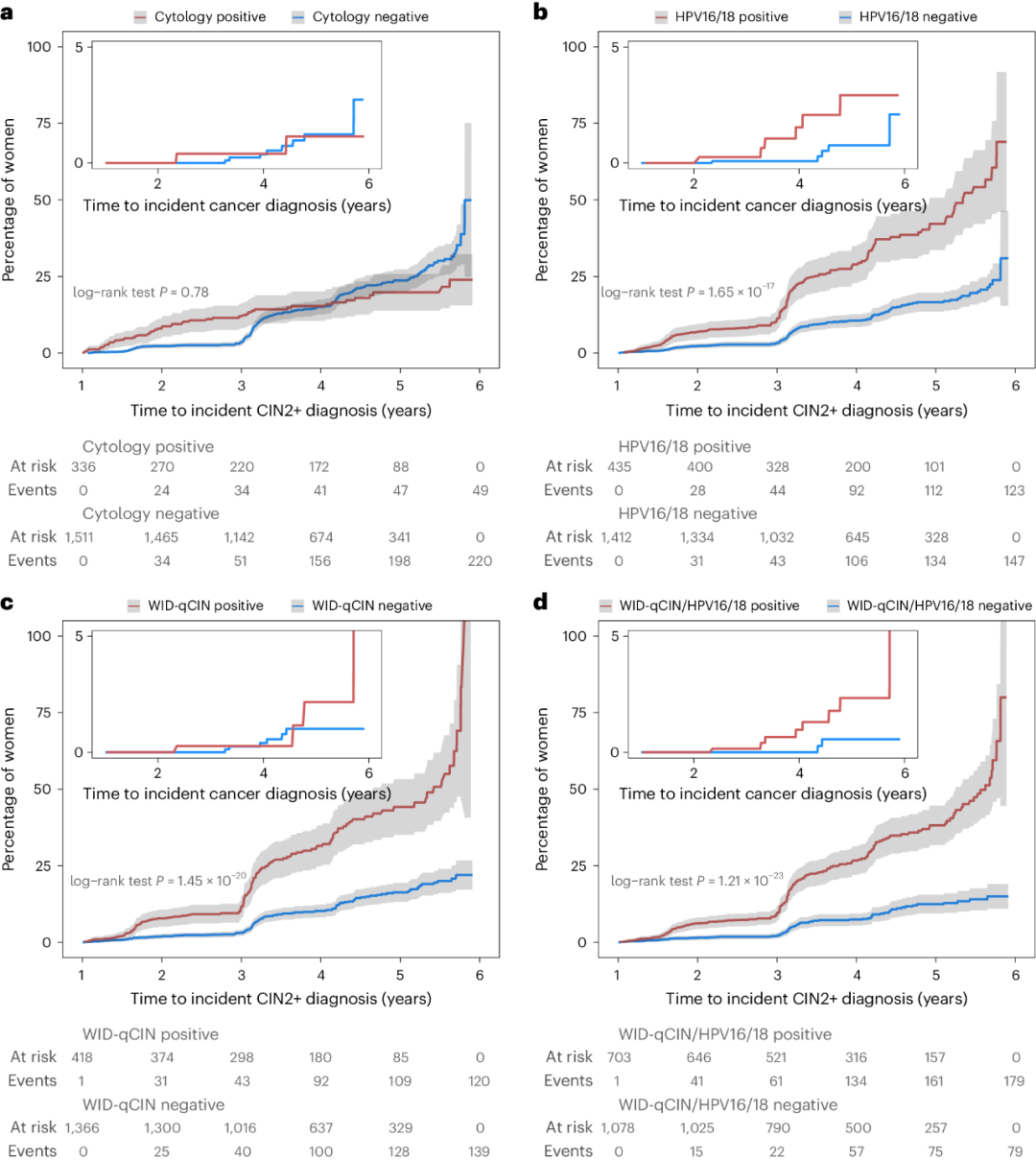
图2. KI-q1-2017队列中CIN2+病例累积发病率的Kaplan–Meier估计。
此外,研究人员还建立了一个患病率-发病率统计模型。首先,该模型考虑了未确诊流行病例的可能性(因为一些偶发CIN2+病例可能是以前未诊断的流行病例);其次,偶发病例是间隔统计的(因为疾病发作只发生在不定期就诊之间)。根据该模型,WID-qCIN检测的风险比为2.31,HPV16/18的风险比为2.47,WID-qCIN/HPV16/18的风险比为2.83(图3)。
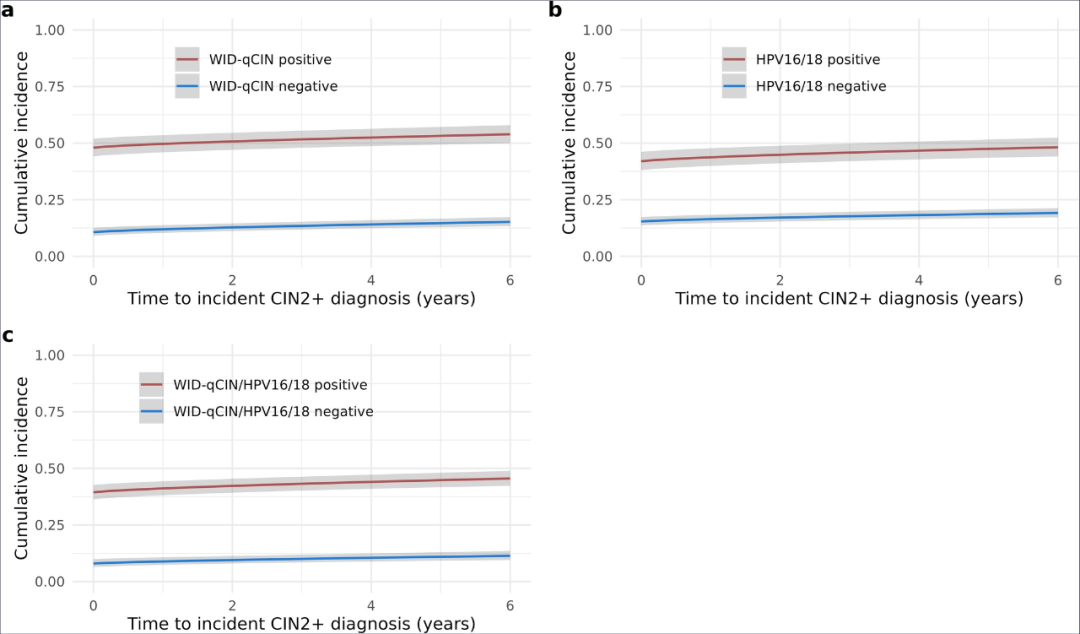
图3. KI-q1-2017队列的Logistic-Weibull混合模型分析。
总的来说,该研究数据表明,在对HPV阳性女性进行检测时,基于DNA甲基化的WID-qCIN检测可以补充HPV16/18基因分型,与广泛使用的细胞学检查相比,其表现有所改善。同时,这种分诊检测方法不依赖于细胞形态的评估,可以单独只对DNA进行检测,说明其适于自采样的筛查策略。WID-qCIN与HPV16/18筛查相结合的实施有助于避免在自身样本中HPV检测呈阳性后对患者进行重新采样的问题。
该研究团队此前已经开发了一种基于DNA甲基化的检测方法,名为WID-qEC(来自Sola Diagnostics公司的WID-easy),用于帮助奥地利人群子宫内膜癌和其他形式子宫癌的筛查分诊。根据欧洲体外诊断设备法规第5条,WID-easy检测目前可以作为内部检测方法进行应用。
文章通讯作者Widschwendter教授表示:“妇科医生现在有了简单的检测方法,可以评估异常出血或HPV女性罹患子宫癌症的风险。WID-qCIN检测用于宫颈癌症筛查的前瞻性临床试验目前正在进行中。所以,我们对更佳的宫颈癌筛查策略抱有充分的信心。”
参考资料:
1.Schreiberhuber, L., Barrett, J.E., Wang, J. et al. Cervical cancer screening using DNA methylation triage in a real-world population. Nat Med (2024). https://doi.org/10.1038/s41591-024-03014-6
2.https://www.genomeweb.com/cancer/cervical-cancer-screening-study-points-potential-dna-methylation-based-triage-strategy
作者:测序中国
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#宫颈癌# #DNA甲基化#
0