韩雅玲:临床研究的指导原则(视频)
2012-06-26 MedSci MedSci原创
在第十届中国介入心脏病学大会上,沈阳军区总医院韩雅玲教授在第四届临床研究专题研讨峰会上介绍了临床研究的指导原则,包括药物临床试验质量管理规范(GCP)、人体试验委员会(IRB)、知情同意、培训等内容。 韩教授指出,临床研究是以人为研究对象,其结果应用于人,首先应严格遵守赫尔辛基宣言,并遵循GCP。GCP是临床试验全过程的标准规定,包括方案设计、组织实施、监察、稽查、记录、分析总结和

在第十届中国介入心脏病学大会上,沈阳军区总医院韩雅玲教授在第四届临床研究专题研讨峰会上介绍了临床研究的指导原则,包括药物临床试验质量管理规范(GCP)、人体试验委员会(IRB)、知情同意、培训等内容。
韩教授指出,临床研究是以人为研究对象,其结果应用于人,首先应严格遵守赫尔辛基宣言,并遵循GCP。GCP是临床试验全过程的标准规定,包括方案设计、组织实施、监察、稽查、记录、分析总结和报告,以使数据及结果的真实性和准确性、受试者的权益、人格及隐私得到保护。
研究设计的GCP标准要求科学性和可行性,应制定研究方案、研究者手册,有充足的资源和随机化或盲法过程。组织实施的GCP包括经管理部门和IRB批准,遵循研究方案,受试者签署知情同意书,保护受试者隐私。还需要进行医疗处置及收集不良事件,研究药品使用及管理记录,进行研究者的资质认定及培训。
在临床研究的记录中,完成病例报告表(CRF)是最主要的环节,另外还需要注意数据处理、安全性、稽查索引等的GCP标准。在研究中,需要向研究发起者、伦理委员会、行政管理部门和其他研究者提供不良事件报告、中期评估、进展报告、最终报告和监察/稽查报告。
IRB极独立的伦理委员会(IEC)在临床试验中保护受试者方面发挥重要作用。IRB对研究方案进行审查,以确保受试者知情同意、受试者不会遭受不合理的风险、研究方案具有科学性。IEC是临床试验中保护人类受试者的基石。知情同意应在任何研究步骤之前进行,如采血(用于病例筛选而不是常规医疗行为)、问卷调查等。但在紧急条件下允许有特例。
临床研究流程如图所示:
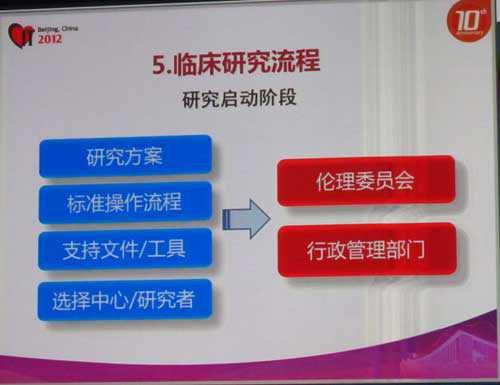
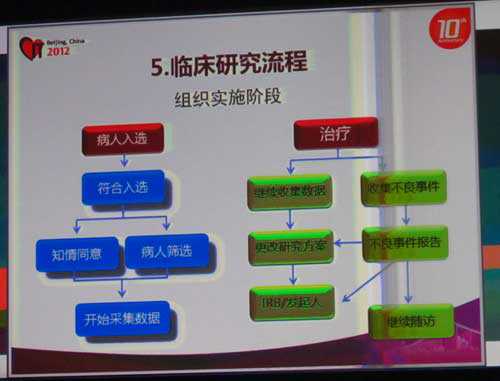
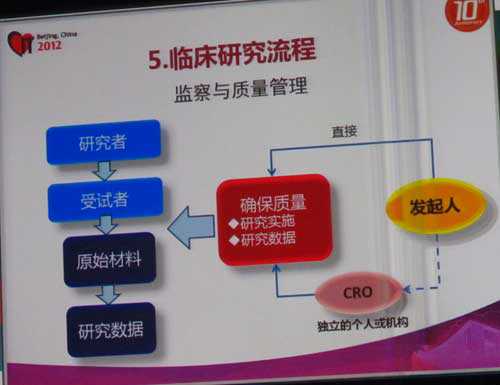

视频观看:
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







应该重点学习如何做科研
134
值得学习!
175
#韩雅玲#
60