欧盟监管机构开始审查LEO的IL-13单抗tralokinumab,治疗特应性皮炎
2020-06-13 MedSci原创 MedSci原创
traokinumab治疗16周后,患者湿疹面积和严重程度指数得分改善了75%及以上。
欧盟药品监管机构开始对LEO Pharma的白细胞介素13(IL-13)单抗tralokinumab治疗中度至重度特应性皮炎进行审查。
该药物是一种全人源的单克隆抗体,可特异性中和IL-13细胞因子——特应性皮炎中潜在的关键驱动因素。
该申请是基于关键的ECZTRA 1、2和3期III期研究的数据,该研究评估了traokinumab的功效和安全性。
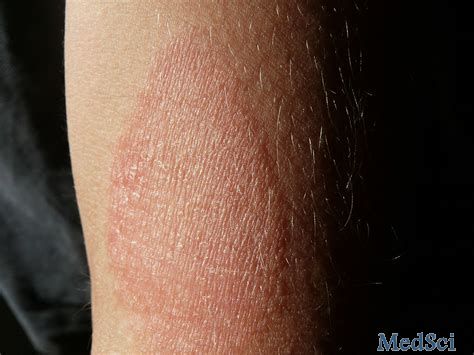
在试验中,traokinumab治疗16周后,患者表现出清晰或几乎透明的皮肤,在第16周时湿疹面积和严重程度指数(EASI)得分与基线相比至少变化了75%及以上。
此外,总体不良事件发生率与安慰剂相当。
LEO Pharma全球研究与开发执行副总裁KimKjøller说:“患有特应性皮炎的人们通常面临巨大的身体、社交和情感挑战。”
“由于特应性皮炎是一种异质性疾病,我们将重点放在具有针对性的治疗方法上,以满足个体需求并减轻疾病负担。”
原始出处:
http://www.pharmatimes.com/news/eu_regulators_agree_to_review_leos_dermatitis_drug_1342110
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#TRA#
53
#mAb#
42
#IL-13单抗#
69
#监管#
64
#IL-1#
51