FDA批准的PD-1适应症及使用剂量总览
2017-09-28 佚名 全球肿瘤医生网
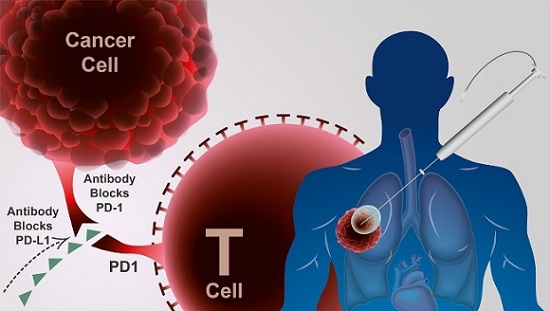
PD-1/PD-L1免疫疗法(immunotherapy)是当前全世界备受瞩目、广为研究的新一类抗癌免疫疗法,旨在充分利用人体自身的免疫系统抵御、抗击癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力,实质性改善患者总生存期。目前,全球最热门的两大PD-药物KEYTRUDA(pembrolizumab)”、“Opdivo(nivolumab)”自2014年以来,一路
h: 100%; box-sizing: border-box !important; word-wrap: break-word !important;">治疗后出现进展且无其他治疗方案的无法切除或转移的微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)的成人或儿童实体瘤患者,或同时包括在先前接受氟嘧啶类化疗药物、伊立替康以及铂化疗后疾病进展的高度微卫星不稳定(MSI-H)或错配修复缺陷(dMMR)的结直肠癌患者
成人:200mg
儿童:2 mg/kg(最多200mg)
每三周注射一次。
直到病情进展或出现不可耐受的毒性,或持续治疗达到两年
2017年9月22日
治疗复发性局部晚期或转移性胃癌及胃食管交界处腺癌(GEJ)的患者。且肿瘤表达PD-L1的患者
200mg,30分钟以上静脉注射,每三周注射一次,直到病情进展或出现不可耐受的毒性,或持续治疗达到两年


FDA批准时间 | 适应症 | 使用剂量 |
2014年12月22日 | 不可切除或转移性黑色素瘤及ipilimumab治疗后病情进展的BRAF V600E突变患者 | 3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
2015年3月4日 | 铂类化疗后进展的转移性非小细胞鳞癌(NSCLC)患者 | 3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
2015年9月30日 | 与ipilimumab联合用于治疗BRAF V600野生型,不可切除或转移性黑色素瘤患者 | nivolumab 联合ipilimumab:nivolumab 1 mg / kg,静脉滴注60分钟,随后注射ipilimumab,每3周4次。nivolumab 单药:33 mg/kg ,60分钟以上静脉注射,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
2015年10月9日 | 铂类化疗后进展的转移性非小细胞癌(NSCLC)患者 | 3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
2015年11月23日 | 既往接受过抗血管生成疗法的进展期肾细胞癌 | 3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
2016年5月17日 | 自体干细胞移植和本妥昔单抗治疗或三线及以上系统治疗后出现复发获进展的经典型霍奇金淋巴瘤 | 3 mg/kg ,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
2016年11月10日 | 治疗含铂化疗后出现局部进展的复发或转移性头颈鳞状细胞癌(HNSCC) | 3 mg/kg ,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
2017年2月2日 | 含铂化疗期间或含铂辅助化疗、新辅助化疗一年内出现疾病进展的局部晚期或转移性尿路上皮癌 | 240mg,每两周注射一次 |
2017年7月31日 | 氟尿嘧啶,奥沙利铂和伊立替康治疗后出现进展的MSI-H或dMMR转移性结直肠癌(成人或≥12岁儿童) | 240mg,每两周注射一次 |
2017年9月22日 | 接受过索拉菲尼(多吉美)治疗后的肝细胞癌患者 | 240mg,每两周注射一次 |
FDA批准时间 | 适应症 | 使用剂量 |
2014年9月4日 | 不可切除或转移性黑色素瘤及ipilimumab治疗后病情进展的BRAF V600E突变患者 | 2 mg/kg ,30分钟以上静脉注射,每三周注射一次 |
2015年10月2日 | PD-L1阳性、含铂化疗进行或术后疾病进展的转移性非小细胞肺癌患者
| 2 mg/kg ,30分钟以上静脉注射,每三周注射一次 |
2016年8月5日 | 治疗含铂化疗后出现局部进展的复发或转移性头颈鳞状细胞癌(HNSCC) | 200mg,30分钟以上静脉注射,每三周注射一次 |
2017年3月14日 | 治疗难治性经典霍奇金淋巴瘤(cHL)的成人和儿科患者,或经三次以上治疗复发的患者 | 成人:200mg 儿童:2 mg/kg(最多200mg) 每三周注射一次 |
2017年5月10日 | 联合培美曲塞和卡铂治疗以前未经治疗的转移性非鳞状非小细胞肺癌(NSCLC) | 200mg,每三周注射一次,直到病情进展或出现不可耐受的毒性,或持续治疗达到两年 |
2017年5月18日 | 一线治疗不合适铂类药物化疗的局部晚期或转移性尿路上皮癌,以及二线治疗铂类药物化疗后疾病进展或术前/术后接受铂类药物化疗12个月内疾病恶化的局部晚期或转移性尿路上皮癌 | 200mg,30分钟以上静脉注射,每三周注射一次 |
|
作者:佚名 版权声明: 本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 在此留言 相关资讯Nat Immunol:CD8αα上皮内淋巴细胞来源于两个主要的胸腺前体TCRαβ+CD4-CD8α+CD8β-肠上皮内淋巴细胞(CD8αα IELs)是一种胸腺来源的数量丰富的T细胞,保护肠屏障表面。本研究旨在通过分析胸腺IEL前体的成熟、定位和迁出来更好的定义这一群体。这项研究通过对激酶TAK1的依赖性和严格的细胞系-排除标准,在TCRαβ+CD4-CD8-胸腺细胞中定义了两个前体细胞群。这些IEL前体细胞群包括一个初期的PD-1+细胞群和一个随年龄积累的T-be CLIN CANCER RES:肺癌TP53及KRAS突变预测阻断PD-1免疫治疗反应临床研究表明在非小细胞肺癌(NSCLC)中靶向PD-1及PD-L1信号通路治疗具有前景,但是能够预测对检查点抑制剂治疗有反应的患者特征尚缺乏研究。CLIN CANCER RES近期发表了一篇文章,研究TP53及KRAS突变预测PD-1免疫治疗反应。 NEJM:“广谱抗癌药”PD-1抑制剂治疗纵隔灰区淋巴瘤有效纵隔灰区淋巴瘤是指介于结节硬化型霍奇金淋巴瘤与原发纵隔大B细胞淋巴瘤之间的一种淋巴瘤类型。其预后要差于结节硬化型霍奇金淋巴瘤及原发纵隔大B细胞淋巴瘤。美国国立癌症中心的Wilson教授领导的研究表明,DA-EPOCH-R治疗纵隔灰区淋年巴瘤有效,但从长期预后来看,5年的无进展生存率与总生存率为62%与74%, 提示部分患者治疗不佳,且挽救治疗作用有限。近期,Wilson教授在新英格兰医学杂志上报道 重要警示!2篇论文证实:这种PD-1抗体联合疗法,效果不佳还“有害”PD-1抗体是最成功的癌症免疫疗法药物之一,目前已被FDA批准用于包括黑色素瘤、非小细胞肺癌、肾细胞癌、经典型霍奇金淋巴瘤、头颈癌、膀胱癌、结直肠癌等在内的多个适应症。然而,这类免疫检查点抑制剂也有它的局限。目前,仅约有15%-25%的患者能够响应这类药物。 CLIN CANCER RES:黑色素瘤治疗期间PD-L1表达改变可以预测PD-1治疗反应利用免疫检查点抑制阻断PD-L1/细胞毒T细胞PD-1信号可以改善肿瘤患者预后。CLIN CANCER RES近期发表了一篇文章,研究黑色素瘤患者接受抗PD-1治疗时肿瘤PD-L1表达以及肿瘤相关免疫细胞密度,并将其与治疗反应相联系。 JAMA Neurol:PD-1单抗治疗相关神经系统并发症及其处置方法研究发现,神经系统不良反应与抗PD-1治疗相关,表现出多种表型以及频繁的神经并发症,尽管上述并发症较为罕见,但PD-1单抗疗法的并发症频率显著高于其他肿瘤疗法,且发作时间不可预知,进展迅速且致命。研究认为出现PD-1治疗相关的神经系统并发症后应立即终止治疗,必要时采取免疫应激治疗 |








#FDA批准#
28
#适应症#
34