重要警示!2篇论文证实:这种PD-1抗体联合疗法,效果不佳还“有害”
2017-09-06 佚名 生物探索
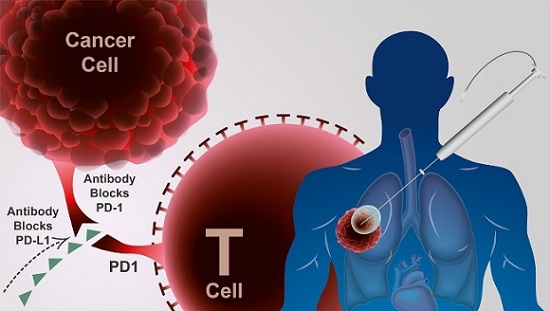
PD-1抗体是最成功的癌症免疫疗法药物之一,目前已被FDA批准用于包括黑色素瘤、非小细胞肺癌、肾细胞癌、经典型霍奇金淋巴瘤、头颈癌、膀胱癌、结直肠癌等在内的多个适应症。然而,这类免疫检查点抑制剂也有它的局限。目前,仅约有15%-25%的患者能够响应这类药物。

作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#联合疗法#
23
#PD-1抗体#
31
学习了.谢谢分享
59