Nat Commun:微生物所揭示结核分枝杆菌与宿主相互作用的分子机制
2017-08-18 佚名 中国生物技术网
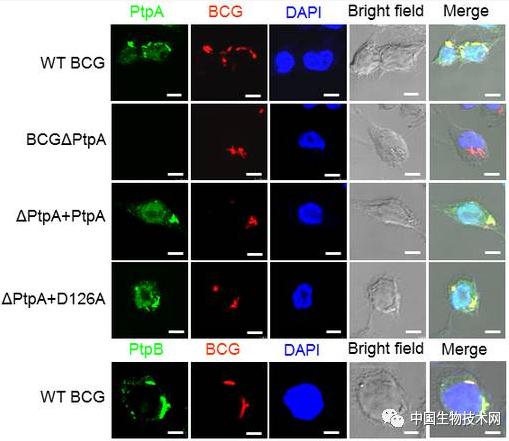
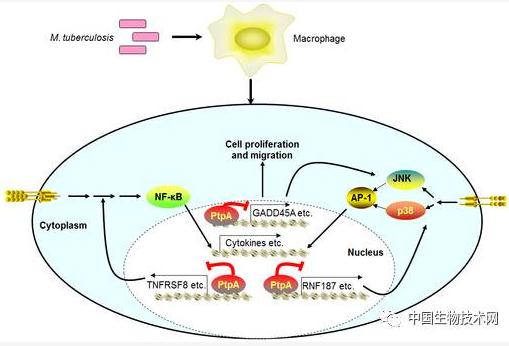
由结核分枝杆菌(Mycobacterium tuberculosis, Mtb)引起的结核病是一种古老的慢性传染病,并且至今仍是全球死亡人数最多的单一传染病。据世界卫生组织(WHO)报道:2015年全球有1040万新发结核病患者,有180万人死于结核病。
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#COMMUN#
39
学习学习.了解了解
79
#分枝杆菌#
40
#微生物#
45
#相互作用#
30