Alzheimers Dement:阿尔茨海默病病理学对生物学和临床进展有独特贡献
2023-03-02 影像小生 MedSci原创
针对Aβ和tau的治疗可能部分阻断AD进展。
阿尔茨海默病(AD)是一种神经退行性疾病,其特征是具有三个神经病理特征,包括淀粉样β(Aβ)斑块、tau神经纤维缠结和神经退行性变,其中Aβ沉积可能引发tau增殖和神经炎改变的级联,进而导致AD进展。美国国家老龄化研究所-阿尔茨海默氏症协会(NIA-AA)先前提出了一个基于生物标志物的框架,该框架明确定义了AD的机制背景,与假设相一致。因此,NIA-AA框架由三个生物标志物组成:A多聚化Aβ(脑脊液[CFS]中Aβ水平较低或Aβ正电子发射断层显像(PET)沉积);T-多聚化tau(CSF中较高的磷酸化tau[p-tau]水平或PET上的tau积聚);自发布以来,NIA-AA研究框架为AD的标准化表征带来了巨大的进步。
淀粉样β(Aβ)沉积、tau积聚和脑萎缩依次发生,但阿尔茨海默病(AD)病理对生物学和临床进展的贡献仍不清楚。
复旦大学华山医院脑启发智能科学技术研究院神经内科Wei Cheng团队分别从哈佛老化大脑研究(HABS)和阿尔茨海默病神经成像倡议(ADNI)数据集对Aβ-正电子发射断层扫描(PET)、tau PET、磁共振成像和认知功能进行了纵向评估,共纳入290名和70名参与者。使用偏最小二乘结构方程模型(PLS-SEM)确定AD病理对生物学和临床纵向变化的贡献。研究结果发表在Alzheimers Dement 。

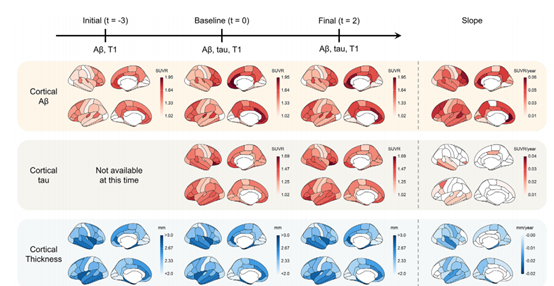
图1.HABS的研究设计和Aβ、tau和皮质厚度的时空进展。
HABS的基线被定义为tau PET图像最初可用的时间(t=0,其中t表示从基线开始的时间,单位为年)。前三列显示了Aβ、tau和皮质厚度的时空变化。每个大脑区域在三个时间点的平均值来自参与者。FDR校正后,通过线性混合模型计算的Aβ和tau显著增加率和皮质厚度显著减少率(P<0.05)以及年龄、性别、种族、教育年限和载脂蛋白Eε4状态的控制协变量显示在最后一列。
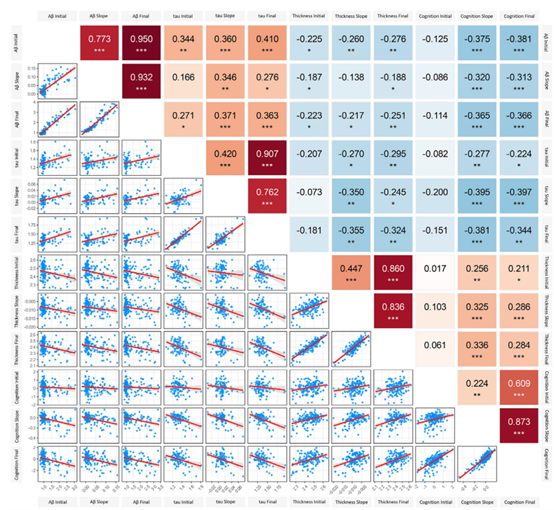
图2.影像生物标志物的初始值、斜率和最终值与认知之间的关联模式。
淀粉样β蛋白(Aβ)、tau和皮质厚度变化率显著的大脑区域被选为感兴趣的元区域,并计算每个参与者在不同时间点的各种成像数据的汇总值。线性混合模型用于估计个体认知斜率和成像数据的汇总值。在控制年龄、性别、种族、教育年限和载脂蛋白Eε4状态作为协变量后,Aβ、tau和皮质厚度的认知初始值、斜率和最终值与成像总结值之间的部分相关性显示在上三角中。对多次比较使用错误发现率校正(P<0.05)。下面的三角形中显示了一系列带有拟合线的散点图,其中散点图中的每个点代表一个参与者。(*表示0.01≤P<0.05**表示0.001≤P<0.01,***表示0≤P<0.001)。
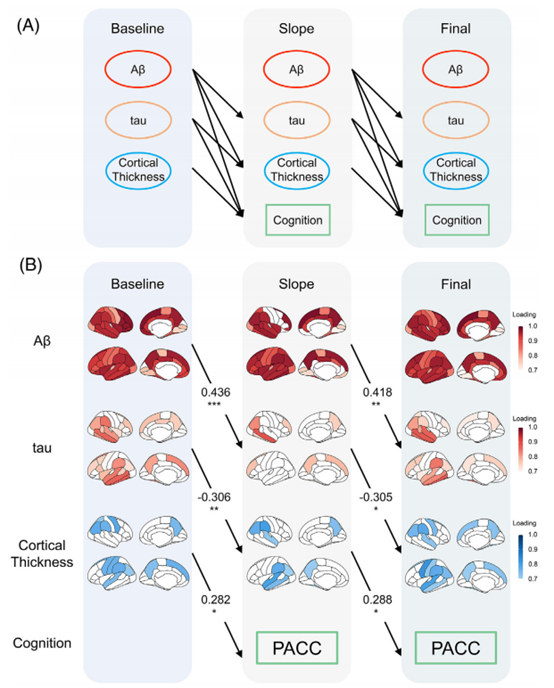
图3.哈佛老化大脑研究中的偏最小二乘结构方程模型。
基线时的Aβ与tau斜率显著正相关(β=0.436,P<0.001),而最终时间点的Aβ斜率也与tau显著正相关,(β=0.418,P=0.001)。基线时的tau与皮质厚度斜率显著负相关(β=−0.306,P=0.004),tau斜率也与最终时间点的皮质厚度显著负相关(β=−0.305,P=0.016)。基线时的皮质厚度与认知斜率显著正相关(β=0.282,P=0.040),皮质厚度的斜率也与最终时间点的认知显著正相关(β=0.288,P=0.040)。
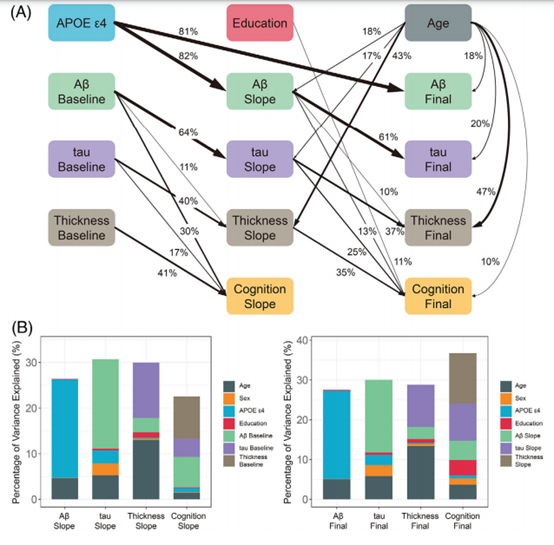
图4.量化通过影像生物标志物和AD风险因素解释的方差比例。(A) PLS-SEM中潜在变量和观察变量解释的方差百分比(仅显示解释10%以上方差的变量)。(B) PLS-SEM中斜率和最终时间点的成像生物标志物和AD风险因素分别解释的方差百分比的堆积条形图。
上图显示了PLS-SEM中潜在变量和观察变量解释的方差百分比;仅绘制了解释10%以上方差的变量。PLS-SEM解释了认知斜率中23%的方差,基线Aβ、tau和皮质厚度分别独立解释了30%、17%和41%的方差。APOEε4状态解释了Aβ斜率82%的方差。基线Aβ和年龄分别解释了tau斜率变化的64%和17%。年龄、基线tau和Aβ分别解释了皮质厚度斜率的43%、40%和11%。在最后一个时间点,PLS-SEM解释了37%的认知差异,Aβ、tau和皮质厚度的斜率分别独立解释了13%、25%和35%的差异,教育和年龄的AD风险因素分别解释了11%和10%的差异。同时,APOEε4状态解释了Aβ81%的变异。β斜率和年龄分别解释了tau方差的61%和20%。年龄、tau斜率和Aβ分别解释了皮质厚度变化的47%、37%和10%。
综上所述,这项研究为基于AD假说的生物标志物框架提供了有力支持。基线时的Aβ负荷与导致最终皮质厚度减少的tau累积斜率相关,而基线时的tau积累与导致最终认知能力下降的皮质厚度减少相关。通过评估AD连续体中生物标志物的动态轨迹,该研究还首次量化了AD病理的独特贡献比例,其中结合风险因素解释的斜率方差百分比为Aβ沉积26%,tau积累31%,脑萎缩30%,认知功能下降23%。更具体地说,Aβ负荷占tau累积解释方差的64%,tau累积占皮质厚度解释方差的40%,皮质厚度占认知下降解释方差的41%。
该研究强调了AD病理对生物学和临床进展的独特贡献。针对Aβ和tau的治疗可能部分阻断AD进展。
原文出处:
Zhang W, Wang HF, Kuo K, et al. Contribution of Alzheimer's disease pathology to biological and clinical progression: A longitudinal study across two cohorts [published online ahead of print, 2023 Feb 25]. Alzheimers Dement. 2023;10.1002/alz.12992. doi:10.1002/alz.12992
作者:影像小生
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








我国卒中患病总人数超2800万,每5位死亡者中就至少有1人死于卒中;河南省年发病率为十万分之三百,相当于每小时约有36人突发脑卒中;其中,很大一部分患者,因错失了最佳溶栓、取栓治疗时间而致残、致死。
63