Adv Sci:南京医科大学唐卫卫等团队合作揭示间隙连接蛋白β2在促进肝癌进展中的作用机制
2024-08-22 iNature iNature
该研究通过单细胞RNA测序发现间隙连接蛋白β2(GJB2)在恶性细胞中高度富集,GJB2高表达提示预后较差。
尽管近年来肝细胞癌的治疗取得了实质性的突破,但许多患者被诊断时已是中晚期,无法进行手术切除,因此寻找有效的肝细胞癌治疗靶点至关重要。
2024年8月20日,南京医科大学唐卫卫、Wang Hanjin、宋进华、上海交通大学Li Zhouxiao、天津中医药大学Liu Li共同通讯在Advanced Science 在线发表题为“GJB2 Promotes HCC Progression by Activating Glycolysis Through Cytoplasmic Translocation and Generating a Suppressive Tumor Microenvironment Based on Single Cell RNA Sequencing”的研究论文。该研究通过单细胞RNA测序发现间隙连接蛋白β2(GJB2)在恶性细胞中高度富集,GJB2高表达提示预后较差。
与正常肝组织相比,GJB2在肝细胞癌癌细胞中的定位发生了改变,在癌细胞中GJB2倾向于定位于细胞质和细胞核,而在正常组织中GJB2主要定位于细胞膜。GJB2与糖酵解相关,通过诱导IκBa泛素化降解来促进NF-κB通路,并激活HIF-1α/GLUT-1/PD-L1通路。此外,GJB2敲低重塑了肿瘤免疫微环境,而丹酚酸B抑制了GJB2的活性。总之,GJB2通过胞质转位激活糖酵解并产生抑制性肿瘤微环境来促进HCC进展。丹酚酸B抑制GJB2的表达并增强抗PD1治疗的敏感性,这可能为HCC新型联合治疗策略的开发提供参考。

肝癌在癌症类型中发病率排名第八,是导致死亡的第三大原因。值得注意的是,HCC占所有肝癌病例的80%。2019年全球约有747000例HCC病例,自1990年以来增长了70%,该疾病导致480000人死亡。HCC的治疗方案可能非常有效,尤其是在早期诊断时。然而,肿瘤复发仍然是一个重大挑战。可用的治疗方式包括经动脉化疗栓塞术(TACE)、肝移植、消融治疗和手术切除。不幸的是,由于疾病的无症状性质,大多数HCC患者都处于晚期。对于这些人来说,全身用药通常是切实可行的选择,因为手术替代方案可能不可行。
近年来,癌症免疫疗法,尤其是免疫检查点抑制剂(ICI)的使用,极大地改变了HCC的临床治疗。贝伐单抗(抗VEGF)和阿特珠单抗(抗PD1)联合使用已被证明比一线疗法索拉非尼更有效。尽管取得了这些进展,但由于HCC经常复发和药物耐药性,它仍然是最具挑战性的癌症之一。不幸的是,相当一部分HCC患者要么出现免疫相关的副作用,要么无法从这些免疫疗法中受益。尽管如此,免疫疗法的快速发展为HCC患者带来了新的希望,尽管进一步的研究对于提高治疗敏感性至关重要。
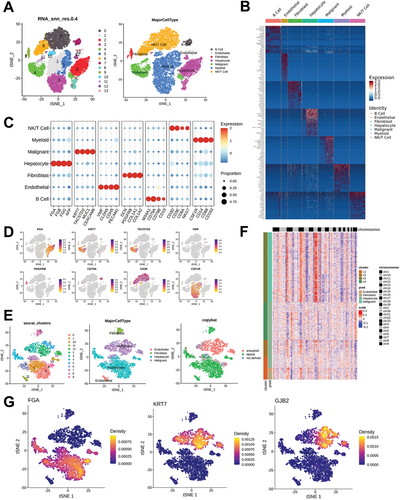
根据scRNA-seq,GJB2在肿瘤细胞中特异性富集(图源自Advanced Science )
快速发展的单细胞RNA测序(scRNA-seq)为遗传学和肿瘤生物学提供了深刻的启示,证明了其表征单细胞表观基因组、转录组和基因组的能力,使我们能够研究肿瘤生长各个阶段发生的动态变化,甚至包括晚期转移性癌症的复杂情况。此外,scRNA-seq的临床应用可以深刻改变我们治疗癌症的方式。事实上,scRNA-seq开创了生物学探索的新时代。尽管面临持续的挑战,但我们始终坚信,这项技术所展示的能力将不断推动创新并为现有的难题提供解决方案。在此过程中,它有望阐明疾病的错综复杂,丰富我们的理解并为变革性突破铺平道路。
这里必须提到的是,基于scRNA-seq技术的发展,肿瘤微环境(TME)的阐明已经取得了巨大进展,并且发现了许多新的靶点。本研究基于scRNA-seq数据发现GJB2特异性富集于恶性细胞中,而非免疫细胞等其他细胞。有趣的是,与正常肝组织相比,GJB2在HCC癌细胞中的定位发生了改变。在癌细胞中,GJB2倾向于位于细胞质和细胞核中,而在正常组织中,GJB2主要位于细胞膜上。GJB2与糖酵解密切相关,促进NF-κB通路,激活HIF-1α/GLUT-1,增加PD-L1表达。免疫共沉淀(Co-IP)结果显示,GJB2通过募集ASB2蛋白促进IκBa泛素化降解,进而激活NF-κB通路。质谱流式细胞术结果显示,GJB2敲低重塑TME,更有利于抗PD1治疗。此外,作者进行了虚拟筛选,获得了GJB2的小分子抑制剂丹酚酸B,并验证了其在体外和体内抑制HCC生长的能力。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202402115
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#肝癌# #间隙连接蛋白β2#
0