华中科大罗志强、张丽/宾大蒋圆闻《自然·通讯》:高精度生物电子水凝胶用于慢性神经调控
2024-09-18 BioMed科技 BioMed科技
通过在网络形成过程中引入多功能分子调节剂,我们通过微调反应动力学和导电网络内的多尺度相互作用,优化了水凝胶的可注射性和导电性。同时,在不损害其可注射性的情况下,实现了水凝胶的机械和电气稳定性。
电疗药物通过选择性调节目标器官附近的周围神经,为治疗难治性疾病提供了希望。然而,这些神经的尺寸小且性质脆弱,使得简化神经电极的固定和稳定电耦合界面面临挑战。在这里,华中科技大学罗志强/张丽&宾夕法尼亚大学蒋圆闻使用一种可注射的生物粘附水凝胶生物电子学构建了一个用于细小周围神经的强大神经界面。通过在网络形成过程中引入多功能分子调节剂,我们通过微调反应动力学和导电网络内的多尺度相互作用,优化了水凝胶的可注射性和导电性。同时,在不损害其可注射性的情况下,实现了水凝胶的机械和电气稳定性。最小的组织损伤以及注射式神经界面的低且稳定的阻抗,使得在雄性大鼠模型中进行慢性迷走神经调节以治疗心肌梗死成为可能。我们这种高稳定性、可注射、导电的水凝胶生物电子学,易于针对具有挑战性的解剖位置,为未来的精准生物电子医学铺平了道路。该研究以题为“A Foundation Model Identifies Broad-Spectrum Antimicrobial Peptides against Drug-Resistant Bacterial Infection”的论文发表在《Nature Communications》上。

图1展示了一种新型的注射式、具有生物粘附性的水凝胶生物电子学材料,该材料通过引入单宁酸(TA)作为分子调节剂,优化了点击化学反应动力学和导电网络内的多尺度相互作用,从而实现了对细小周围神经的强大神经界面构建。这种水凝胶不仅具有优良的注射性和导电性,还展现了出色的机械稳定性和抗膨胀性能,能够与神经组织形成稳定的粘附,为长期、有效的神经调节提供了可能。通过在大鼠模型中进行的实验验证,这种水凝胶能够用于慢性迷走神经刺激,以治疗心肌梗死,展示了其在生物电子医学领域的应用潜力。
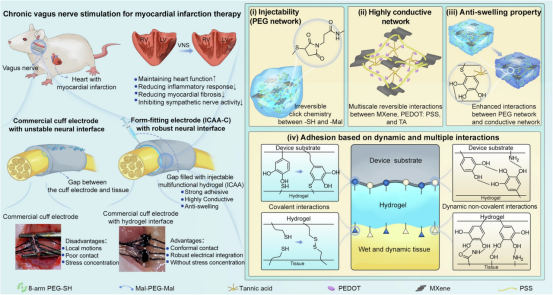
图1.通过ICAA水凝胶实现的贴合式袖套电极(ICAA-C)的示意图
【ICAA水凝胶的注射性、稳定性、机械和粘附性能】
图2详细展示了ICAA水凝胶的注射性、稳定性、机械性能和粘附特性。通过可控的点击化学反应和引入单宁酸(TA)作为分子调节剂,成功调控了水凝胶的凝胶化时间,确保了其良好的注射性。同时,水凝胶展现出了与软生物组织相匹配的机械模量和优异的抗膨胀性能,这有助于维持其长期的电气和机械稳定性。此外,水凝胶对神经组织和聚多巴胺(PDA)涂层基底的粘附强度和界面韧性均表现良好,证明了其在实际应用中与组织和设备基底形成稳定粘附的能力。
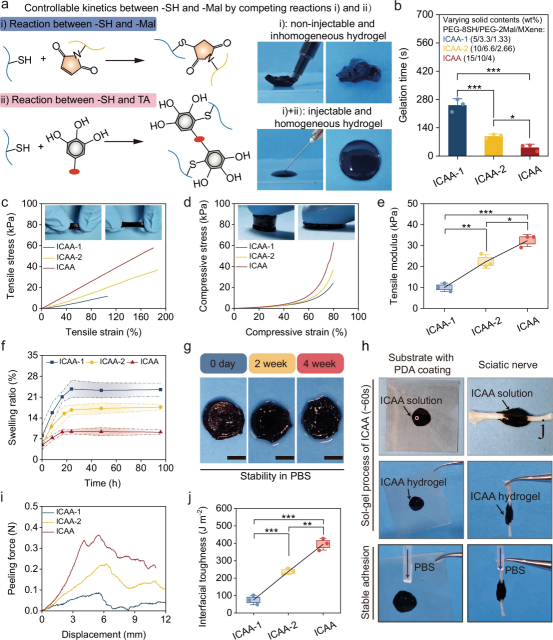
图2. ICAA水凝胶的注射性、稳定性、机械和粘附性能
【ICAA水凝胶的电气和电化学性能】
图3阐述了ICAA水凝胶的电气和电化学特性,揭示了通过精心设计的多尺度导电网络和分子调节剂TA的引入,水凝胶实现了优异的电导率和稳定的电化学性能。该水凝胶展示了低阻抗和高电荷注入能力,这在电刺激应用中是至关重要的。此外,其电导率在长时间浸泡于模拟体内环境的磷酸盐缓冲液中后仍能保持稳定,表明了卓越的长期电气稳定性。这些结果证实了ICAA水凝胶作为生物电子应用中神经界面材料的潜力,特别是在需要长期稳定性和高效电荷传输的慢性神经调控治疗中。
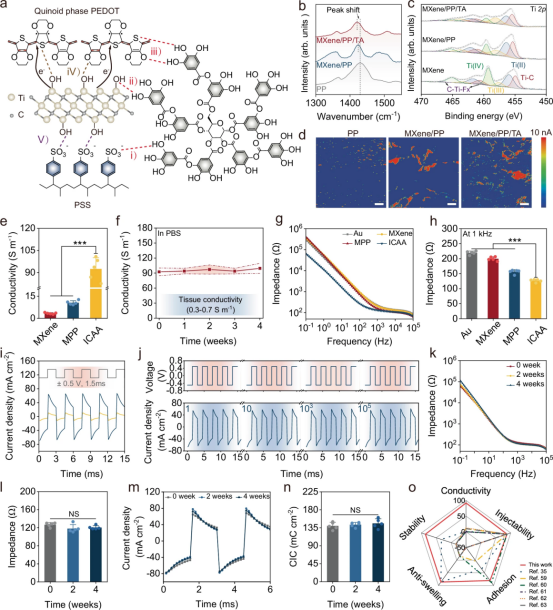
图3. ICAA水凝胶的电气和电化学性能
【通过ICAA-C构建的稳定神经界面】
图4展示了ICAA水凝胶构建的神经界面在体内环境中的稳定性和生物相容性。通过在雄性大鼠模型中进行的实验,研究者们观察到ICAA水凝胶与迷走神经的接触界面显示出了最小的组织损伤和炎症反应,与商用袖套电极相比,ICAA水凝胶电极在植入后4周的阻抗变化极小,表明了其长期稳定性。这些结果表明,ICAA水凝胶是一种有效的神经界面材料,能够在不引起显著组织反应的情况下,实现对神经的长期稳定调控,这对于慢性神经调控治疗具有重要意义。
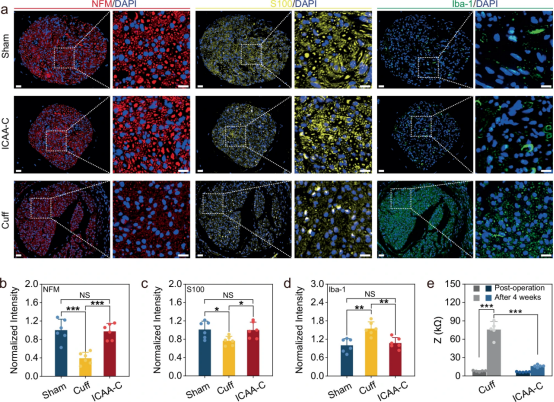
图4. 通过ICAA-C构建的稳定神经界面
【基于ICAA-C的慢性迷走神经刺激允许有效的心肌梗死治疗】
图5展示了ICAA-C神经界面在大鼠心肌梗死模型中进行慢性迷走神经刺激的治疗效果。通过对比ICAA-C组和心肌梗死(MI)组的心脏组织切片,发现ICAA-C组在心脏形态和功能上表现出显著的改善,包括减轻的左心室壁变薄、减少的心肌纤维损失和胶原纤维沉积,以及缩小的心肌梗死面积。此外,ICAA-C组的心脏功能参数(如射血分数EF和缩短分数FS)也有所提高,血清中的心脏损伤和心衰生物标志物水平也有所降低。这些结果表明,ICAA-C神经界面能够有效地促进心肌修复,抑制炎症反应和心脏重塑,从而为心肌梗死后的康复提供了一种有效的治疗策略。
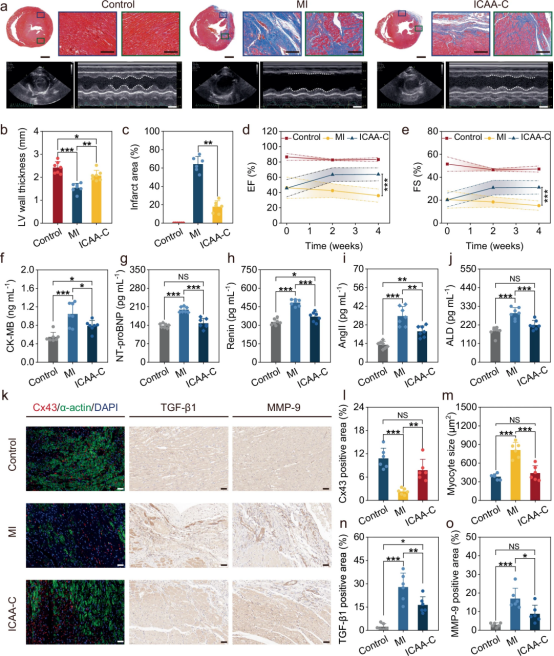
图5. 基于ICAA-C的慢性迷走神经刺激允许有效的心肌梗死治疗
【基于ICAA-C的迷走神经刺激调节炎症和心脏交感神经活动】
图6探讨了基于ICAA-C的迷走神经刺激对大鼠心肌梗死后炎症和心脏交感神经活动的调节作用。研究发现,与心肌梗死(MI)组相比,ICAA-C组大鼠血清中的炎症因子(如肿瘤坏死因子α和白细胞介素6)水平显著降低,表明刺激有助于减轻炎症症状。同时,ICAA-C组的交感神经活动标志物(如去甲肾上腺素和肾上腺素)水平下降,心脏组织中交感神经再生和活动的标志物(如生长相关蛋白43、神经丝200和酪氨酸羟化酶)的表达也减少,显示了迷走神经刺激对抑制心脏交感神经重构的潜在效果。这些结果表明,ICAA-C基的慢性迷走神经刺激不仅能够减轻心肌梗死后的炎症反应,还能有效调节心脏的交感神经活动,为心肌梗死后的心脏修复和功能恢复提供了新的治疗策略。
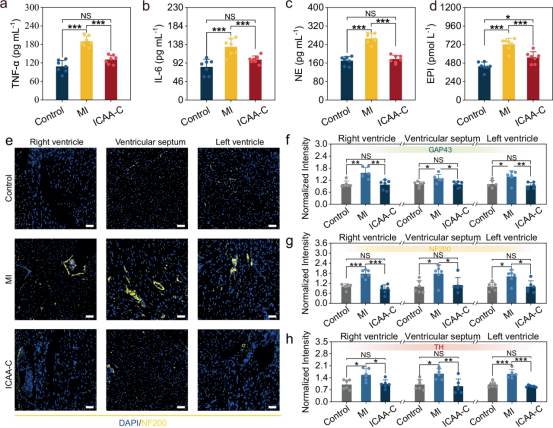
图6. 基于ICAA-C的迷走神经刺激调节炎症和心脏交感神经活动
【小结】
该研究开发了一种高稳定性、可注射的导电水凝胶生物电子学材料,通过在水凝胶网络形成过程中引入多功能分子调节剂,优化了其可注射性和导电性,同时保持了机械和电气稳定性,实现了对细小周围神经的长期稳定神经调节,为心肌梗死治疗提供了有效途径,并为未来精准生物电子医学的发展奠定了基础。
原文链接:
https://www.nature.com/articles/s41467-024-52418-y
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#心肌梗死# #慢性神经调控# #电疗药物# #水凝胶生物电子学#
12