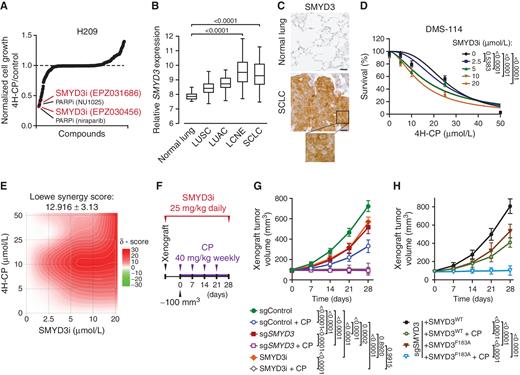
小细胞肺癌(SCLC)是一种侵袭性恶性肿瘤,是最致命的癌症之一。SCLC往往会较早且快速地转移,三分之二的病例在确诊时已经发生转移,并且化疗的效果差强人意。近来有研究发现不同SCLC分型间的治疗敏感性不同。但不同分型间是否存在可塑性、不同分型的转移和免疫抑制特征等问题目前尚不清楚。
2022年11月12日,第25届全国临床肿瘤学大会暨2022年CSCO学术年会特邀东部战区总医院宋勇教授就SCLC分子分型的相关研究进行分享。

在RNA水平上,可根据关键转录调节因子ASCL1,NeuroD1,POU2F3,YAP1的相对表达定义SCLC亚型。为更好地将上述分子分型应用于临床,目前通过免疫组化检测ASCL1,NeuroD1,POU2F3,YAP1蛋白表达定义亚型:SCLC-A,SCLC-N,SCLC-P,SCLC-Y。SCLC-A和SCLC-N为神经内分泌表型,伴有神经内分泌分化驱动基因INSM1及TTF-1等高表达;SCLC-P和SCLC-Y亚型为非神经内分泌表型,伴有上皮间质转化、NOTCH、HIPPO信号通路等激活。

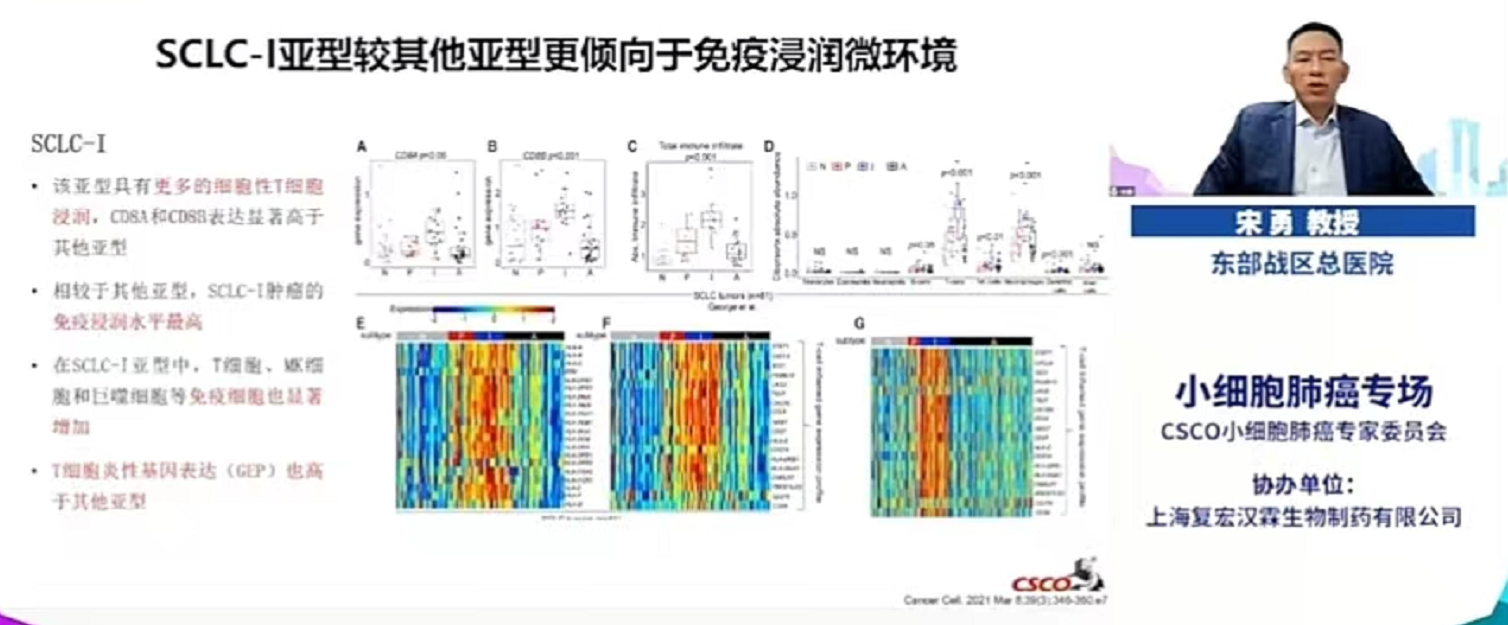
然而进一步研究发现,YAP1在SCLC-P中也会表达,因此YAP1作为SCLC亚型分类的标志物存在争议。近期,通过对81例SCLC患者的手术切除标本进行肿瘤基因表达数据分析与非负矩阵因式分解重新定义SCLC的分型,并在SCLC-A、SCLC-N、SCLC-P的基础上提出了高表达抗原提呈相关基因、T细胞炎性基因表达谱(gene expression profile,GEP)的亚型—SCLC-I。与SCLC-Y相比,SCLC-I更加准确地定义了潜在的免疫获益亚型的特征,为后期SCLC免疫获益患者的筛选提供了可能。
IMpower133试验是一项随机、双盲、国际多中心、1期(安全性)和3期(疗效)临床试验。入组标准主要为经组织学或细胞学证实的ES-SCLC,ECOG评分0-1分,且此前未接受过全身治疗的成人患者,允许纳入经过治疗的无症状脑转移患者。主要排除标准为合并自身免疫性疾病,或既往使用CD137激动剂、免疫检查点抑制剂的患者。入组后,患者按照1:1随机分配,接受4周期Atezolizumab+化疗或者安慰剂+化疗,诱导治疗结束后,继续接受Atezolizumab或安慰剂维持治疗,直至患者出现疾病进展。主要研究终点为OS和无进展生存期(PFS),次要研究终点包括客观缓解率(ORR)、缓解持续时间(DoR)和安全性。

研究结果显示,Atezolizumab+化疗组与安慰剂+化疗组的中位OS分别为12.3 vs 10.3个月(HR=0.70,95%CI:0.54-0.91,p=0.07),中位PFS分别为5.2 vs 4.3个月(HR=0.77,95%CI:0.62-0.96,p=0.02)。两组的12个月OS率分别为51.7% vs 38.2%。与安慰剂+化疗组相比,Atezolizumab+化疗组获得了更好的OS。
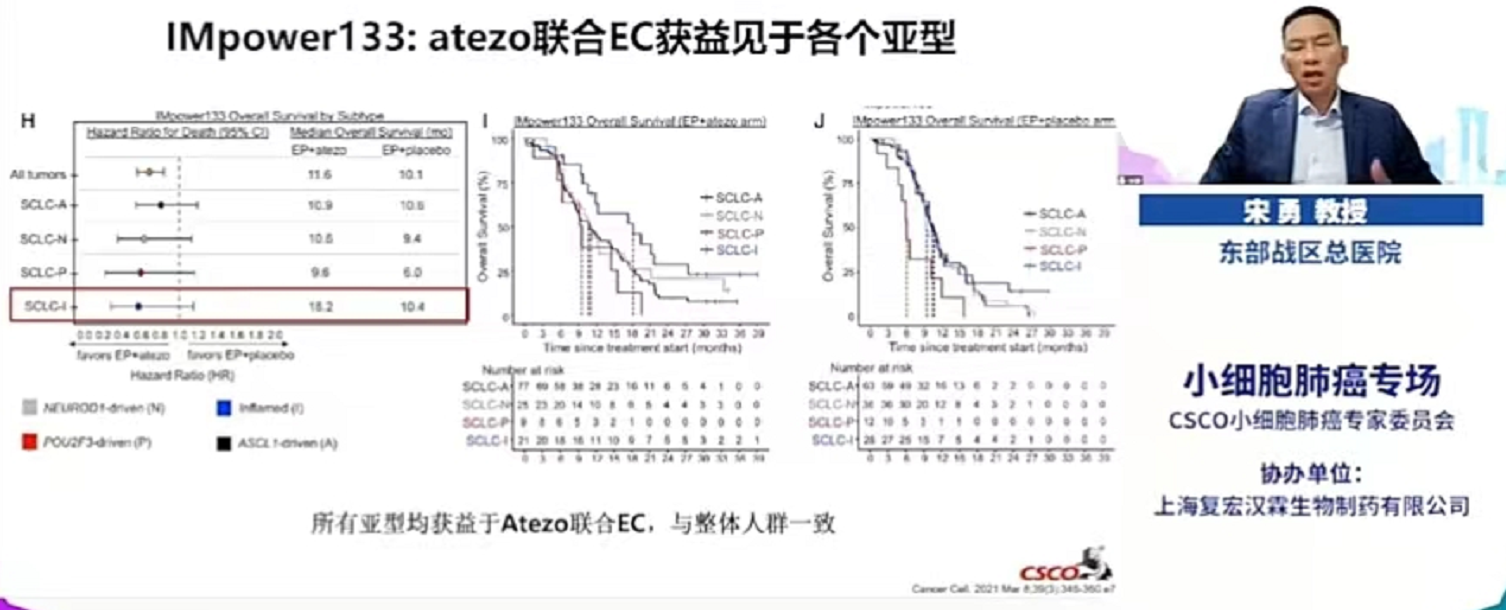
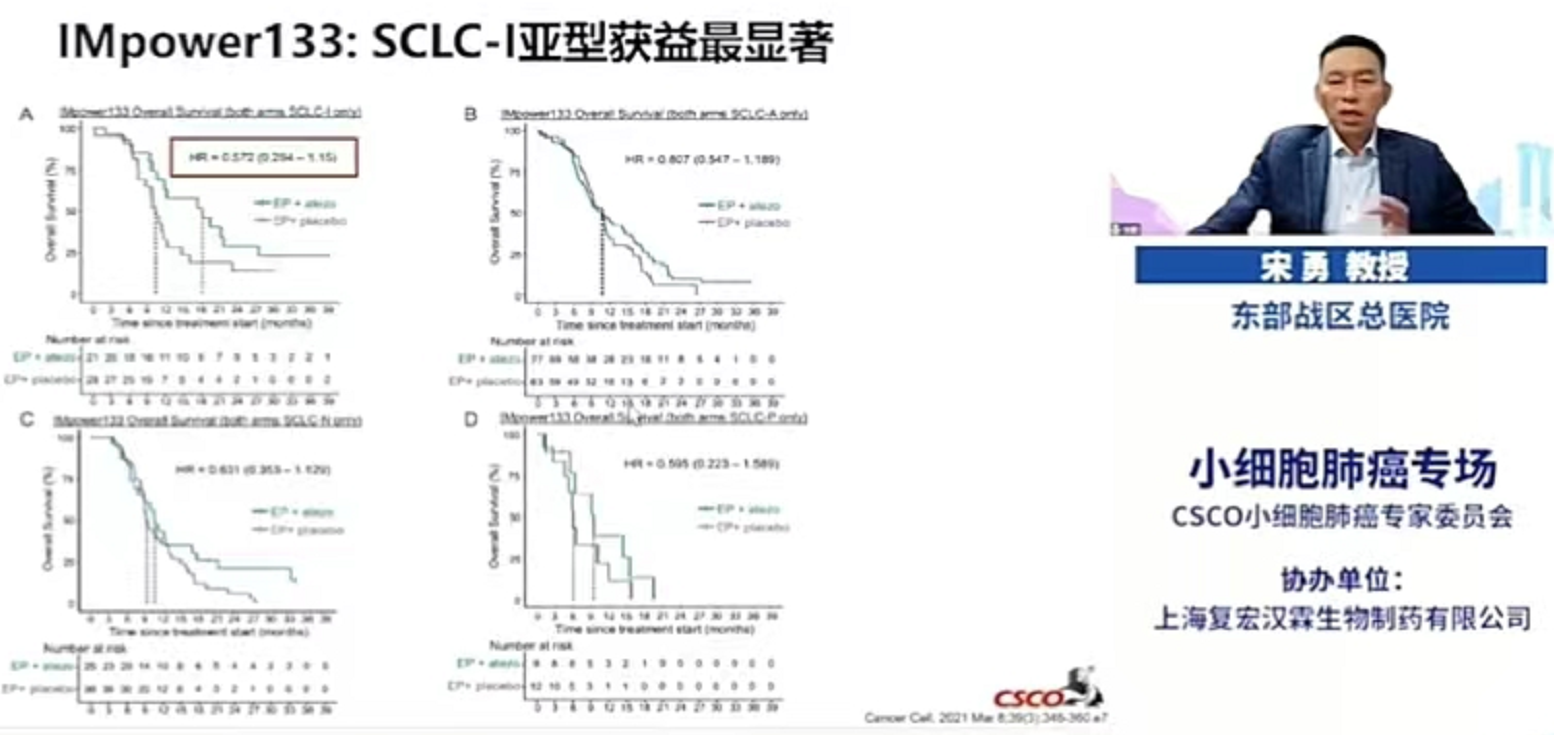
IMpower133临床试验的阳性结果是近20年来SCLC治疗方式的里程碑式突破。但与安慰剂组相比,接受Atezolizumab治疗的ES-SCLC患者中位OS仅提高2月。为了更好的解析可精准受益于免疫治疗的SCLC人群,MD Anderson肿瘤中心的Byers教授利用了Impower133临床试验患者的RNA-seq进行相关探索,发现SCLC-I亚型免疫浸润程度较高,富集杀伤性T细胞、NK细胞和巨噬细胞,同时高表达抗原提呈相关分子等。后续的预后分析结果提示,与安慰剂+化疗组人群相比,SCLC-I亚型人群可明显受益于Atezolizumab+化疗治疗,两组患者中位OS分别为18.2 vs 10.4个月。相比于整体人群2个月的中位OS改善,SCLC-I亚型获得了7.8个月的中位OS改善,SCLC-P亚型获得了3.6个月的中位OS改善,而SCLC-A,SCLC-N则无明显中位OS改善。
近年来生物信息学技术发展迅速,测序技术的普及和空间转录组学的发展使充分探索SCLC生物学特性成为可能。但受SCLC肿瘤异质性高、取材困难等制约,目前对于SCLC生物标志物的研究进展较为缓慢,一些在NSCLC中有效的标志物对于SCLC免疫疗效的预测效能未达到预期。研究者对于SCLC的进一步探索从未止步,更加全面地了解SCLC特性、准确地定义SCLC的亚型以挖掘真正有临床价值的疗效预测物将是未来SCLC领域发展的方向之一。
作者:梅斯医学
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言