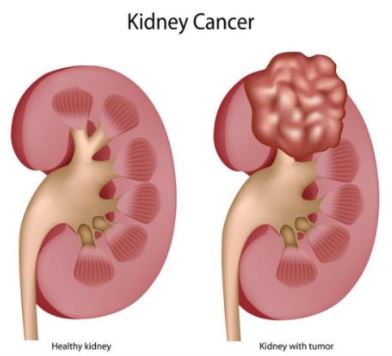
Eur Urol Focus:Nivolumab单药治疗晚期肾细胞癌的疗效如何?
2022-02-10 AlexYang MedSci原创
进行了NORA(NivOlumab in Renal cell cArcinoma)非干预性研究(NIS),旨在获取真实世界的数据以补充关键的CheckMate 025临床试验结果。
欧洲药品管理局在2016年批准了免疫检查点抑制剂(ICI)nivolumab作为第一个靶向PD-1的抗体,用于治疗既往治疗后的晚期肾细胞癌(aRCC)。该决定的得出基于了关键的3期CheckMate 025(CM025)随机临床试验(RCT)的结果。

近期,来自德国的研究人员在《Eur Urol Focus》上发表文章,他们进行了NORA(NivOlumab in Renal cell cArcinoma)非干预性研究(NIS),该研究旨在获取真实世界的数据以补充关键的CheckMate 025临床试验结果。

NORA是一项在德国进行的前瞻性、多中心的NIS。任何亚型的RCC患者在既往治疗后进行nivolumab治疗的均都符合纳入条件。研究的主要目标是估计总体人群和相关亚组的总生存期(OS)。次要目标包括无进展生存期(PFS)、客观反应率(ORR)、反应持续时间(DOR)、安全性和患者报告的结果(PROs)。研究人员使用了描述性统计对基线特征进行了总结。OS和PFS则通过Kaplan-Meier方法估计。
总共有228名aRCC患者符合条件。中位年龄为70岁,71%为男性,14%具有有利的风险,58%具有中等风险,15%具有较差的国际转移性RCC数据库联盟风险(12%信息缺失)。随访的中位数为37个月。在整体人群中,中位OS为24个月(95%置信区间[CI]19-28),中位PFS为5.3个月(95% CI 3.9-6.7)。ORR为20%,中位DOR为28个月(95%CI为16-无法估计)。没有出现新的安全事件(分别有46%和15%的患者出现所有等级和3-4级的治疗相关不良事件;有1例因肝衰竭而导致治疗相关的死亡)。在研究期间,PROs没有显示出损失。局限性包括缺乏中央病理审查,影像学评估和毒性评估没有标准化。

Nivolumab单药治疗的抗肿瘤活性情况
综上所述,该真实世界人群的有效性和安全性与关键性临床试验结果一致,并支持在广泛的aRCC人群中,可在既往的系统治疗后使用nivolumab治疗。
原始出处:
Marc-Oliver Grimm , Viktor Grünwald , Harald Müller-Huesmann et al. Real-World Data on the Use of Nivolumab Monotherapy in the Treatment of Advanced Renal Cell Carcinoma after Prior Therapy: Interim Results from the Noninterventional NORA Study. Eur Urol Focus. Dec 2021
作者:AlexYang
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#mAb#
77
#单药治疗#
76
#NIV#
78
#细胞癌#
58
#晚期肾细胞癌#
129