Nat Med:肿瘤免疫微环境在大B细胞淋巴瘤CAR T治疗中具有决定性作用
2022-09-07 聊聊血液 聊聊血液
目前而言,CAR T 细胞治疗在侵袭性 B 细胞非霍奇金淋巴瘤,患者中的获益最大,然而仍有约60%的 DLBCL 患者在CD19 CAR T 细胞治疗后会最终进展。
CAR T免疫微环境
目前而言,CAR T 细胞治疗在侵袭性 B 细胞非霍奇金淋巴瘤(称为弥漫性大 B 细胞淋巴瘤 (DLBCL))患者中的获益最大,然而仍有约60%的 DLBCL 患者在CD19 CAR T 细胞治疗后会最终进展。
CAR T的耐药机制已有很多研究,如肿瘤 CD19 缺失(称为‘抗原逃逸’),但治疗失败的原因常不明确,也没有足够的生物标志物来预测 CAR T 细胞治疗的结局。肿瘤微环境 (TME) 的免疫内容(immune content)可以预测细胞毒性和检查点抑制剂治疗实体瘤和血液恶性肿瘤的结局,但其在预测 CAR T 细胞应答中的作用方面一直缺乏证据。
在近日的《Nature Medicine》上,Scholler等在 ZUMA-1 II 期研究中评估了接受 CAR T (Axicabtagene ciloleucel,axi-cel) 治疗的 DLBCL 患者的TME,结果显示 TME 的免疫内容与临床缓解、生存期和毒性结局均相关。

在他们的研究中,Scholler等评估了51例患者的135份肿瘤活检样本,样本采集于 axicabtagene ciloleucel 治疗前后,然后使用数字化免疫组织化学平台(例如Immunoscore)和靶向转录组学(例如Immunosign21和 PanCancer 免疫分析平台)分析样本;并在3个独立 DLBCL 队列中验证了平台之间相关性的重现性,包括初治 LBCL 患者、入组正在进行的 Zuma-7 临床试验(二线治疗)的 LBCL 患者和在Moffit 癌症中心接受商业化 axi-cel 的 LBCL 患者。
本研究显示了TME和临床结局之间新颖且令人印象深刻的强大相关性。具体而言,治疗前肿瘤中高水平的细胞因子、趋化因子和某些活化标志物与高完全缓解率相关,而治疗后低 T 细胞耗竭与较高水平的循环 CAR T 细胞(与持久缓解相关)相关。最重要的是,治疗前肿瘤浸润性淋巴细胞 (tumor-infiltrating lymphocytes,TIL) 的高数量(Immunoscore) 和高细胞毒性特征 (Immunosign) 与总生存期改善相关。后者的意义深远:高 Immunosign 评分可预测约70%的患者超过2年的长期生存率,而低 Immunosign 评分患者仅有25%。
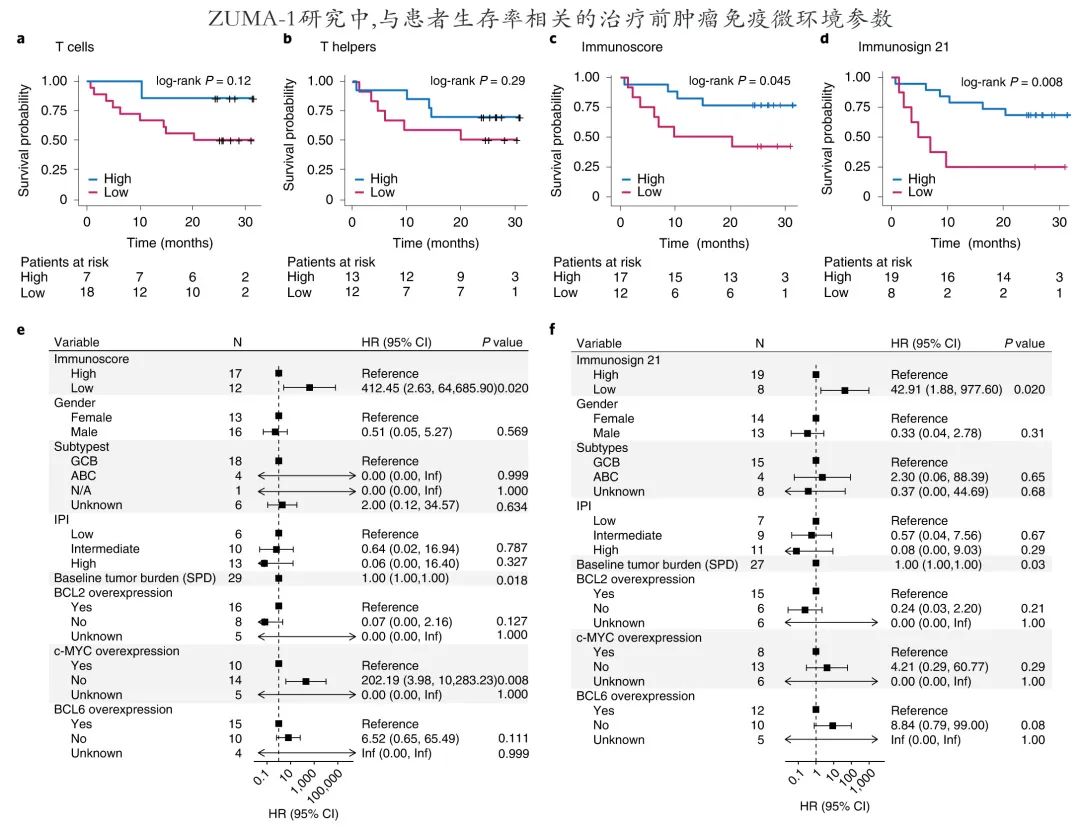
除了 CAR T 细胞疗效,治疗前 TME 也可预测 CAR T 细胞治疗的安全性:瘤内调节性 T 细胞与治疗后较低的严重神经毒性率相关,且不影响临床结局(影响临床结局的免疫微环境因素见下图)。并且至关重要的是,治疗后2周就可以观察到免疫微环境的变化,并据此区分应答者和非应答者。

对于CAR T,如果能设计治疗前或治疗后不久预测结局的生物标志物非常重要,因为它们可能为未来含CAR T联合方案治疗高危患者的试验提供重要信息。目前修改 TME 以增强肿瘤清除的策略包括重振功能失调的内源性 T 细胞的药物(如 PD-1 抑制剂)、表达免疫调节细胞因子的“装甲”CAR T细胞和产生抵抗免疫抑制的 CAR T 细胞(例如通过基因编辑或表达将抑制信号转化为刺激信号的“开关”受体)。使用预测性生物标志物(例如Immunosign 高/低)指导临床试验设计的可能优势在于,可个性化治疗和针对未满足需求最大的患者。
Scholler 等证明了, CAR T 治疗前细胞毒性 T 细胞上 PD-1 的表达与完全缓解率之间存在有利相关性。尽管 PD-1与 T 细胞耗竭有关,但它也在活化和效应 T 细胞上表达,可能是抗肿瘤 T 细胞功能更强的标志。化疗可能影响 T 细胞增殖、产生细胞因子和趋化因子的能力并使其变得具有细胞毒,表明将 CAR T 细胞纳入早期治疗策略可能有获益。因此基于随机 ZUMA-7 研究中CAR T 细胞治疗优于自体干细胞移植,美国FDA已批准 axi-cel 作为 DLBCL 患者的二线治疗;此外最近发表的 Zuma-12 II 期研究结果表明,axi-cel作为高危 DLBCL的一线治疗有效。除此之外,治疗前活化 T 细胞水平是否与依赖内源性 T 细胞的其他治疗(如双特异性抗体)后的临床结局相关?这个问题也非常有趣,而这些治疗在进行中的淋巴瘤和骨髓瘤研究中都极具前景。
根据本研究,DLBCL 的传统分子亚型与 CAR 后 T 结局之间缺乏相关性,这与关键 CAR T 临床研究结果一致,而探索最近定义的 DLBCL 分子亚型与 CAR T 结局之间的潜在关联也很有吸引力。
值得注意的是,一些与临床疗效相关的生物标志物也可能反过来是其疗效的根本原因,因此针对标志物也许可使疗效更佳。例如存在治疗前肿瘤浸润性淋巴细胞可能仅表明存在允许 CAR T 渗透的可穿透肿瘤(即相关,correlative),也可能表明肿瘤浸润性淋巴细胞可在 CAR T 浸润时“参与”肿瘤杀伤(即起因,causative);如果后者是真的,那么装甲 CAR T 细胞可使肿瘤浸润性淋巴细胞活化:例如活化诱导的 IL-2/IL-7/IL-12/IL-15 分泌性 CAR T 细胞可能会增强疗效。同样,CAR T细胞治疗后肿瘤中趋化因子 (CCL2/CCL5) 的快速增加可能仅仅与活化良好的治疗细胞的释放相关,或可能导致 CAR T 细胞募集持续波;在后一种情况下,趋化因子改造的 CAR T 细胞或肿瘤内注射趋化因子可能会增加 CAR T 细胞的疗效。而剖析原因与关联性可能需要一个转化,即从临床回溯到实验室,从而孤立各变量并证实其因果关系。
随着 CAR T 细胞疗法整合入 DLBCL 早期治疗、其在多发性骨髓瘤中的最新获批以及实体瘤和血液恶性肿瘤中新型 CAR T 细胞的研究,接受 CAR T 细胞治疗的患者数量将大幅增加。Scholler 等的研究结果为确定预测 CAR T 治疗后结局的生物标志物奠定了基础,具有潜在的改变临床实践的意义。
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#细胞淋巴瘤#
95
#Nat#
78
#B细胞#
144
#肿瘤免疫微环境#
113
#Med#
140