【衡道丨笔记】免疫新辅助时代对食管外科带来的新思考
2024-06-23 衡道病理 衡道病理
文章论述食管癌新辅助治疗现状及问题,如传统方法远处复发率高,探讨免疫治疗在食管癌中的作用、对手术方式影响及器官保留策略。
新辅助(放)化疗可为食管癌患者带来总生存时间(OS)获益
-
CROSS与NEOCRETEC5010研究均证实,新辅助放化疗+手术对比单纯手术,可改善患者OS获益;
-
JCOG9907与OEO2研究均证实:术前化疗可改善患者OS获益。
传统新辅助治疗方法的问题和困惑
-
虽然和单纯手术或术后辅助治疗比较,提高了5年生存率,但远处复发率仍然相对较高;
-
在可以完全切除的肿瘤中,术前放疗是否有必要?
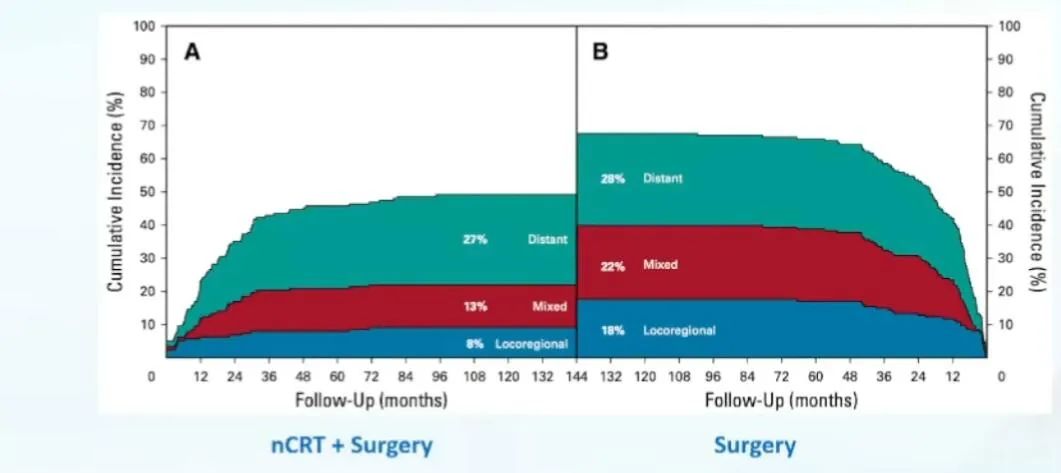
CROSS研究10年随访结果显示,与单纯手术治疗相比,手术联合新辅助放化疗在肿瘤远处转移方面并没有显著差异。
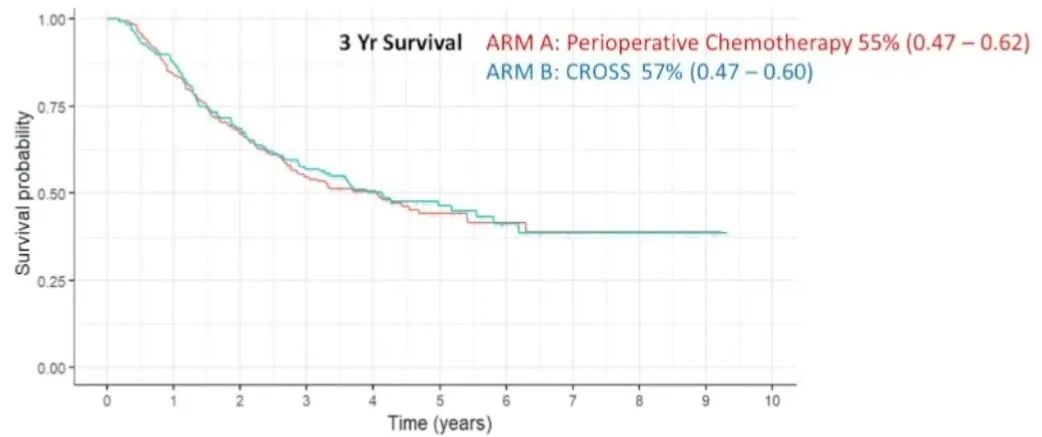
NEWAGES研究显示,A组(术前化疗)与B组(术前放化疗)在三年生存率方面没有显著差异。
日本一项针对鳞癌患者的研究表明,同步放化疗与两药化疗相比并没有显著优势。
国内纳入局部肿瘤患者为主的研究表明,相比化疗,同步放化疗并未显示出优势。
免疫治疗显著改善了食管癌患者的生存
在多变量COX分析中,与未接受免疫治疗的患者相比,接受免疫治疗者OS显著改善(HR 0.756;95%CI 0.713-0.801;P=0.001)。
免疫治疗时代食管外科的相关问题
可切除食管癌免疫介入的时机
新辅助免疫治疗,将肿瘤视为抗原库,通过发挥免疫系统的监视清除功能,增强系统抗肿瘤免疫,清除远端微小转移灶,达到治疗目的。
新辅助免疫治疗病理反应和影像学评估的不一致性
In MPRs(包括pCR),viable tumor可能被纤维化、浸润淋巴细胞、淋巴滤泡样三级淋巴结构所取代,而在影像学评估上仍呈现为measurable tumor。
新辅助治疗后病理反应深度与EFS/RFS(Event-free survival/Recurrence-free survival)相关
在TNBC和NSCLC两项成功的新辅助ICB联合化疗的注册试验中,均发现术后病理示pCR的患者,复发可能更小。提示术后病理示应答可能代表系统抗肿瘤免疫的成功诱导和微小转移灶的清除。
部分原发肺癌患者,病理示轻微应答,仍有较长的EFS。提示活化的抗肿瘤T细胞能更有效地清除微小转移灶。
从新辅助治疗后肿瘤样本(resected tumor,serum/plasma ctDNA,proteomic technologies)中获得的信息更好地指导个性化术后辅助治疗,以期改善患者预后。
免疫治疗是否能够影响食管外科手术方式
多项研究已证实肿瘤周围正常淋巴结内相关淋巴细胞在免疫治疗中的重要作用。今年发表的一项针对头颈部鳞癌(HNSCC)周边淋巴结的研究揭示了此类患者中存在的一个模型:即经过免疫检查点抑制剂治疗(ICB)后,Tpex细胞增殖活化,并向Tex-int分化,经外周血,运输至肿瘤组织,成为终末耗竭T细胞(Tex-term)——通常被认为有助于免疫细胞抗肿瘤反应。这类细胞在转移淋巴结中都被一致了,而在正常淋巴结中则为睡眠或“疲惫期”,可以被PD1、PDL1的抗体激活,是免疫治疗的主力军。如果前期手术或放疗范围太广,将这些正常的淋巴细胞切除或抑制了,则可能影响免疫治疗的效果。
因此,免疫时代对食管癌淋巴结清扫出现了新的挑战,问题包括日本提倡的“三野淋巴结清扫”是否过度?临床上是否具有“选择性淋巴结清扫”的可能性?以及除了肿瘤和淋巴结病理评估,ctDNA是否可以成为判断肿瘤治疗“彻底性”的指标。这些问题均有待在进一步的研究中得到探索。
免疫治疗为器官保留带来新曙光
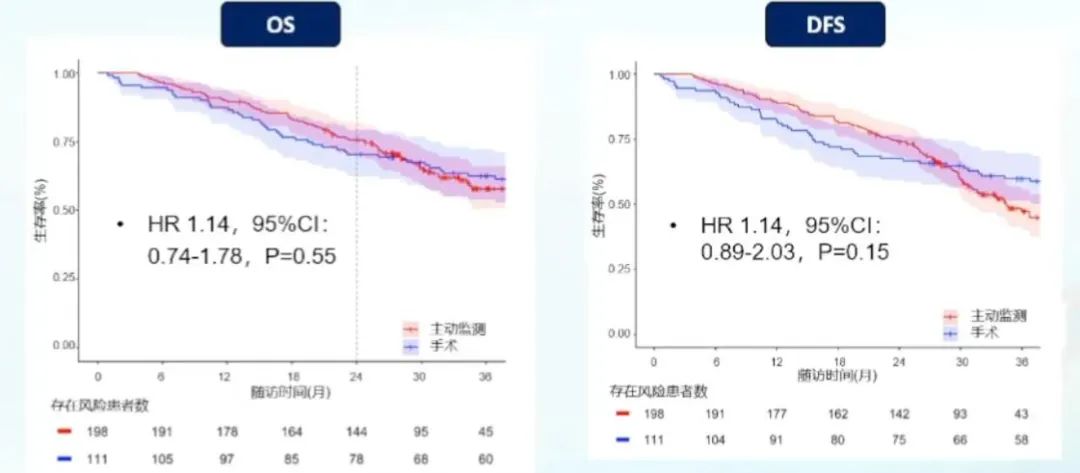
旨在比较新辅助放化疗后主动监测与标准手术治疗局部晚期食管癌疗效的SANO研究提示,接受主动监测的患者2年总生存率非劣于手术,而主动监测期间局部复发者可以安全手术;至少35%接受主动监测的患者免于无意的食管切除,进而改善了短期健康相关生活质量;此外,长期肿瘤学疗效需要持续随访。
PALACE-1研究表明,联合放化疗中加入免疫治疗,可进一步提升手术患者的pCR率(达到55.7%)。免疫联合新辅助放化疗有望实现食管癌治疗的器官保留策略 。
作者:衡道病理
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#食管癌# #新辅助治疗# #免疫治疗#
89