四川大学王娜《Small》:MOFs纳米酶水凝胶助力糖尿病感染伤口愈合
2024-09-13 BioMed科技 BioMed科技
糖尿病伤口炎症微环境复杂,四川大学团队构建 MOFs 纳米酶水凝胶,用于糖尿病伤口管理,加速伤口愈合。
糖尿病伤口的炎症微环境
随着人口老龄化的发展和超重人群比例的增多,糖尿病逐渐成为一种严重的公共卫生问题。糖尿病通常伴有多种并发症,如由糖尿病伤口或溃疡引起的糖尿病足,甚至可能导致患者截肢或死亡。与普通伤口相比,糖尿病伤口由于其复杂的炎症微环境(如细菌感染、ROS 过度积累和局部组织缺氧等),严重破坏了健康皮肤再生过程,且往往会发展成为慢性的不愈合伤口。反过来,糖尿病伤口部位的受损的血管又阻碍了正常的血液循环,导致氧气供给不足,又进一步恶化了伤口的炎症反应。因此,如何合理设计一种兼顾并同时解决糖尿病伤口的复杂炎症微环境,并加速其愈合过程的策略,是十分具有挑战性的。
抗氧化MOFs纳米酶
在糖尿病伤口的愈合过程中,活性氧(ROS)异常积累激活的氧化应激是导致剧烈炎症的主要因素。利用天然抗氧化酶,如超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GPx)和过氧化氢酶(CAT)等,是清除体内 ROS 的有效策略。然而,天然酶的脆弱性和高成本限制了其进一步的临床应用。因此,具有高稳定性、多孔性和可调性的金属有机框架(MOFs)可作为模拟类酶催化活性的纳米酶。通过活性金属位点与有机配体的配位作用(类似于天然酶中的活性中心结构),MOFs 可以模拟各种氧化还原酶的活性。然而,大多数已开发的MOFs 纳米酶的金属节点同时作为结构位点和活性中心,导致其配位结构网络不稳定,催化机制不明确等问题。
MOFs纳米酶水凝胶加速糖尿病伤口愈合
近期,四川大学王娜副教授等人报道了一种 MOFs 纳米酶水凝胶,并将其应用于糖尿病伤口管理。通过构建双金属 MOFs 纳米酶,明确区分和分离了 MOFs 配位网络中的结构位点和活性中心。受天然血红素的催化活性中心结构的启发,构建了基于卟啉的仿生 Mn-N4 活性位点,赋予其类 CAT 的催化活性。最后,将 MOFs 纳米酶与天然产物抗菌剂绿原酸(CGA)共同锚定于由京尼平(GP)交联的壳聚糖(CS)水凝胶中,该纳米酶水凝胶通过消除氧化应激、增加氧合作用以及逆转体内细菌感染,加速了 Ⅰ 型糖尿病小鼠的感染伤口愈合。这项工作成功开发了一种基于多功能水凝胶伤口敷料的有效策略,以“Kill Two Birds with One Stone: Dual-Metal MOF-Nanozyme-Decorated Hydrogels with ROS-Scavenging, Oxygen-Generating, and Antibacterial Abilities for Accelerating Infected Diabetic Wound Healing”为题发表于《Small》。四川大学化学学院王娜副教授和刘艳红实验师为该论文的共同通讯作者,四川大学化学学院博士研究生韦运洁为该论文的第一作者。本研究受到四川省科技厅科技计划项目等基金资助。
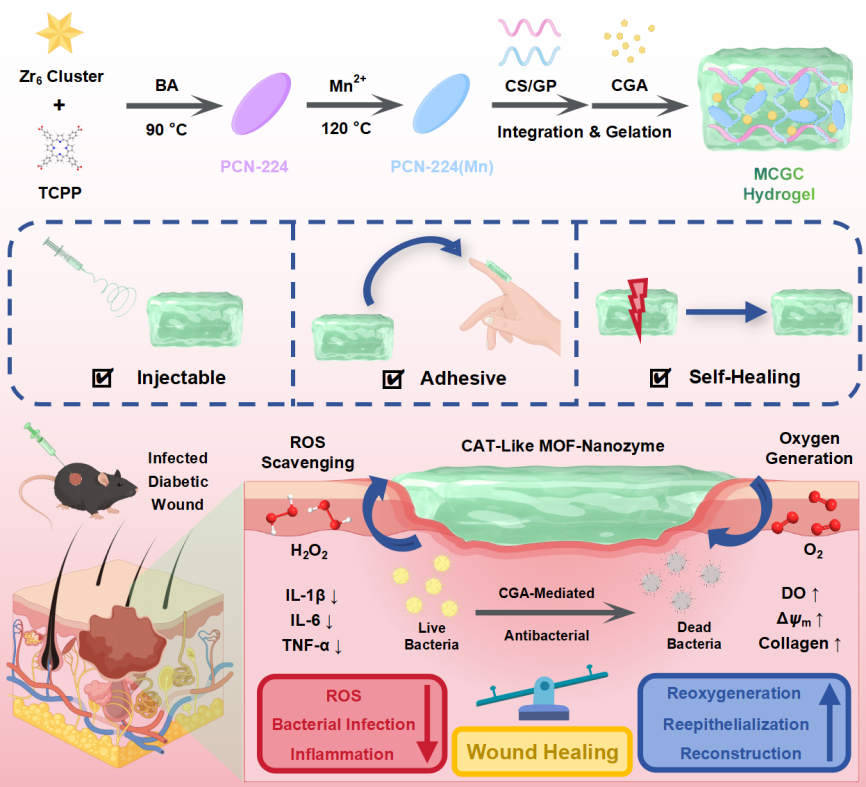
【文章要点】
首先,构建了基于 Mn-卟啉和 Zr6 团簇的双金属 MOF 纳米酶 PCN-224(Mn)。其中,作为结构金属结点,Zr6 团簇能够提供丰富的配位位点,供给有机配体以形成 MOF 配位网络。随后,引入了 Mn2+ 与卟啉环的中心吡咯氮原子配位。PCN-224(Mn) 纳米酶形成了血红素类的 Mn-N4 仿生结构,从而模拟了类 CAT 的催化活性。进一步,利用具有良好生物相容性和可生物降解性的 CS 和 GP 制备了水凝胶。同时,将该CS-GP水凝胶作为固定化平台,均匀负载了天然产物抗菌剂 CGA 和 MOFs 纳米酶,最终构建了具有可注射性、粘附性、自愈合性的多功能水凝胶 MCGC,并用于糖尿病感染伤口敷料。
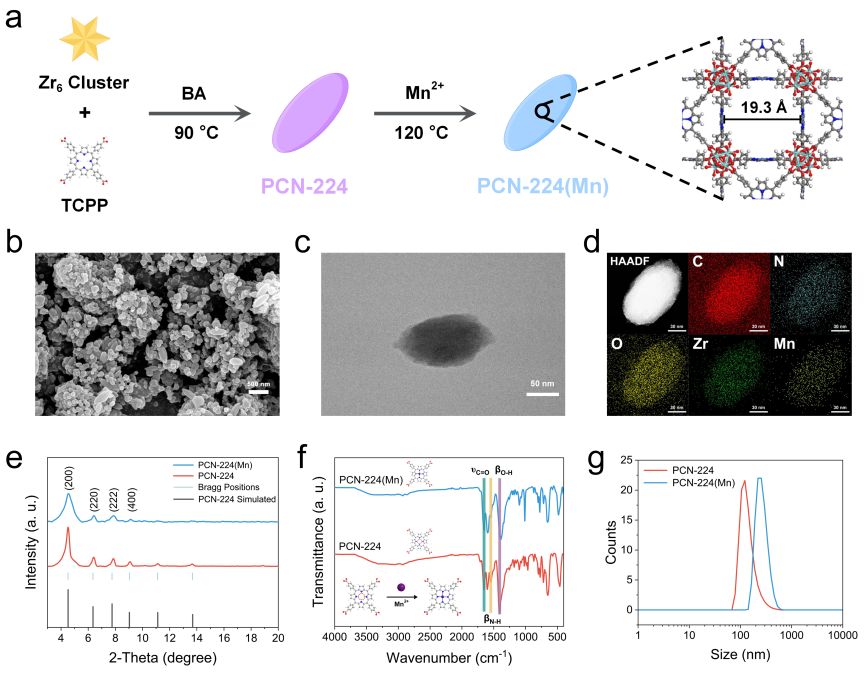
图1 MOFs纳米酶的表征
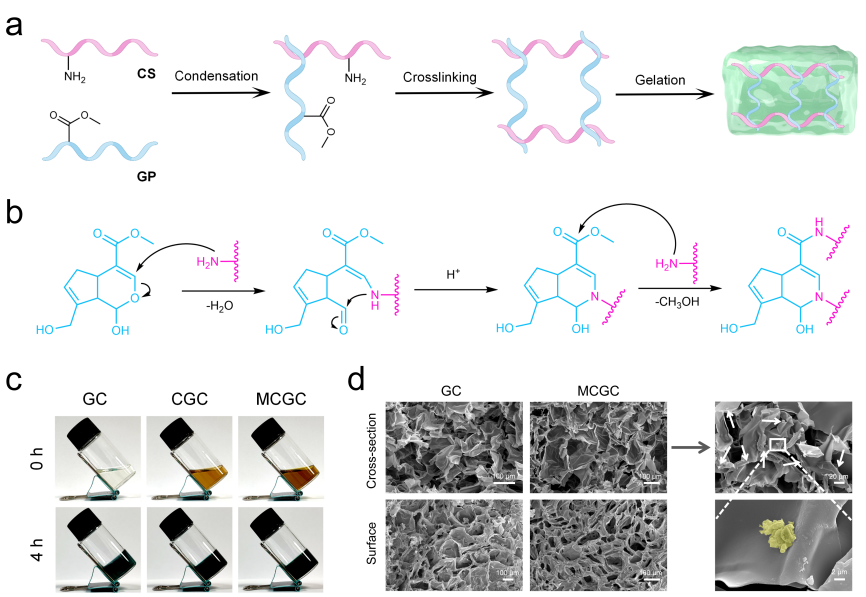
图2 MOFs纳米酶水凝胶的表征
CGA 主要存在于一种名为金银花(Lonicera japonica Thunb.)的传统中药中,是其具有抗菌、抗病毒活性的有效成分之一。作为一种天然多酚类化合物,CGA 可以有效抑制细菌生长,并可作为一种抗生素替代物,以避免产生潜在的抗生素耐药性。在成功负载 CGA 后,MCGC 水凝胶同时对革兰氏阴性菌和革兰氏阳性菌均有显著的抑制作用。MCGC 水凝胶对大肠杆菌(E. coli)的抑菌率高达99.91%,而对金黄色葡萄球菌(S. aureus)的抑菌率则高达99.97%。经探究其抑菌机理发现,MCGC 水凝胶主要通过改变细菌细胞膜的通透性,使细菌正常生理代谢紊乱并阻止其增殖。另外,MCGC 水凝胶还能有效清除由 E. coli 和 S. aureus 形成的成熟细菌生物膜,成功逆转糖尿病伤口细菌感染。
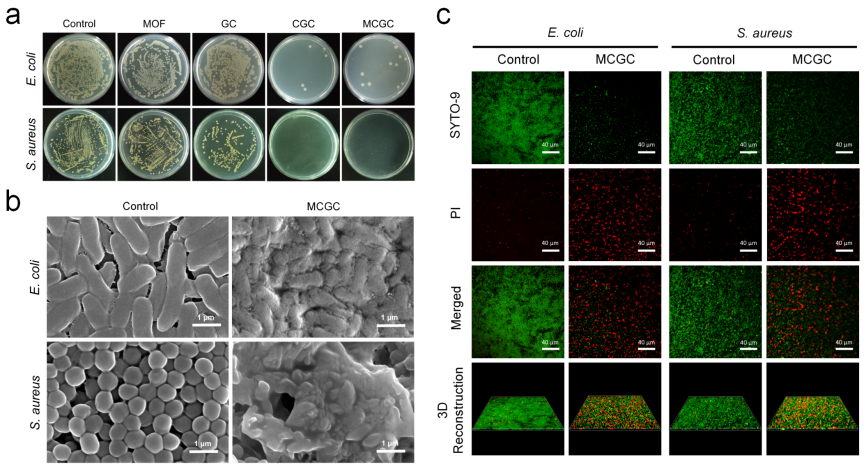
图3 MOFs纳米酶水凝胶的抗菌活性
ROS 积累和伤口局部缺氧会加剧炎症风暴和伤口肿胀,使得糖尿病伤口难以愈合。该PCN-224(Mn) MOF 纳米酶通过构建 Mn-N4 仿生化学结构,模拟了类 CAT 酶催化活性。类 CAT 纳米酶可将伤口部位累积的 H2O2 转化为 H2O 和 O2,在缓解氧化应激的同时,还能供给溶解氧以促进伤口愈合。在成功负载 MOF 纳米酶后,MCGC 水凝胶可有效降解 H2O2,并产生大量溶解氧。在 12 h 内,MCGC 水凝胶对 H2O2 的清除率高达 87.9%,并在 24 h 内达到 97.7%。这种ROS清除活性,使得 MCGC 水凝胶能够成功缓解由 H2O2 介导的细胞内严重氧化应激,逆转细胞内线粒体膜电位,并恢复小鼠成纤维细胞的正常生理代谢。
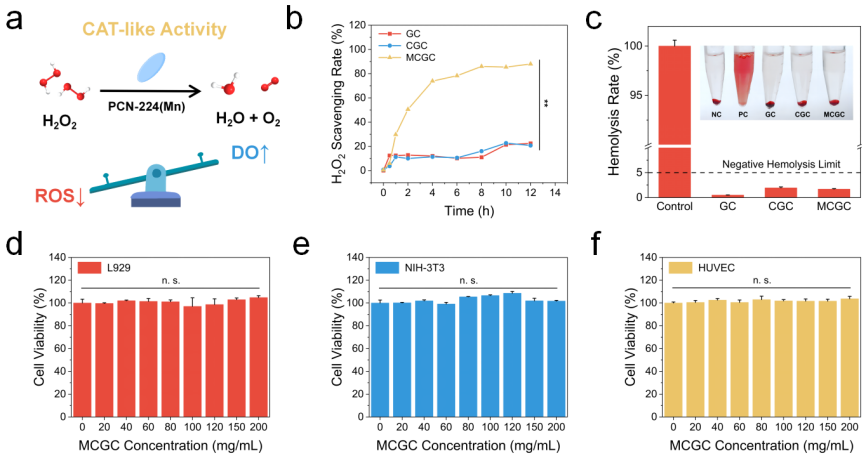
图4 MOFs纳米酶水凝胶的ROS清除活性
在 Ⅰ 型糖尿病小鼠的伤口愈合过程中,MCGC 水凝胶处理组的小鼠伤口愈合速率显著高于对照组,且在治疗终点(第 8 天)的伤口愈合率达 ~95%。在组织病理分析中,HE 染色显示 MCGC 水凝胶有效缓解了伤口部位的炎症响应,并促进了新生毛囊、皮脂腺和其他皮肤附属器的再生;而 Masson 染色则展示了 MCGC 水凝胶有效促进了与伤口愈合相关的胶原纤维在伤口部位的再生与沉积。进一步通过免疫组织化学分析,MCGC 水凝胶显著下调了伤口部位的IL-1β、IL-6 以及 TNF-α 等炎症因子的表达。在该Ⅰ型糖尿病小鼠的感染伤口模型中,MCGC 水凝胶作为多功能伤口敷料,成功加速了糖尿病感染伤口愈合。
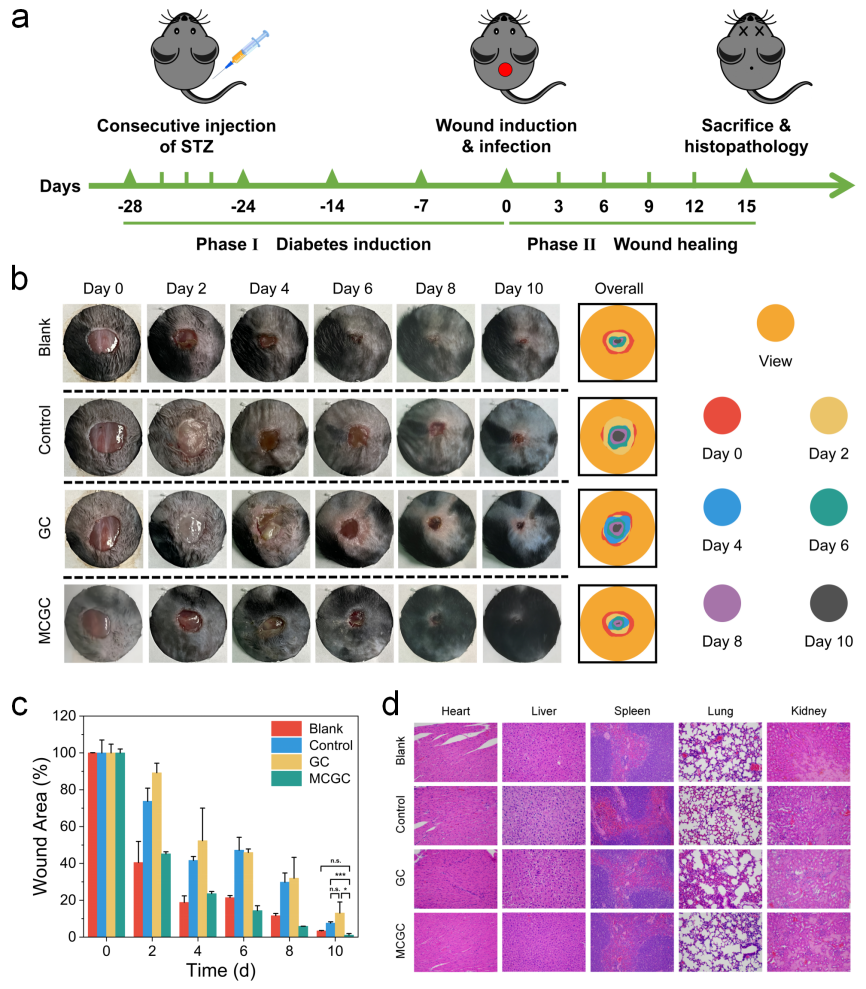
图5 MOFs纳米酶水凝胶加速糖尿病伤口愈合
【总结与展望】
综上所述,该研究成功构建了可注射、自粘附和自愈合的 MCGC 水凝胶,并作为可定制的个性化伤口敷料。MCGC 水凝胶为天然抗菌剂 CGA 和 MOF 纳米酶提供了负载平台,使其同时具有促进 ROS 清除、溶解氧生成和优异抗菌性能的多功能自适应活性。在 Ⅰ 型糖尿病小鼠感染伤口模型中,MCGC 水凝胶通过显著加速伤口闭合、诱导胶原沉积、缓解炎症响应,实现了促进糖尿病感染伤口愈合。最后,MCGC 水凝胶作为一种具有良好生物相容性的伤口敷料,为临床糖尿病伤口治疗提供了一种有效的潜在策略。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/smll.202403679
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#糖尿病# #MOFs纳米酶水凝胶#
65