Nat Commun:NOD2的缺乏促进克罗恩病分泌型IgA复合物的逆向转运
2021-01-20 xiaozeng MedSci原创
宿主免疫系统区分病原体和共生体的能力对于粘膜稳态的维持是必不可少的。
宿主免疫系统区分病原体和共生体的能力对于粘膜稳态的维持是必不可少的。当存在功能或遗传缺陷时,维持肠道粘膜稳态的相关机制尤为重要。而慢性肠道炎症如克罗恩氏病(CD)的发生发展也与免疫反应精细平衡的紊乱相关。
CD是一种特发性的慢性区域性肠炎,通常会影响回肠末端,但也可能影响从口腔到肛门的胃肠道中的任何部分。CD一般被认为是由具有特定遗传背景的个体中共生细菌的自我识别能力下降和粘膜屏障功能障碍所引起的。
在CD患者中NOD2突变会增加SIgA的反向胞吞作用
分泌型IgA(SIgA)是人类和许多其他哺乳动物粘膜表面上最丰富的免疫球蛋白。SIgA可以通过区分肠道病原体和肠道共生细菌来保护肠道上皮。肠道免疫系统对肠道病原体的识别会诱导高亲和力、T细胞依赖性的病原体特异性IgA的产生。
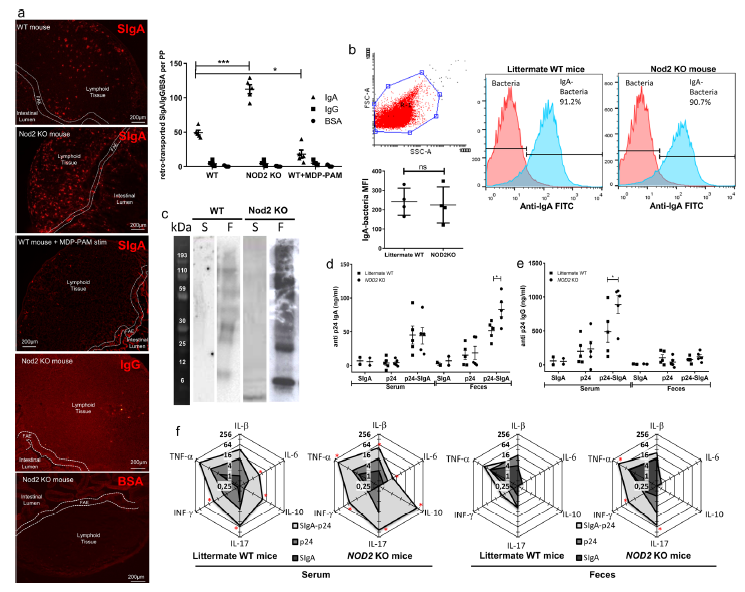
NOD2缺乏增加了体内IgA的逆向转运
肠道微皱折细胞(M细胞)主要负责将SIgA-病原体复合物转运到肠道相关淋巴组织中。SIgA/共生复合物的摄取对于启动粘膜的适应性免疫至关重要。
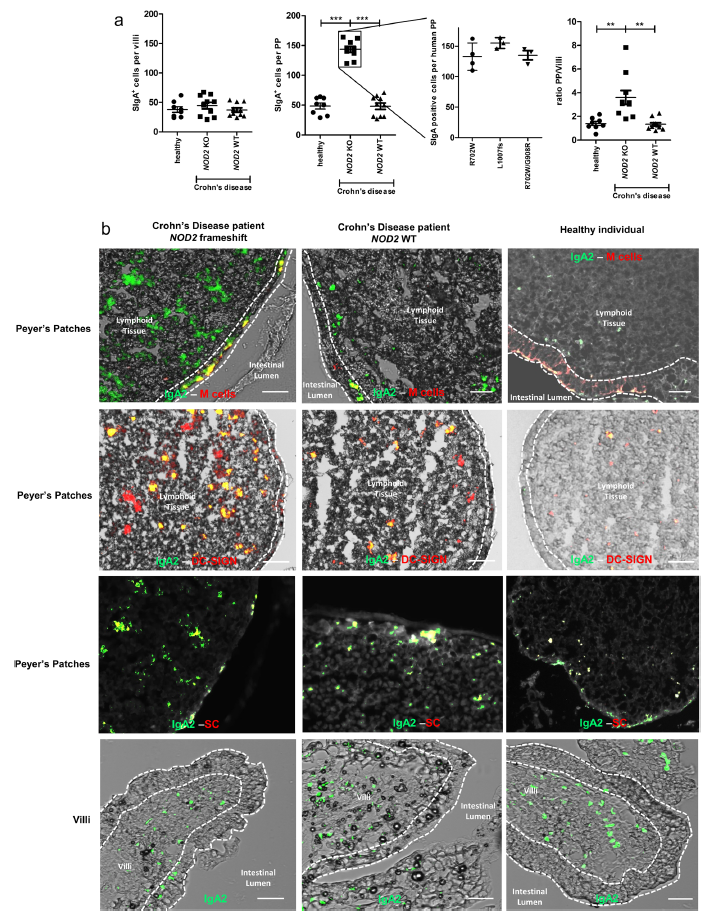
CD患者的SIgA-病原体复合物在M细胞中的逆向运输增加
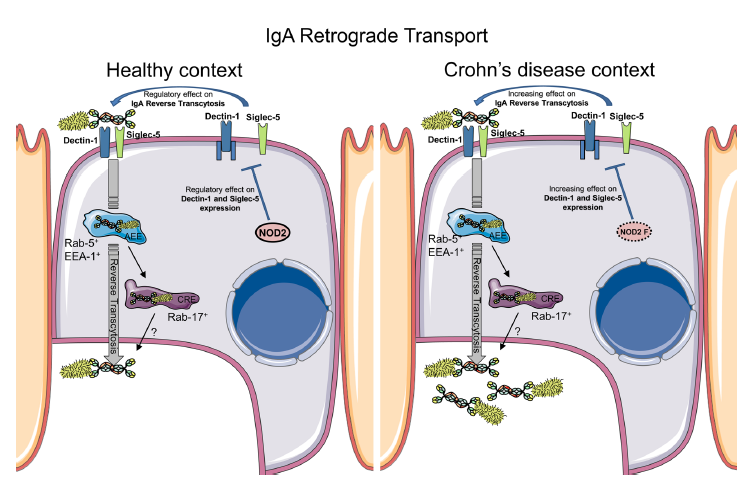
该研究旨在探究在克罗恩病(CD)中SIgA逆向转运免疫复合物的作用。研究人员发现,与无NOD2突变的CD患者以及健康个体相比,携带NOD2突变的CD患者的SIgA转运显著增加。NOD2通过下调参与逆行运输的两个受体Dectin-1和Siglec-5的表达水平,以影响M细胞的IgA运输。
总而言之,以上的研究结果揭示了NOD2介导的对肠道菌群的粘膜反应的调节机制,该机制引起了克罗恩病患者的肠道炎症和营养不良。
原始出处:
Rochereau, N., Roblin, X., Michaud, E. et al. NOD2 deficiency increases retrograde transport of secretory IgA complexes in Crohn’s disease. Nat Commun 12, 261 (11 January 2021).
作者:xiaozeng
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#COMMUN#
70
#转运#
88
#Nat#
87
#分泌#
0
#复合物#
73