Nature子刊综述:热免疫纳米医学在癌症中应用
2023-01-31 周 “ iNature”公众号
目前存在的各种挑战损害了更有效TINs的开发及其临床转化,但可以预测的是,结合热疗和免疫疗法的纳米药物最终将提供安全有效的癌症治疗。
免疫疗法使癌症患者的治疗发生了革命性的变化。然而,促进对这些疗法有抗性的肿瘤患者的抗肿瘤免疫仍然是一个挑战。热疗法为免疫治疗提供了一种有前途的免疫辅助策略,因此,各种癌症的热免疫治疗策略是一个相当有研究前景的领域。
2023年1月5日,西安交通大学田中民、杨哲、周口师范学院靳林、哈佛大学张兴才共同通讯在Nature Reviews Clinical Oncology(IF=65)在线发表题为“Thermal immuno-nanomedicine in cancer”的综述论文,该文总结了近年来热免疫纳米医学在癌症中的应用。
该综述描述了各种热疗法的作用,并提供了在临床试验中尝试将它们与免疫疗法结合的最新情况。该综述还概述了各种热免疫纳米药物的临床前开发,这些药物能够将热疗法与各种免疫治疗策略结合在一个单一的治疗平台上。最后,该综述讨论了与热免疫纳米药物临床转化相关的挑战,并强调了多学科和跨专业合作的重要性,以促进该技术从实验室到床边的最佳转化。

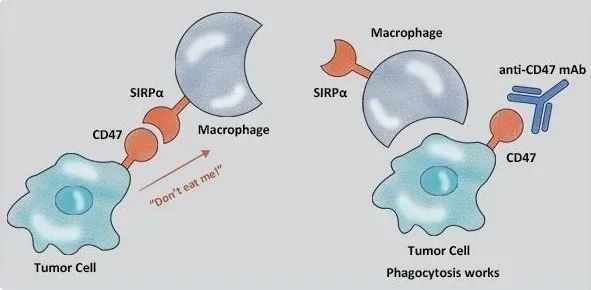
免疫疗法已经彻底改变了癌症治疗。然而,癌症有一种臭名昭着的逃避免疫系统的能力,而没有发炎和/或不引起免疫反应的肿瘤,即所谓的“冷”肿瘤,通常对免疫治疗没有反应。此外,免疫抑制肿瘤微环境(TME)通常作为免疫细胞浸润的屏障,使肿瘤能够逃避免疫监测,导致肿瘤进展。因此,重新编程TME以将冷肿瘤转化为热肿瘤,从而提高免疫治疗疗效的方法是研究的焦点。
为了应对这些挑战,已经在临床前模型和临床试验中开发和测试了免疫治疗与其他治疗方式相结合的策略。例如,FDA已经批准了8种以上的免疫检查点抑制剂(ICIs)联合化疗方案用于转移性非小细胞肺癌(NSCLC)患者,并且在几项试验中正在探索针对相同适应症的ICIs联合放疗。
热疗法已被证明可诱导癌细胞的免疫原性细胞死亡(ICD),从而在临床前模型中促进先天免疫和适应性免疫。此外,热疗法可改善灌注并降低瘤内间质压,这很可能是由于血管通透性的短暂增加。促进治疗共刺激分子和/或免疫细胞的积累,促进促炎细胞因子和趋化因子的释放,从而克服免疫抑制TME。各种结合热疗法和免疫疗法的临床试验已经进行,并可能导致癌症治疗的进步。

多学科团队推动的热免疫纳米药物的未来发展(图源自Nature Reviews Clinical Oncology )
尽管热免疫疗法在临床前模型中的表现令人鼓舞,但存在一些局限性,可能会损害这种方法在癌症患者中的治疗效果。首先,免疫治疗和/或热治疗药物通常是全身给药和非特异性累积,不仅影响其抗肿瘤活性,还可能导致不良事件;其次,在未来,基因编辑技术越来越有可能被用于修饰肿瘤细胞和/或其微环境,包括调节免疫检查点的表达,以及潜在的其他感兴趣的靶标,这将需要安全有效的转染系统。
越来越多的研究数据表明,纳米药物具有克服这些挑战的巨大潜力,因为与传统药物配方相比,纳米药物具有一些独特的优势,例如增强的靶向能力、细胞内给药、治疗药物的可控释放、生物利用度和多功能。因此,热免疫纳米药物(TINs)是一个快速发展的研究领域,它涉及纳米颗粒介导的热疗法和免疫治疗剂的传递,能够与热疗法同时协同作用。
作者在这篇综述中指出,开发更有效的TINs需要多学科专家团队的合作,以充分了解热疗协同免疫疗法的作用机制,开发更有效的组合平台,并制造更有效的加热和温度监测设备。解决这些问题可以进一步提高纳米药物的性能。目前存在的各种挑战损害了更有效TINs的开发及其临床转化,但可以预测的是,结合热疗和免疫疗法的纳米药物最终将提供安全有效的癌症治疗。
原始出处:
Yang, Z., Gao, D., Zhao, J. et al. Thermal immuno-nanomedicine in cancer. Nat Rev Clin Oncol 20, 116–134 (2023). https://doi.org/10.1038/s41571-022-00717-y.
作者:周
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言