【TCT】B-ALL CAR-T治疗缓解后异基因移植巩固的结局较佳
2024-07-14 聊聊血液 聊聊血液
希望之城国家医疗中心开展一项回顾性研究,评估了接受CAR-T治疗后在CR期接受第一次或第二次alloHCT巩固治疗的成人R/R B-ALL患者的结局。
B-ALL CAR-T后移植
CD19 CAR-T治疗复发/难治性(R/R)B细胞急性淋巴细胞白血病(B-ALL)儿童和成人患者的完全缓解(CR)率非常高,但大多数成人会在初始缓解后复发。延长CAR-T治疗后缓解持续时间的方法之一就是异体造血细胞移植(alloHCT)。但总的来说,CAR-T治疗后alloHCT在R/R B-ALL中的数据有限,特别是在CAR-T缓解后接受第二次alloHCT,此外CAR-T可能对后续移植造成负面影响,也存在一定局限性。
希望之城国家医疗中心(City of Hope)开展一项回顾性研究,评估了接受CAR-T治疗后在CR期接受第一次或第二次alloHCT巩固治疗的成人R/R B-ALL患者的结局。近日发表于《Transplantation and Cellular Therapy》。

本文要点
CAR-T缓解后AlloHCT是可行的,且与较低早期NRM相关。
在高危R/R B-ALL中,CAR-T应答者的异基因HCT结局令人鼓舞。
令人鼓舞的结果可扩展到CAR-T应答者的二次移植。
研究结果
患者特征
研究共纳入CAR-T缓解后接受alloHCT的45例成人R/RB-ALL患者,其中分别有26例(58%)和19例(42%)在CAR-T治疗后接受第一次和第二次alloHCT作为巩固治疗。中位年龄为31岁。Ph样是最常见的遗传亚型,占半数以上(53%;n=24);其中CRLF2重排患者17例,ABL融合患者5例,JAK2融合患者2例;正常核型8例,复杂核型5例。19例第二次alloHCT患者中,分别有5例和15例接受与第一次alloHCT相同供者和不同供者的干细胞;第一次alloHCT到首次复发的中位时间为15个月,第一次alloHCT到第二次alloHCT的中位时间为25个月。
在CAR-T治疗之前(清淋化疗前),24例(53%)患者仅在骨髓(BM)中患有R/R疾病(原始细胞≥5%),13例(29%)患者患有髓外病变伴或不伴BM受累,8例(18%)患者仅为MRD+。移植前既往中位治疗5线,分别有67%和22%的患者CAR-T前接受过贝林妥欧单抗和奥加伊妥珠单抗治疗。alloHCT时疾病状态为CR1、CR2或≥CR3的患者分别有7例(16%)、22例(49%)和16例(35%)。多数患者在移植均为MRD-状态,只有2例患者在移植前立即转化为MRD+(1例CD19阳性疾病和1例CD19阴性疾病)、1例患者移植前MRD状态未知。从CAR-T治疗到alloHCT的中位时间为93天。222例(49%)患者的预处理方案为基于放疗的清髓性预处理方案(MAC)。10例(22%)患者接受相合同胞供者移植,24例(53%)患者为非亲缘相合或不全相合供者移植,10例(22%)患者为单倍型供者移植。在3例Ph+ ALL患者中,只有1例移植后接受了ponatinib维持治疗。患者、疾病和移植的全部特征见表1。
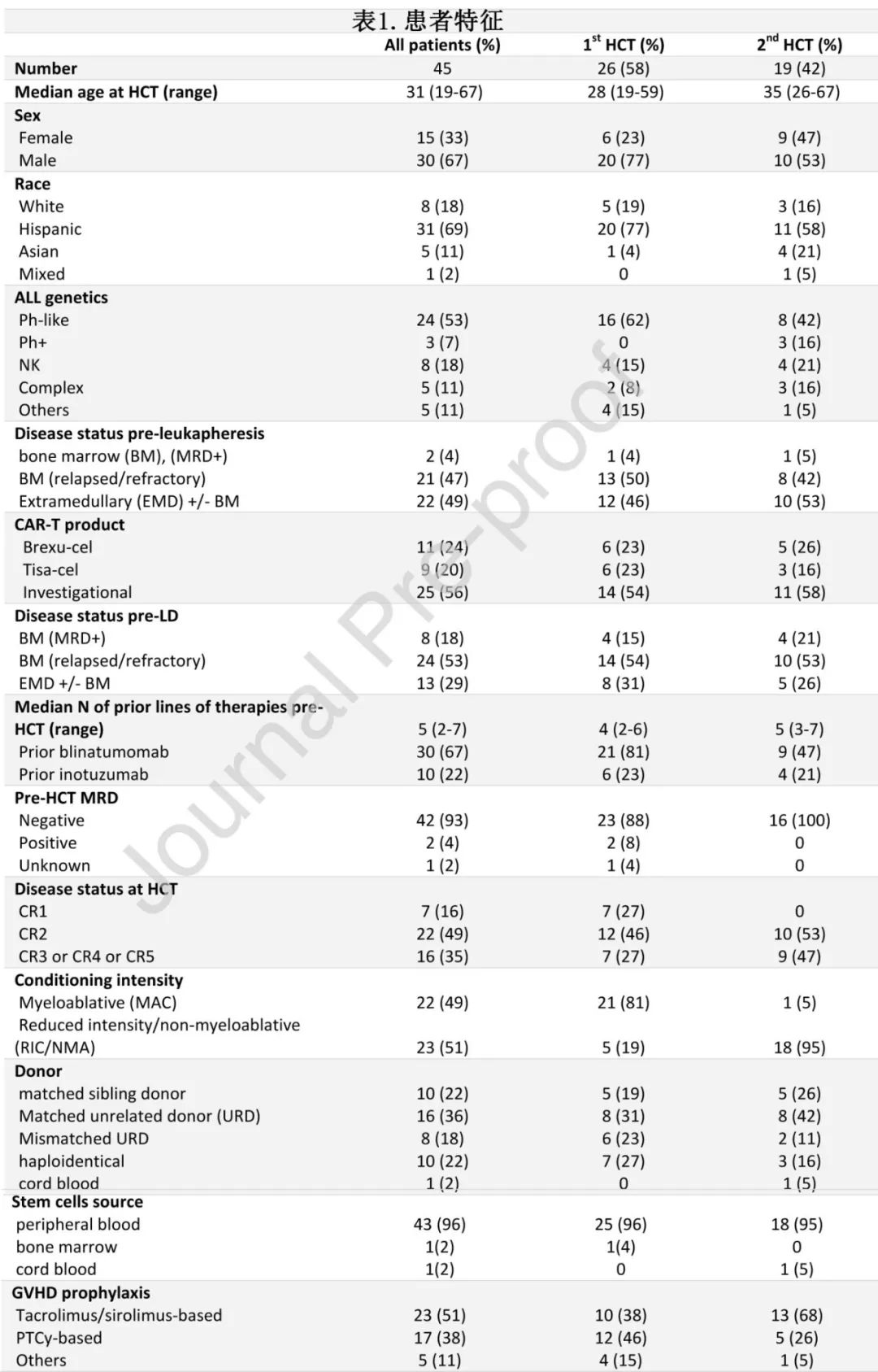
与CAR-T治疗后接受第一次移植的患者相比,接受第二次移植的患者年龄更大(35岁vs 28岁)、既往治疗线更多(5线vs. 4线)、CR3期或之后更多(47% vs. 27%)、更多接受基于RIC或NRM的治疗(95% vs. 19%)和基于他克莫司/西罗莫司的GVHD预防(68% vs. 38%),但具有ph样基因型的B-ALL(42% vs. 62%)的比例较小。
生存结局、复发率和非复发死亡率
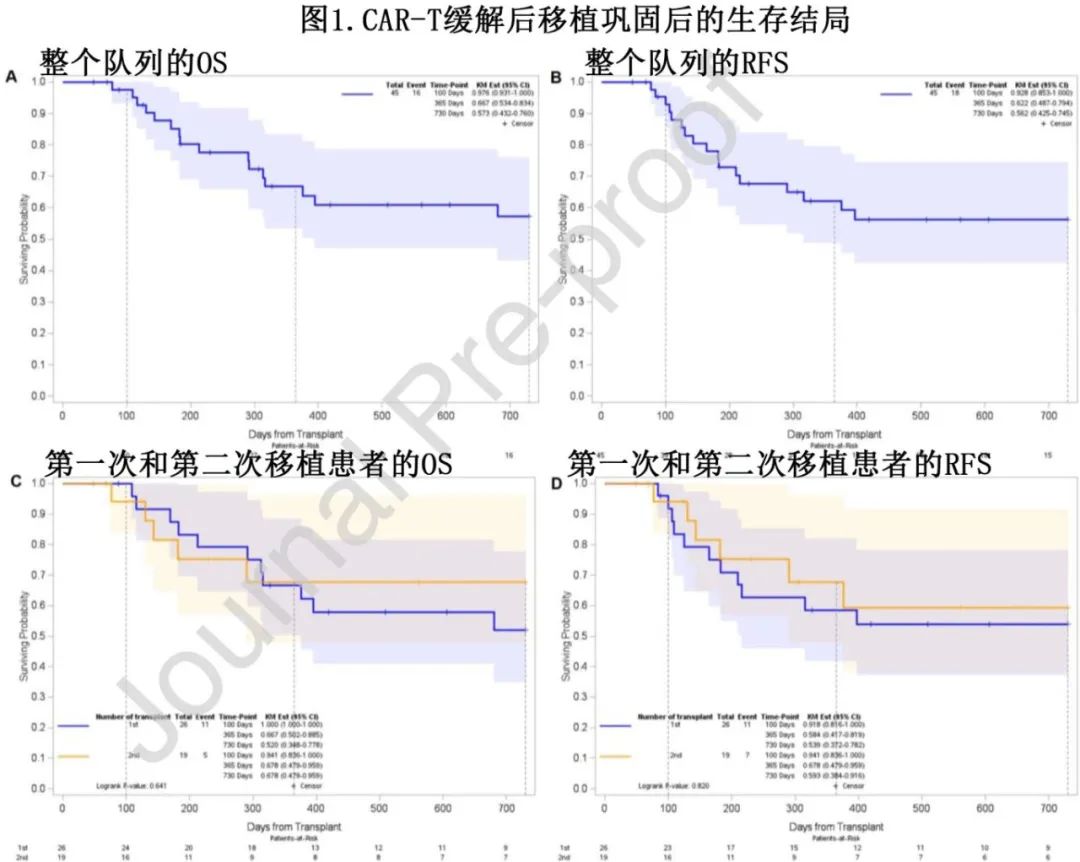
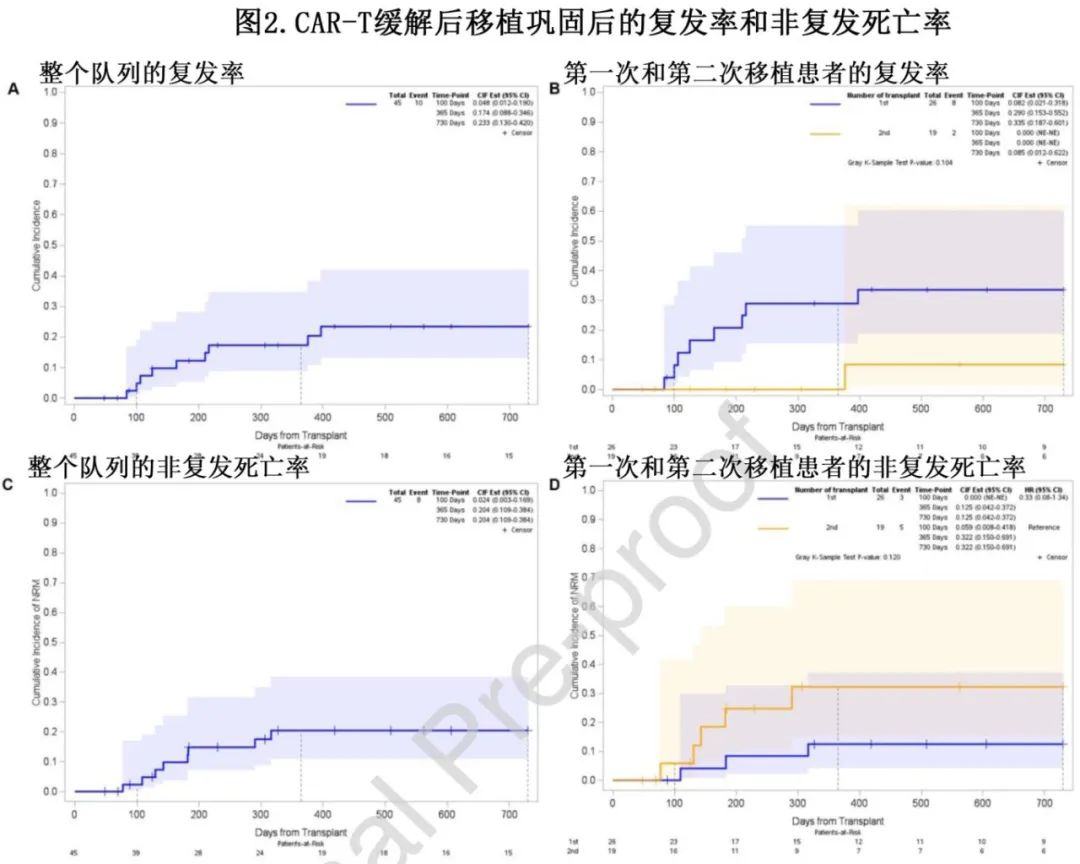
中位随访2.47年,2年总生存率(OS)、无复发生存率(RFS)、累计复发率(CIR)和非复发死亡率(NRM)分别为57.3%、56.2%、23.3%和20.4%。2年OS (52% vs. 68%,p=0.641)、RFS (54% vs. 59%,p=0.820)、CIR (33.5% vs. 8.5%,p=0.104)和NRM (12.5% vs. 32.2%,p=0.120)在第一次和第二次移植患者之间无显著差异。
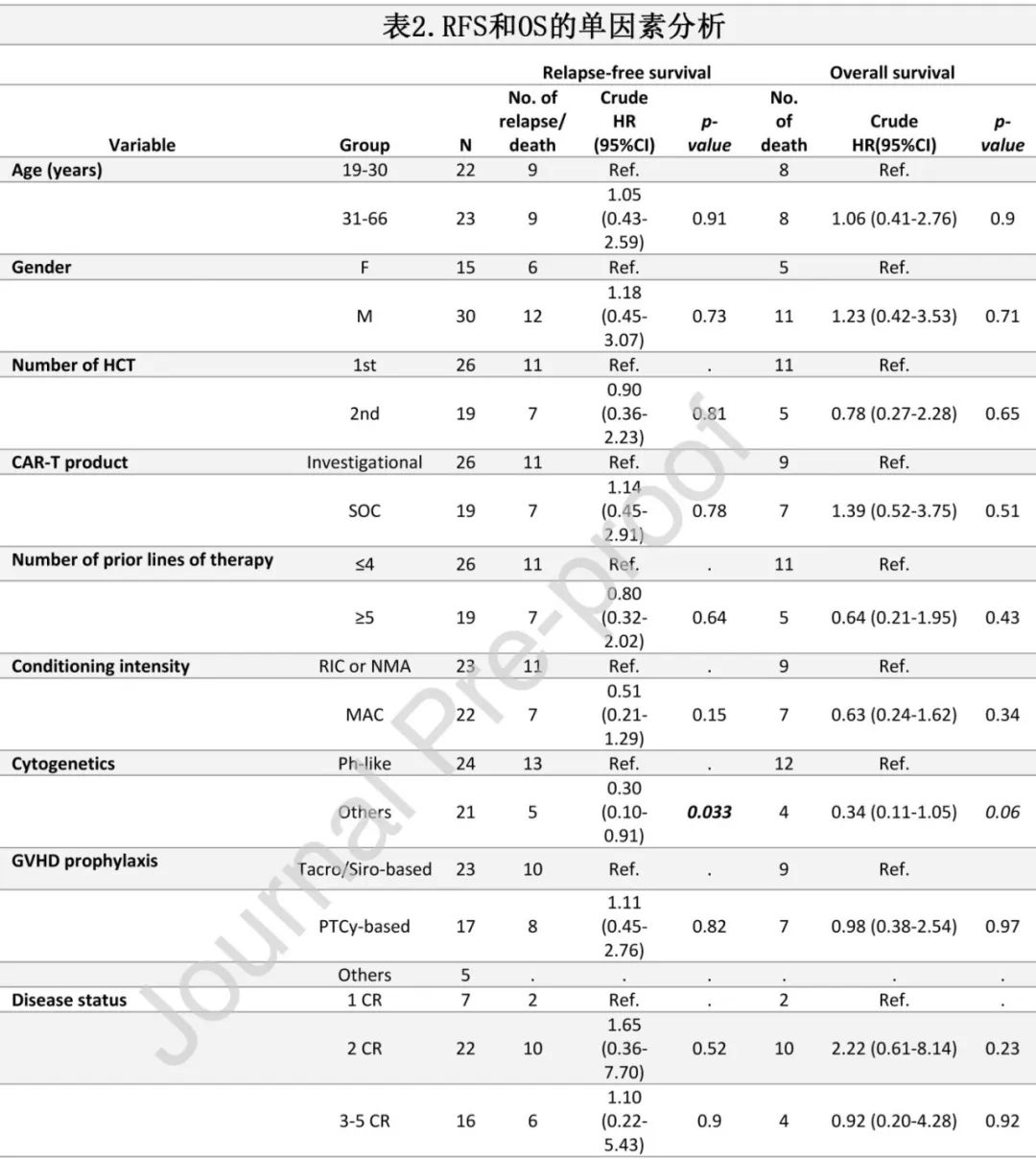
在单因素分析中,只有Ph样基因型与较差的RFS相关(HR=0.30,p=0.03),且与较差OS有临界相关性(HR=0.34,p=0.06)。
移植后至中性粒细胞恢复(>500 K/μL)的中位时间为16天,至血小板恢复(计数>20 K/μl)为24天。2-4级急性GVHD累积发生率为37.5%,慢性GVHD累积发生率为33.8%。
总结
对于成人R/R B-ALL高危患者,CAR-T缓解后alloHCT与相对较低的早期死亡率和令人鼓舞的生存结局相关,且适用于fit和适合移植患者的第二次alloHCT。虽然CAR-T后移植或不移植巩固的数据有限,但该研究结果支持移植的可行性、安全性和治疗潜力。因此,建议接受挽救性CAR-T治疗的R/R B-ALL成人患者早期考虑移植,特别是对于挽救性选择有限的高危患者。且最好在CAR-T输注之前就开始考虑移植,以便在达到缓解并且患者身心状态适合移植的情况下尽快移植。
参考文献
Aldoss I, et al.Consolidation with First and Second Allogeneic Transplants in Adults with Relapsed/Refractory B-ALL Following Response to CD19CAR T Cell Therapy, Transplantation and Cellular Therapy (2024), doi: https://doi.org/10.1016/j.jtct.2024.06.013
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#B-ALL# #CAR-T治疗# #B细胞急性淋巴细胞白血病#
64