Neurology:血管周围间隙扩张是小血管病的生物标记物
2021-06-18 MedSci原创 MedSci原创
EPVS在疾病早期也与SVD相关,支持EPVS是SVD标记物的假设,但不支持EPVS在AD早期发病机制中的作用。但与认知的相关性缺乏表明EPVS的临床重要性有限,特别是在AD的早期疾病阶段。
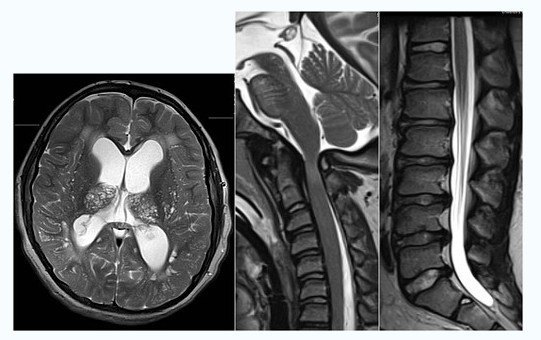
血管周围间隙是脑深部穿通动脉周围充满脑脊液的空腔。当它们扩张时,可以在MR图像上看到,然后被称为血管周围间隙扩张(EVPS)。EPVS被认为与白质间质液引流受损有关。与小血管疾病(SVD)、年龄和高血压有关。此外,一些研究表明EPVS与脑淀粉样血管病有关联,这可能存在于痴呆,特别是阿尔茨海默病(AD)中。Banerjee等人描述了半卵圆中心(CSO)中EPVS与AD之间的关联。然而,尽管一些研究表明EPVS与认知衰退之间存在关联,但其他研究未能证实这些发现。因此,CSO区、基底神经节(BG)和海马区(HP)的EPVS与AD的关系以及它们与认知衰退的关系尚不清楚。特别是EPVS在AD早期疾病阶段的作用研究较少。
Neurology杂志发表研究论文研究在认知未受损(CU)和轻度认知受损(MCI)人群中,CSO、BG和HP中EPVS与SVD和AD的测量(包括临床诊断、疾病相关的生物标志物和认知测量)之间的关系。并测试了EPVS和AD痴呆样本中年龄和白质病变匹配的CU参与者之间的相关性。

为了研究血管周围间隙扩张(EPVS)与阿尔茨海默症(AD)、小血管病(SVD)、认知、血管危险因素和神经炎症之间的关系,该研究分析了778名研究参与者的EPVS与不同相关神经影像,生化和认知之间的关联。
该研究纳入了瑞典早期及可靠地识别神经退行性疾病生物标志物(BioFINDER)研究中的499名认知无障碍(CU)患者、240例轻度认知障碍患者和39例AD患者。在MRI中确定CSO、 BG和海马的直径> 1 mm的EPVS;并采集海马体积、白质病变(WML)和其它SVD标记。β-淀粉样蛋白42(Aβ42),磷酸化tau,总tau和神经炎症标记物的CSF水平;用[ 18 F]-氟美他莫PET测定淀粉样蛋白的积累;确定并收集了血管危险因素和认知测试的结果。
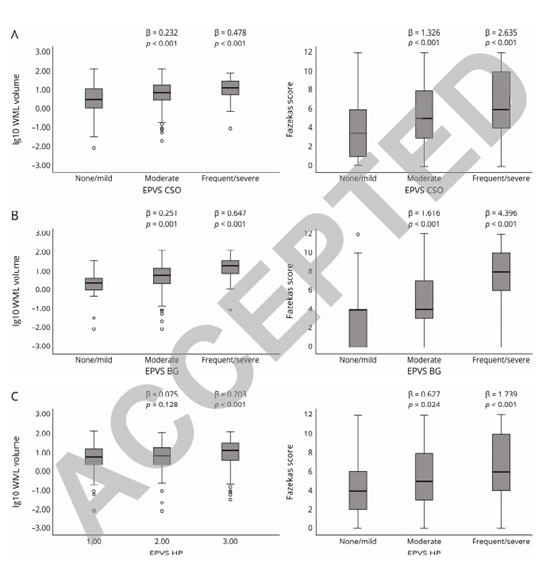
EPVS严重程度、WML体积Fazekas评分。结合CU和MCI样本的WML体积(lg10 WML体积)和EPVS严重程度的Fazekas评分,分别显示每个解剖区域的三个水平的EPVS测量(面板A-C)。p值来自以EPVS为预测因子的线性回归模型(以“无/轻度”水平作为参考组)。这些模型根据年龄、性别和诊断进行了调整。
CSO,BG和HP中的EPVS与无痴呆患者的WML量和Fazekas评分相关。EPVS和脑脊液Aβ42、总tau蛋白和tau蛋白磷酸化、神经炎症标志物、血管危险因素和认知测试之间没有发现关联。海马的EPVS与海马萎缩有关。在AD和CU的匹配人群中,HP的EPVS与AD诊断相关。
EPVS在疾病早期也与SVD相关,支持EPVS是SVD标记物的假设,但不支持EPVS在AD早期发病机制中的作用。但与认知的相关性缺乏表明EPVS的临床重要性有限,特别是在AD的早期疾病阶段。
原文出处
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Neurol#
78
#标记物#
98
#血管病#
70
#扩张#
0
#小血管病#
80