今日,施一公创立的诺诚健华递交港股上市申请
2019-10-17 佚名 医谷
今日(10月17日),根据港交所信息,诺诚健华(Innocare)已递交港股上市申请,联席保荐人为摩根士丹利和高盛。
今日(10月17日),根据港交所信息,诺诚健华(Innocare)已递交港股上市申请,联席保荐人为摩根士丹利和高盛。
公开资料显示,诺诚健华成由中国科学院院士、西湖大学校长施一公和前PPD旗下保诺科技总经理兼首席科学官、前美国默克集团心脏病学研发总监崔霁松联合创立,2015年11月3日在开曼群岛注册,2016年在中国开始研发,是一家处于临床阶段,专注于研究治疗癌症及自身免疫性疾病疗法的生物医药公司,截止目前,诺诚健华发现并研发了九种候选药物,包括一种处于注册性试验的候选药物、两种处于I/II期临床试验的候选药物及六种处于IND准备阶段的候选药物,其中进度最快的两个注册性试用于评价奥布替尼针对两种适应症(复发/难治慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)及复发难治套细胞淋巴瘤(MCL))的疗效,并预期将于今年年底向国家药监局提交新药申请。
诺诚健华的管线中有三种处于临床阶段并涵盖了主要癌症适应症且具有潜力成为同类最佳及╱或首创的肿瘤候选药物,包括Orelabrutinib(奥布替尼,酪氨酸激酶(BTK)抑制剂)、ICP-192(泛成纤维细胞生长因子受体(泛FGFR)抑制剂)及ICP-105(成纤维细胞生长因子受体4(FGFR4)抑制剂)。
新药研发监测数据库CPM显示,Orelabrutinib (ICP-022)为拥有全球自主知识产权的1类新药候选化合物,是创新性高效特异的BTK抑制剂,具有优异的激酶选择性和良好的成药性,具有自主知识产权,可用于治疗各种B细胞恶性肿瘤以及自身免疫性疾病。数据显示,Orelabrutinib比同类药物有更好的药物暴露量,剂量相关性药靶占有率高且持续时间长。目前Orelabrutinib正在进行针对上述适应症的PhaseI/II临床实验。据披露,公司正在从开展的注册性试验中评估ICP-022针对两种适应症(复发/难治慢性淋巴细胞白血病或小淋巴细胞淋巴瘤及复发难治套细胞淋巴瘤),并预计将于2019年底向NMPA提交新药申请。
ICP-192是基于结构优化设计的小分子靶向化药一类创新药,也是目前在中国处于研发阶段的首创的临床阶段泛FGFR抑制剂之一,具有抗多种实体肿瘤的活性、良好的安全性和类药性,抑瘤效果显着,目前在进行对具有FGFR2融合的胆管癌患者及具有FGFR2/3基因突变的尿道上皮癌患者初步集中进行延伸研究,同时计划进一步收集数据以评价ICP-192是否可作为治疗FGFR突变患者的联合治疗剂(例如免疫检查点抑制剂)的潜在治疗方案。
ICP-105是高特异性FGFR4抑制剂,具有优异的靶点选择性和良好的成药性,在FGFR4信号通路异常的肝细胞癌动物模型中的抑瘤效果显着,将为肝癌高发的中国患者带来安全性更高、疗效更好的全新治疗方案。目前正在中国的I期计量递增实验中进行临床评估已确定MTD及/或OBD。
此外,诺诚健华还有六种处于IND准备期的候选药物,招股书公布了两种,括ICP-723及ICP-330。ICP-723是一种第二代泛酪氨酸受主激酶(泛TRK)小分子抑制剂,用于治疗不同肿瘤类型的神经营养性酪氨酸激酶(NTRK)阳性的肿瘤患者以及由于抗性TRK基因突变而对第一代酪氨酸激酶(TRK)抑制剂产生耐药性的患者。ICP-330是TYK2小分子抑制剂,用于治疗各种T细胞介导的自身免疫性疾病,如银屑病、炎性肠病及系统性红斑狼疮。
另值得一提的是,诺诚健华现阶段正在广州建造一个占地50000平方米的生产设施用于商业化大规模生产,年产能为十亿粒药片,预期将于2020年第四季度完工并投入使用。该设施的设计遵守美国、欧洲、日本及中国的生产质量管理规范(GMP)规定。公司已组建销售及营销领导团队,且正在扩大商业化团队,预期截至2020年底将拥有80至90名销售代表。
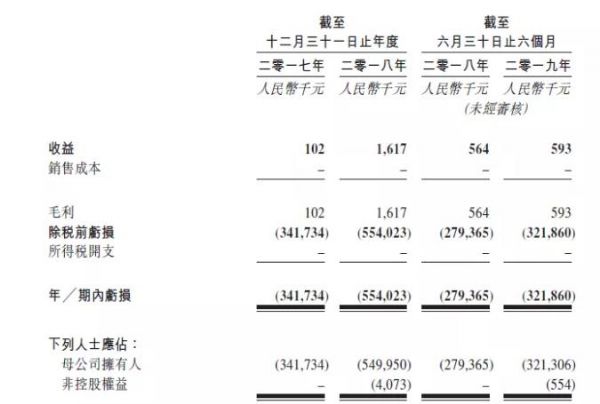
财务方面,由于诺诚健华的产品尚未获准进行商业销售,资料显示,截至2017年12月31日止年度及截至2018年12月31日止年度,经营亏损分别为人民币3.417亿元及为5.54亿元,且截至2018年及2019年6月30日止六个月,经营亏损分别为2.794亿元及3.219亿元。
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录











#施一公#创立的#诺诚健华#
145