【WSPH】肺动脉高压的移植选择
2024-10-01 肺动脉高压研究进展 肺动脉高压研究进展
讨论肺动脉高压患者移植方式及时机。双肺移植首选,介绍转诊及特殊情况,中心需考虑区域因素。新分配系统仍可能使肺动脉高压患者不利。

移植方式和最佳时机-移植类型
对于药物治疗难治的严重PH和RV衰竭患者,双侧肺移植(BLT)或HLT仍然是唯一可能延长生命的治疗选择。由于肺移植后RV几乎总是能充分恢复,因此BLT是首选。对于一些患有间质性肺病(ILD)和COPD/肺气肿以及轻度肺动脉高压的患者,单次肺移植可能就足够了。然而,尚不清楚应使用什么阈值或PH严重程度来做出此决定。一项研究表明,如果平均PAP且肺分配评分(LAS)<45(使用2015年修订前的LAS),特发性肺纤维化患者单次肺移植的结果是有利的。然而,一般来说,对于PH患者(包括患有实质肺疾病的患者),双肺移植的早期和长期结果优于单肺移植。单肺移植与较差的结果相关,并且更容易出现原发性移植物功能障碍(PGD)。
对于严重的PH,没有证据表明HLT与BLT相比可以改善预后。此外,联合HLT会对心脏捐赠者库产生不利影响。因此,我们不建议大多数PH患者接受HLT。HLT应保留用于三尖瓣后先天性心脏缺陷或共存左侧心脏病的患者。一项对442名接受移植的成年患者进行的队列研究联合器官共享网络(UNOS)登记处(1987-2018)诊断为艾森曼格综合征的BLT或HLT表明,房间隔缺损患者在BLT后比HLT后有更好的生存率,而患有更复杂疾病的患者先天性心脏病(例如室间隔缺损)在HLT后有更好的生存率。然而,这些结果可能没有考虑心肺阻滞与单独肺阻滞等待时间较长的影响。尽管许多计划考虑在手术时闭合不复杂的房间隔缺损,但也主张延迟经皮闭合以减少体外循环的暴露。另一种特殊情况是,在极少数情况下,肺动脉瘤或严重心脏肥大阻碍左肺植入可能会影响BLT结果。尽管有修复肺动脉瘤的手术技术,但HLT对于特定患者可能被认为更安全。
为了增加决策的复杂性,值得强调的是,对于患有严重PH和RV扩张/功能障碍的患者,估计LV内在收缩功能可能具有挑战性。人们还认识到,慢性扩张的右心室可能会影响左心室收缩和舒张功能。舒张性左心室功能障碍与较高的PGD风险和较差的长期结果相关。左心室收缩功能障碍也可能发生,并且与PAH患者的较差预后相关。目前尚不清楚左室收缩功能障碍最终如何与移植结果相关,但人们认识到左室功能障碍会使术后病程复杂化。尽管存在这些因素,但人们认为大多数风险与血流动力学因素有关,这些风险可以在PH患者术后早期阶段得到缓解,并且不应用作HLT的指征。
由于手术技术、免疫抑制和术后管理的进步,PH队列的肺移植后1年生存率现已超过90%。从历史上看,肺移植的早期死亡率高于其他移植适应症,证明这些患者在移植后可能会经历血流动力学挑战。从历史上看,PH患者进行移植后PGD的风险较高,随之而来的是发病率、死亡率的增加和长期移植物功能的降低。令人放心的是,如果PAH患者在肺移植后存活至1年,则BLT后条件中位存活期为10.0年;优于COPD(7.0岁)和ILD(6.9岁)队列。
转诊和列出移植的时间
表3列出了肺动脉高压移植的一般建议。作为患者治疗计划的一部分,我们提出肺移植的三个阶段,如下。1)关于移植概念和潜在治疗方法的讨论;2)转诊进行全面肺移植评估,以确定列入移植名单合理性及时间;3)肺移植列表(包括移植和桥接选项的优先顺序)。

ECMO:体外膜氧合;VA:静脉-动脉。#:我们希望建议程序为患者做正确的事情,而不仅仅是他们“知道如何做”的事情;如果需要,送往专门的中心。
我们建议PH患者在病程早期被转诊以促进教育,并为患者提供关于移植选择的初步讨论的机会。这将为帮助患者解决最初可能排除资格的可改变因素提供时间,例如财务资源、体重指数升高或降低、疫苗接种、身体状况不佳和社会支持或物质滥用障碍(例如吸烟)。对于不隶属于肺移植项目的PH项目,我们建议他们与多学科移植项目建立正式联系。此外,我们主张将移植作为一种治疗选择纳入肺科、心脏病学以及心胸外科医师培训课程中。我们建议诊断时处于高风险和/或未能达到治疗目标的患者应尽早考虑转诊、评估并最终列入移植名单。此外,对于具有高风险特征和诊断的患者,我们建议在诊断后尽快向患者介绍移植作为潜在治疗选择的概念。这种对话可以由PH医生发起,随后与移植提供者进行讨论和教育。其基本原理是,对于高危患者,其轨迹是不可预测的,即使面对最佳的医疗管理,许多患者也无法达到治疗目标。这些早期讨论的目的是为护理团队和患者识别出较高风险的患者,以便在最大程度的药物治疗未能达到治疗目标的情况下,他们都可以更好地准备转诊进行评估。需要强调的是,患有高风险诊断(硬皮病、肺静脉闭塞病、合并肺纤维化和肺气肿综合征)的患者,这些患者有对药物治疗难治性或不适合这些治疗的风险,或者那些患有不成比例的疾病的患者诊断后不久即可标记出合并症对其生活质量的负担和高死亡率,因为肺移植的风险/效益平衡可能会在初次诊断后不久出现。
对于患有晚期疾病或未能达到治疗目标的患者,我们建议转诊进行移植评估。患者是否适合移植应由移植计划与PH团队合作,根据当前公认的受者选择标准来确定。欧洲心脏病学会(ESC)和欧洲呼吸学会(ERS)风险算法以及评估早期和长期PAH疾病管理登记处(REVEAL)风险计算器已被用作移植转诊的标准,并且列表已纳入治疗中最近的ESC/ERS指南声明中的算法。尽管风险分层工具可以帮助识别高风险群体,但这些工具不应单独使用来告知何时转诊患者进行移植评估和列出。需要考虑血流动力学数据、右心室功能、生活质量、共存疾病、合并症、血型、患者体型、候选者敏化状态、候补时间和进入器官捐献库的情况,以决定转诊患者进行移植评估。
表4列出了有关转诊移植指征和列出患者进行移植的决定的建议。
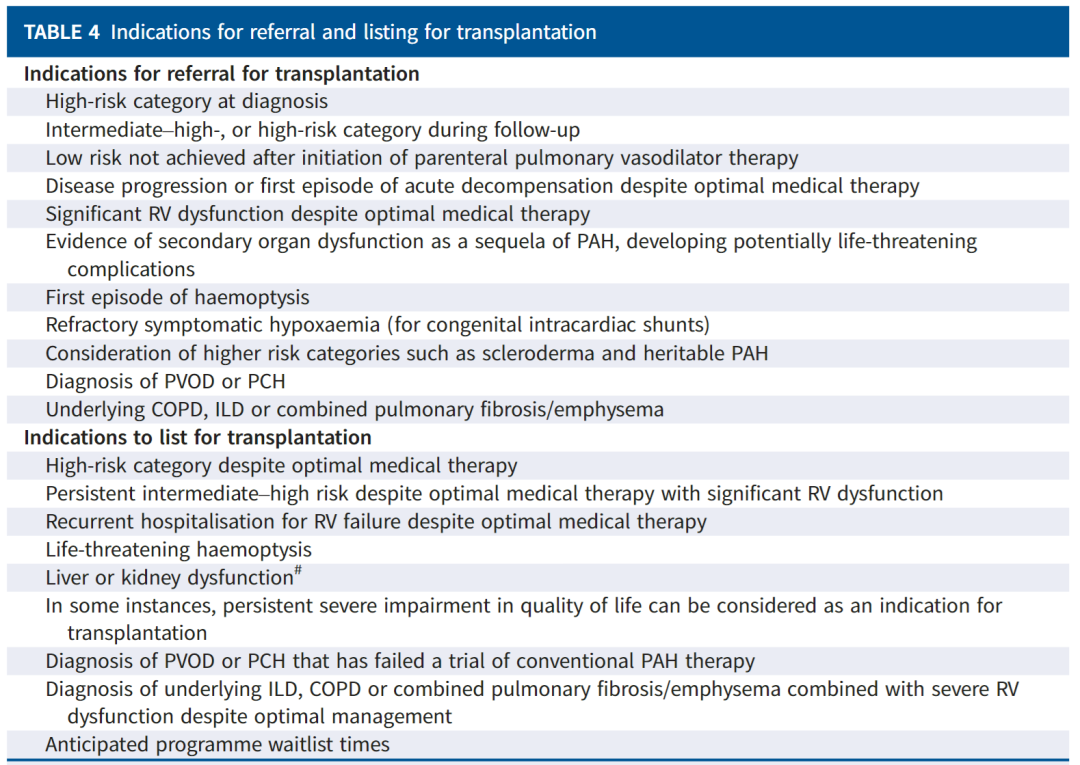
RV:右心室;PAH:肺动脉高压;PVOD:肺静脉闭塞病;PCH:肺毛细血管瘤;ILD:间质性肺疾病。#:理想情况下,患者将在重症监护病房入院或终末器官损伤之前被列出。
特殊情况-实质肺疾病
潜在肺实质疾病的存在也应促使早期转诊进行肺移植。与慢性阻塞性肺病、肺纤维化和结节病等潜在肺部疾病相关的肺PH与高死亡风险相关。除了较低的生存率之外,这些患者的医疗治疗的局限性和合并症的负担也要求早期转诊,并可能将符合标准的患者列入名单。即使传统的PAH疗法应用于轻度ILD患者,结果也比没有ILD的患者更差。轻度ILD患者有更多合并症,因此尚不清楚该组死亡率过高的原因是什么。合并ILD和肺气肿(CPFE)的患者的PH诊断值得一提。PH经常使CPFE复杂化并预示预后不良。在法国的一项登记中,40名患者的一年生存率仅为60%,平均PA压力、肺血管阻力、心率和肺一氧化碳弥散能力较高与较差的结果相关。
硬皮病
硬皮病患者应被视为高风险并尽早转诊进行移植评估。他们的RV功能通常本质上较差,因此他们的RV可能不太能够适应高RV后负荷。此外,他们可能对靶向PAH药物反应较差,特别是同时存在ILD和/或静脉受累的情况。硬皮病患者的PAH患者在移植后具有与其他PAH亚组相似的结果。然而,这些患者代表的是经过精心挑选的患者群体。硬皮病患者通常会因食道运动障碍和细菌过度生长而导致胃肠道转运时间改变,并容易因胃食道功能低下和反流疾病而发生吸入。由于迷走神经的破坏和药物可能进一步损害肠道蠕动,移植后这些挑战往往会加剧,使它们在移植后面临更高的误吸风险,可能导致肺炎和慢性同种异体移植功能障碍。此外,硬皮病患者可能患有严重的外周血管疾病或内在肾脏疾病,这两种疾病不仅影响他们接受移植的资格,还影响他们接受体外支持的资格。最后,在评估硬皮病患者的残疾程度和症状时,必须强调肺外因素可能导致其残疾程度,并且这些因素不会通过移植得到解决。
艾森曼格综合症
艾森曼格综合征患者,特别是接受三尖瓣后分流的患者比其他原因引起的肺动脉高压患者的生存率更高。患有三尖瓣后分流(室间隔缺损或动脉导管未闭)的患者通常具有适应良好的右心室,可以产生超过全身循环的压力。因此,移植转诊和最终列入该人群的指征具有挑战性,特别是因为三尖瓣后分流患者更常被列入HLT;等待时间较长且捐赠者池有限的程序。移植指征通常与慢性低氧血症对器官功能、生活质量或支气管循环的影响有关,这些影响可能导致反复咯血。一般来说,这些患者在移植后状况良好,结果与其他PAH诊断相似。
中心和国家相关因素
除了与患者相关的因素外,中心还需要考虑区域器官的可用性和等待时间,这可能受到捐赠者可用性以及患者因素的影响,例如身高(告知肺部大小)、血型、移植类型和敏感性。从历史上看,与其他诊断相比,许多国家使用LAS来分配肺部,使PAH患者处于不利地位。这可能与该组患者早期死亡率较高有关。2015年,对LAS进行了修订,以改善这种不平等,但即使进行了这些调整,PAH候选者仍然被发现具有最高的候补死亡率和最低的移植可能性。对PAH患者获得肺部公平性的调查结果的担忧也得到了回应接受ECMO作为过渡策略的PAH患者。在UNOS登记的1064名患者队列中,与PAH患者相比,阻塞性肺病、囊性纤维化和ILD患者在ECMO桥接期间接受移植的可能性分别高出78%、69%和62%。重要的是,尽管ILD和PAH的30天死亡率高于囊性纤维化,但所有诊断组的1年结果相似。在美国,当前的LAS于2023年3月被肺部综合分配评分(CAS)取代。肺部CAS寻求平衡生存和紧迫性的权重,并考虑其他与患者相关的因素以及是否可以随时获取器官。肺CAS的目的是平衡生存和紧迫性的权重,同时考虑其他患者相关因素和器官获取情况。尽管数量很少,但CAS6个月和1年的评估结果仍然表明,与其他诊断群体相比,患有PAH的候选人可能仍然处于不利地位。器官采购和移植网络(OPTN)认识到了这一点,并更新了数据收集,纳入与风险评估相关的要素,以进一步完善CAS,以适应分配系统的未来迭代。2022年12月,OPTN批准纳入从REVEAL风险评估分数中获取的风险评估要素。数据点包括纽约心脏协会功能分级、BNP/NT-proBNP、心包积液证据、大咯血证据、弥散能力、平均右心房压力和肺血管阻力。
由于PAH的演变是不可预测的,因此一些国家已针对短期内预后不佳的难治性RHF患者实施了优先分配计划。优先获得移植是开发和促进使用VA-ECMO作为PH患者移植桥梁的重要工具。Eurotransplant的成员(德国、荷兰、比利时、奥地利)在LAS中添加了特殊LAS系统(eLAS)。如果患者计算的LAS不能准确反映移植的紧迫性,移植中心可以申请eLAS。在法国和英国这两个不使用LAS评分的国家,对于入住ICU的严重RHF在最大程度的医疗治疗(包括持续服用正性肌力药物和药物)超过72小时后仍未改善的患者,可以申请国家优先名单。PH的联合治疗。这些紧急分配规则的制定导致名单上的PH患者死亡率大幅降低,并降低了因严重RHF入院的最年轻患者的ICU死亡率。在美国,移植中心针对以下任何属性向国家肺脏审查委员会提交CAS例外请求:生物学劣势、医疗紧急性、患者可及性和移植后存活率。对于符合恶化临床标准的PAH候选者,移植中心可以申请肺CAS等待名单存活率和移植后结果组成部分的第90个百分位。最后,鉴于PAH移植数量相对较少以及管理固有的复杂性,我们建议在可行的情况下考虑转诊至具有ECMO专业知识的较大规模中心。
参考文献:
Savale L, Benazzo A, Corris P, Keshavjee S, Levine DJ, Mercier O, Davis RD, Granton JT. Transplantation, bridging, and support technologies in pulmonary hypertension. Eur Respir J. 2024 Aug 29:2401193. doi: 10.1183/13993003.01193-2024. Epub ahead of print. PMID: 39209471.
作者:肺动脉高压研究进展
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#肺动脉高压# #肺移植#
40