Adv Sci:周子健/于春阳/唐龙光合作设计超小纳米点FerroD用于急性肾损伤治疗
2024-08-22 iNature iNature
该研究设计了由两亲共轭物(四苯乙烯-L-丝氨酸-去铁胺,TPE-lys-Ser-DFO(TSD))和包裹的铁抑素-1组成的超小纳米点,称为FerroD。
已知铁死亡会介导化疗药物引起的急性肾损伤(AKI)的发病机制;然而,利用基于铁死亡的治疗益处来保护肾脏仍然具有挑战性。
2024年8月19日,厦门大学周子健、上海交通大学于春阳及高州市人民医院唐龙光共同通讯在Advanced Science 在线发表题为“Ultrasmall Nanodots with Dual Anti-Ferropototic Effect for Acute Kidney Injury Therapy”的研究论文。该研究设计了由两亲共轭物(四苯乙烯-L-丝氨酸-去铁胺,TPE-lys-Ser-DFO(TSD))和包裹的铁抑素-1组成的超小纳米点,称为FerroD。
通过肾损伤分子-1介导的内吞作用内化后,FerroD可以同时去除超载的铁离子并通过配位-拆卸机制消除脂质过氧化物的过量产生,这两者共同赋予了对铁死亡的显著抑制效率。在顺铂(CDDP)诱导的AKI小鼠中,具有双重抗铁死亡能力的FerroD可以提供长期的肾脏保护作用。这项研究可能为针对各种铁死亡相关肾脏疾病的铁死亡治疗方法的设计和临床转化提供新的启示。

接受化疗的患者由于化疗药物不可避免地通过肾脏排泄,经常面临急性肾损伤(AKI)的高风险。化疗药物引起的AKI以肾功能迅速恶化为特征,可能发展为晚期并发症,包括慢性肾脏病、肾衰竭和死亡。一般而言,AKI的发病机制涉及多种受调控的细胞死亡方式,包括铁凋亡、坏死性凋亡和细胞焦亡。其中,铁死亡是一种由铁依赖性脂质过氧化驱动的细胞死亡形式,已被证明通过释放损伤相关分子模式(DAMP)以波浪式方式引发肾小管坏死。
同步的铁死亡肾细胞随后引发第二波炎性细胞因子介导的坏死,如坏死性凋亡和细胞焦亡,从而加剧肾功能障碍(图1A)。在这方面,提出了针对铁死亡的治疗方法,以减少最初的细胞死亡波,从而更好地治疗AKI。最近的研究表明,单剂量预防性使用铁死亡抑制剂可以有效缓解AKI,而在AKI的情况下针对继发性坏死则需要多次剂量。此外,我们小组先前开发了一种基于青蒿素的探针(Art-Gd)用于铁死亡的增强磁共振成像(feMRI),为铁死亡参与了AKI的早期阶段。总之,认识到铁死亡作为目标机制可以受益于AKI的早期诊断成像和治疗干预。
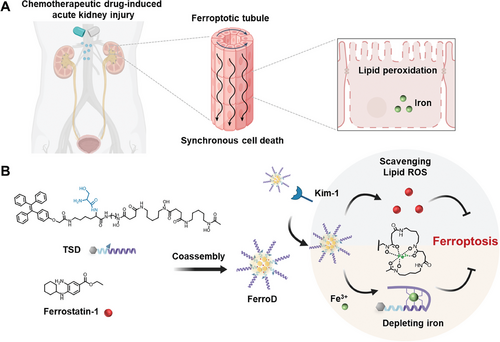
具有双重抗铁电效应的超小纳米点用于急性肾损伤治疗的示意图,表示为FerroD(图源自Advanced Science )
肾脏细胞因氧化还原调控机制失调而发生铁死亡,最终导致多不饱和磷脂和不稳定铁离子的大量过氧化。过氧化物自由基的清除和过量铁的螯合可以有效减少肾脏上皮细胞的丢失,恢复功能障碍的肾脏。自由基捕获抗氧化剂铁蛋白酶抑制剂-1(Fer-1)和铁螯合剂去铁胺(DFO)被广泛用作肾脏疾病的铁死亡抑制剂,并已被证明在各种药物诱导的AKI模型中提供肾脏保护作用,例如顺铂(CDDP)和叶酸诱导的AKI。然而,由于DFO的药代动力学不良和非特异性体内生物分布,其抗铁死亡作用在很大程度上受到损害。
同样,Fer-1在血浆中的不稳定性及差的溶解性在很大程度上限制了其抑制AKI背景下的铁死亡。纳米药物由于其独特的物理化学性质而为传统药物提供了有希望的替代品。通过整合肾脏靶向部分(即肾小管靶向修饰剂L-丝氨酸)和成像部分,例如正电子发射断层扫描(PET)和磁共振成像(MRI),可以纵向监测肾脏损伤,从而使AKI的治疗方案受益。利用纳米材料的优点,过去十年在开发基于铁死亡的AKI纳米药物方面取得了巨大进展。然而,由于单一的铁死亡抑制机制(涉及清除脂质过氧化或螯合铁离子),肾脏保护效果通常较差。因此,开发配备多种铁死亡抑制机制的纳米平台被认为是一种提高治疗效果的高效策略,因为不同机制之间存在潜在的协同作用。
在这项工作中,作者报道了超小纳米点FerroD,它由两亲性共轭物(四苯乙烯-L-丝氨酸-去铁胺,TPE-lys-Ser-DFO(TSD))和包埋的Fer-1组成,用于治疗AKI。TSD可以组装成纳米颗粒并用Fer-1封装以获得FerroD。通过调整TSD和Fer-1之间的重量比,我们获得了可以跨越肾脏过滤阈值的超小FerroD纳米点。此外,由于肾损伤分子1(Kim-1)是AKI早期特异性上调的蛋白质,L-丝氨酸修饰的FerroD纳米点可以利用Kim-1和丝氨酸之间的相互作用促进细胞内化。有趣的是,与Fe(III)螯合后,FerroD发生分解,并通过配位-分解机制释放被捕获的Fer-1。利用这种释放机制,FerroD可以同时发挥脂质过氧化清除和铁螯合能力,以抵消肾脏铁死亡细胞死亡,从而提高肾脏保护作用。此外,我们使用了之前开发的针对铁死亡的MRI探针Art-Gd,来跟踪FerroD对CDDP诱导的AKI小鼠的长期抗铁死亡作用。总之,这项工作旨在阐明针对铁死亡机制的纳米药物联合治疗的合理设计是缓解药物引起的AKI的有效方法。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202403305
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#急性肾损伤# #FerroD#
42