2018 CSCO:新数据!免疫治疗在晚期肝胆胰恶性肿瘤中的疗效和安全性
2018-09-30 肿瘤资讯 肿瘤资讯
肝胆胰恶性肿瘤一直缺乏有效的药物,疗效预后不良,免疫治疗上市后,给肝胆胰恶性肿瘤带来一个新的希望。2018年CSCO年会上,来自浙江大学医学院附属第一医院的吴丽花博士作了关于评估信迪利单抗在中国晚期肝胆胰恶性肿瘤患者中的有效性与安全性的报道,引起了广泛的关注。研究也初步肯定了信迪利单抗在治疗晚期恶性肝胆胰肿瘤方面的有效性和安全性。
研究背景
信迪利单抗(Sintilimab)是由礼来公司和信达生物在中国共同合作开发的重组全人源IgG4亚型PD-1单克隆抗体。由于其避免了IgG1亚型的ADCC效应,因而体现出更好的成药性。同时,信迪利单抗具有高亲和力,临床前研究显示其亲和力比pembolizumab高10倍,比nivolumab高50倍。研究还发现,信迪利单抗有很好的受体占位率。在给药后的24小时即可达到接近100%的占位率,且在28日内维持这一水平。而在nivolumab中仅看到60%-80%的占位率。信迪利单抗更高的受体占位水平,可能带来更好的疗效。
该研究的主要目的,在于评价信迪利单抗在晚期肝胆胰恶性肿瘤中的安全性与耐受性,评估其初步的抗肿瘤活性。
研究方法
临床试验分为ⅠA、ⅠB期临床研究,ⅠA期是经典的3+3设计,共分为4组,第一组是1mg/kg体重,每两周给一次药;第二组是3mg/kg体重,每两周给一次药,其平行组为200mg,每三周给一次药;最高的剂量组是10mg/kg体重,每两周给一次药。在完成队列A2和A3的研究,即平行的两个剂量组研究后,我们开始进行ⅠB期拓展研究,选用的剂量为200mg,每三周给一次药,入组患者按不同肿瘤类型进入6个队列。在整体ⅠA、ⅠB期临床研究中共入组41例肝胆胰恶性肿瘤患者,在3+3爬坡ⅠA期临床研究的第一个剂量组,即1mg/kg体重,每两周给一次药,入组1例;在较高的剂量组,即10mg/kg体重组,入组2例;同时在ⅠA期里还有2例进入到平行组的200mg,每三周给一次药。另有36例是在ⅠB期的临床研究中入组的。所有受试者用药至疾病进展,或毒性不能耐受。治疗期间每9周进行一次影像学评估,相当于三个疗程进行一次评估。研究允许首次进展以后的再用药。入组41例患者中,男性25例,女性16例,中位年龄为51岁。肿瘤分期92%为四期,有80%患者为肝胆肿瘤,另外20%为胰腺和壶腹部的肿瘤。其中80%患者处于二线及以上的治疗阶段。
研究结果
目前为止,中位随访时间为17个月,全部患者接受过至少一次用药,中位用药次数是5次,最长的已达44个疗程,可评估疗效的患者有36例,完全缓解的有1例(为胆管癌),部分缓解患者4例,疾病稳定患者9例,ORR(客观缓解率)为13.9%,DCR(疾病控制率)在38.9%,其中有两例评价为PD的患者选择继续用药后获得SD(根据irRECIST标准)。
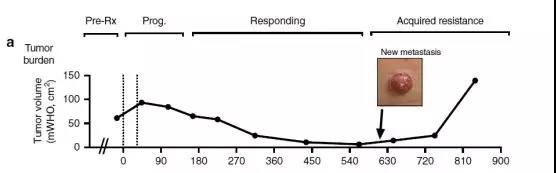
目前为止,中位缓解持续时间(mDOR)尚未达到,在5例获得CR或PR的受试者中,有1例患者出现疾病进展。该患者在第一次疗效评估时即达靶病灶CR,至12个疗程时还是CR,但到第15次用药时在肝脏中出现一个新的病灶,该病灶接受了消融治疗。患者目前处于稳定状态,无新发病灶。中位无进展生存期PFS约为67天,中位总生存时间OS约为11.4个月,目前获得OS的事件发生率是36.6%。
结论
作者:肿瘤资讯
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#疗效和安全性#
64
谢谢梅斯提供这么好的信息,学到很多
72