






作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言























作者:佚名

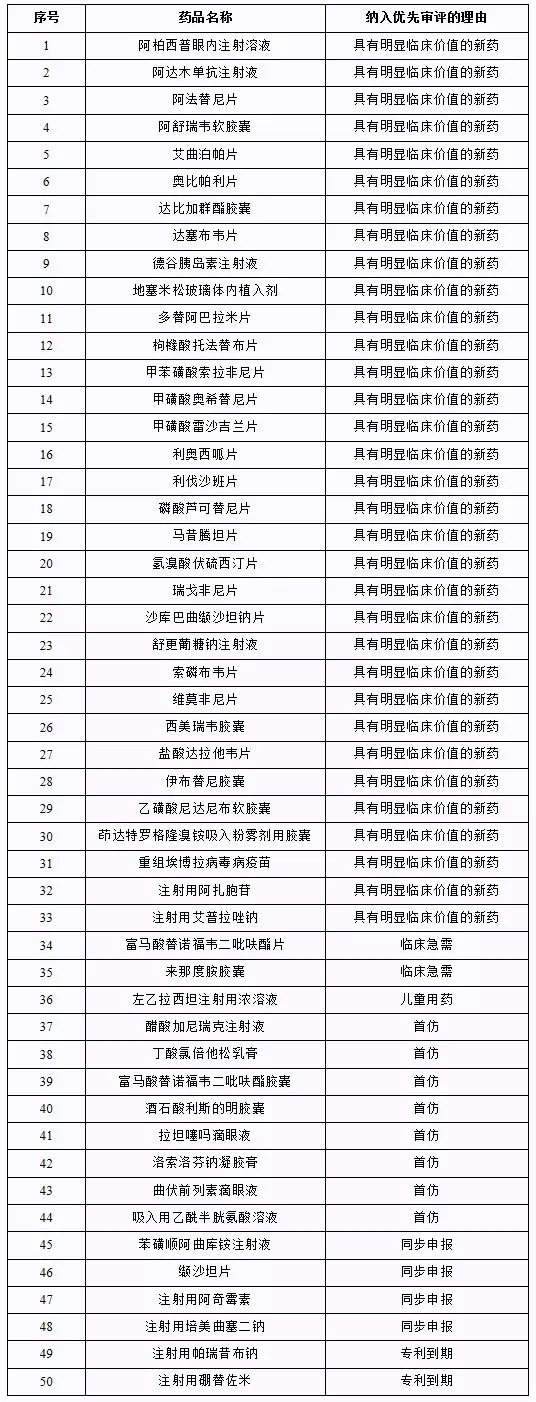
为加快重大新药创制科技重大专项(以下简称“新药专项”)创新成果产出进程,根据有关文件规定和专家评审遴选建议,拟推荐法米替尼等18个专项支持的药物品种为优先审评品种。 现将拟推荐的品种予以公示。公示时间为2015年1月13日至2015年1月22日。如有异议,请实名反馈至我办。 联系电话:010-68792529 传 真:010-68792226 邮&nbs
自2015年8月国务院下发《关于改革药品医疗器械审评审批制度的意见》(44号文)之后,我国开启了药品审评审批制度上全方位的改革,而CFDA药品审评中心的工作也更受瞩目。
尽管在药品审评审批体制机制上已经持续改革,但食药监这次放出的“大招”还是让业界有些诧异。日前,食药监总局发布进口药品注册管理有关决定,拟准许境外未注册或尚未进入临床实验的药品可在国内进行国际多中心临床实验,已经在国内完成临床实验之后,可直接提出药品上市注册申请。
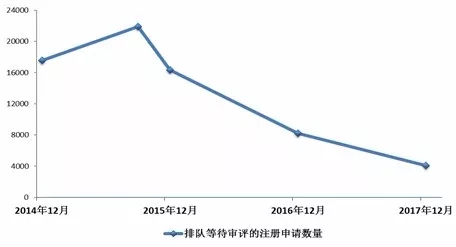
国家食品药品监督管理总局局长毕井泉受国务院委托,向全国人大常委会报告药品管理工作情况时表示,我国目前基本消除了药品注册申请积压,等待审评的药品注册申请已由2015年高峰时的22000件降至6000件。化学药和疫苗临床试验申请、中药各类注册申请已实现按时限审评。毕井泉介绍,为解决长期以来形成的药品注册积压、新药上市慢、制药行业低水平重复、创新能力不足等突出问题,2015年8月国务院印发《关于改革药品
为加快推进药品审评审批制度改革,促进国家总局及省局技术审评优势互补,共同推进药品技术审评能力建设,5月26日,国家食品药品监督管理总局药审中心与山东省食品药品监督管理局签署战略合作协议。总局副局长孙咸泽出席签字仪式并讲话。
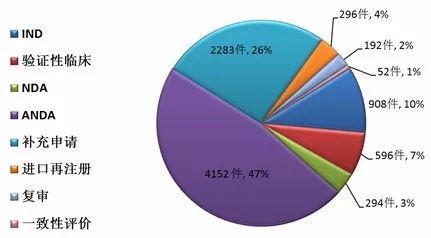
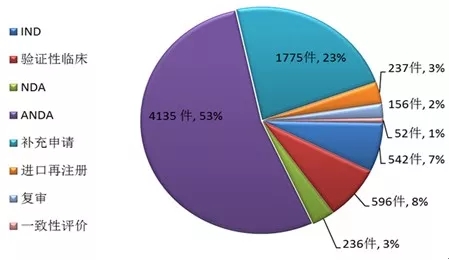
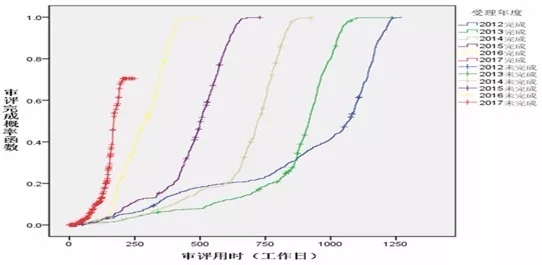
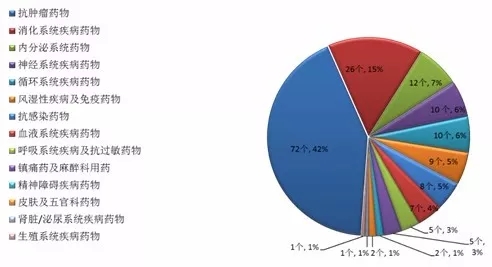
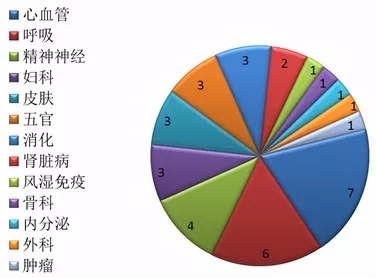
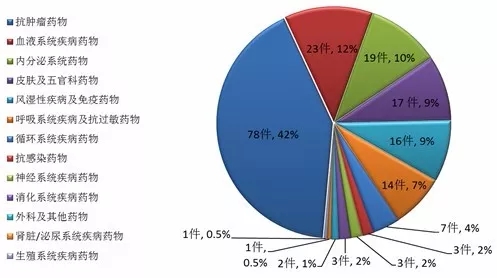
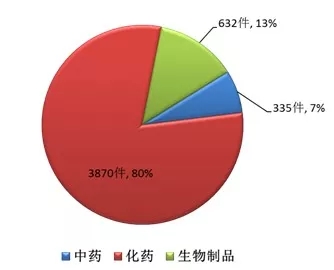
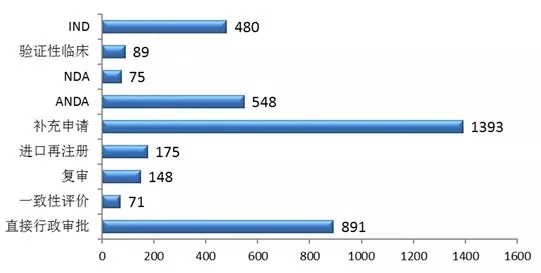
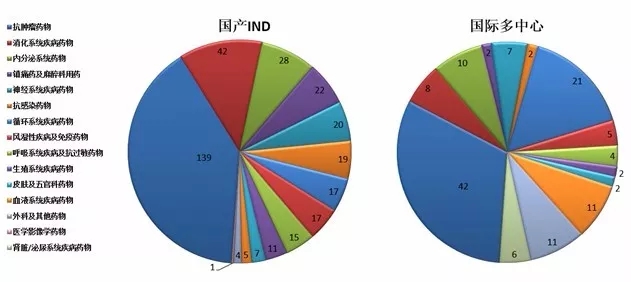
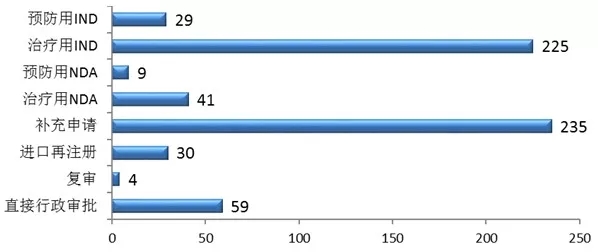
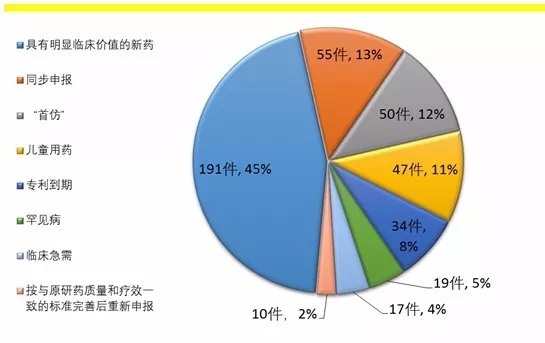
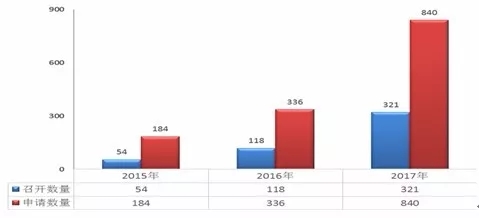
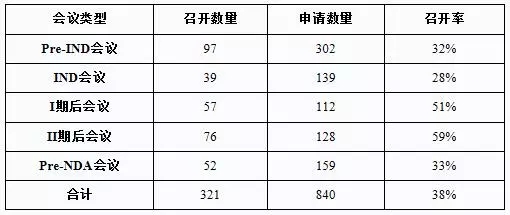
Insight数据库2017年终报告梳理了2017年CDE药品申报和审评的数据情况,让大数据来为你指路。


梅斯医学MedSci APP
医路相伴,成就大医
#CFDA#
31
#药品审评#
30
学习了受益匪浅
74