三家国内PD-1/PD-L1获批临床 肿瘤免疫火热 患者招募难?
2017-09-22 科比crossover 新浪医药新闻
最近关注国内PD-1的朋友们上周应该也看到了恒瑞PD-L1抑制剂SHR1316注射液、广州百奥泰生物PD-1抑制剂重组人源化抗PD-1单克隆抗体注射液以及康方生物PD-1抑制剂AK103同一天获批临床,这也意味着国内肿瘤免疫疗法又增加新的玩家。

最近关注国内PD-1的朋友们上周应该也看到了恒瑞PD-L1抑制剂SHR1316注射液、广州百奥泰生物PD-1抑制剂重组人源化抗PD-1单克隆抗体注射液以及康方生物PD-1抑制剂AK103同一天获批临床,这也意味着国内肿瘤免疫疗法又增加新的玩家。
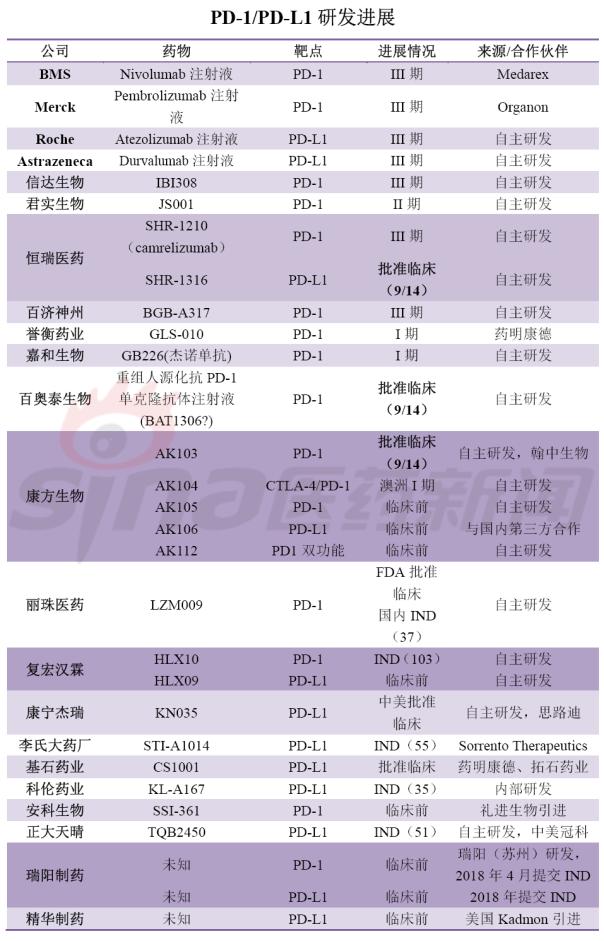
从今年的四川科伦博泰把肿瘤免疫治疗单克隆抗体专利(猜测PD-1单抗)国外权益以400万美元首付、2650万美元总里程碑付款,到药明生物/誉衡药业把GLS-010国外权益许可给Arcus,后者支付1850万美元的前期许可费,里程碑付款可达4.225亿美元。中国生物科技海外许可越来越常见,不仅有类似于恒瑞、百济神州、信达生物、康方生物的海外授权与合作,也有类似于李氏大药厂、精华制药从国外引进PD-L1。
当你还在做肿瘤免疫疗法的时候,国外已经在联合疗法上迅速突破,肿瘤免疫抑制剂+小分子抑制剂已经是一种趋势。要么是百济神州自己PD-1与PARP、BTK、IDO、EGFR、Braf等小分子组合,要么是信达生物从上海有机所买入IDO,或者是恒瑞自己内部小分子组合,那么剩下的那些大分子药物该如何组合,是引进亦或是联合开发?贝达药业、亚盛医药等小分子研发也许是不错的考虑。
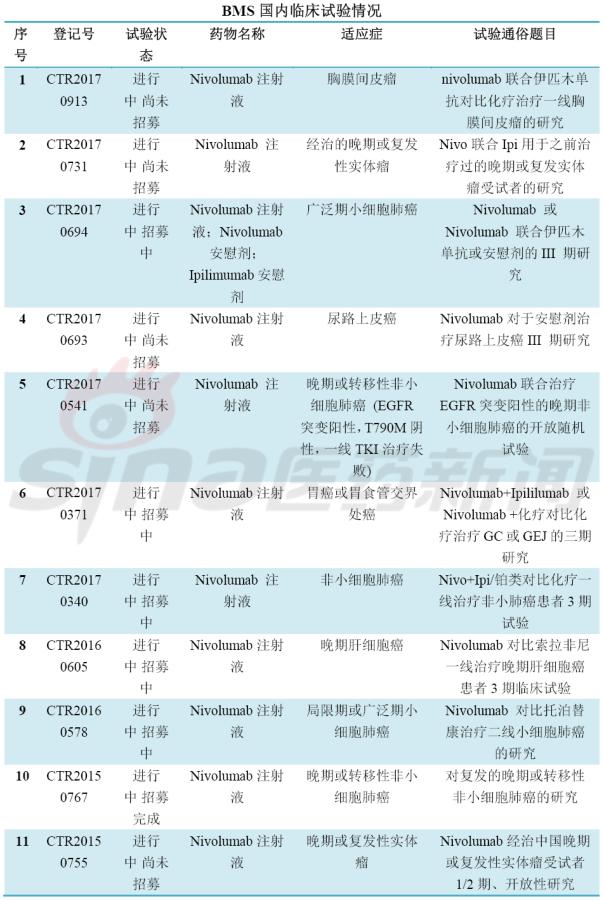
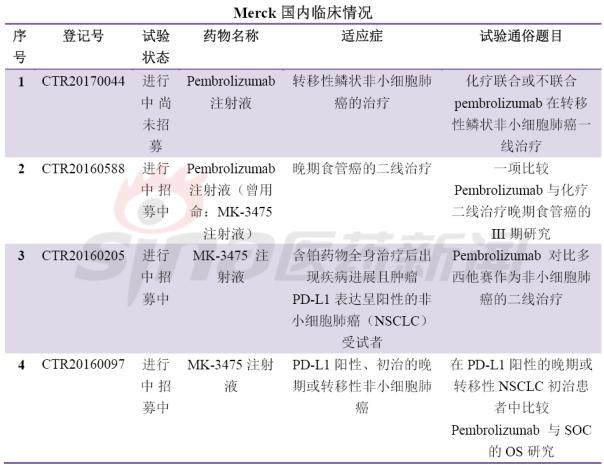
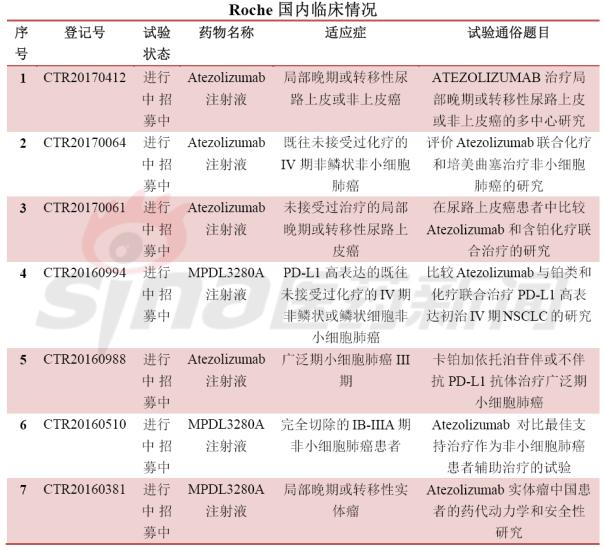
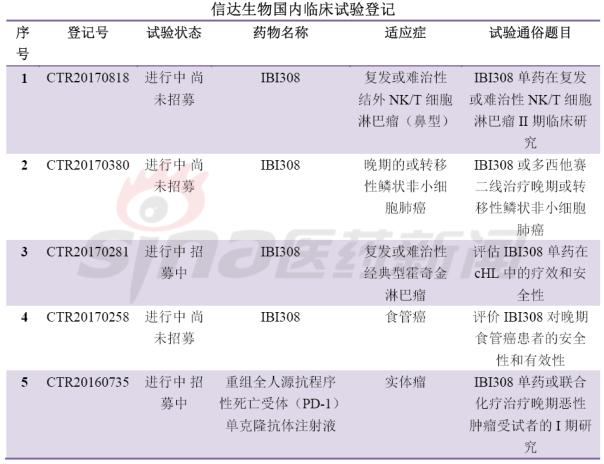
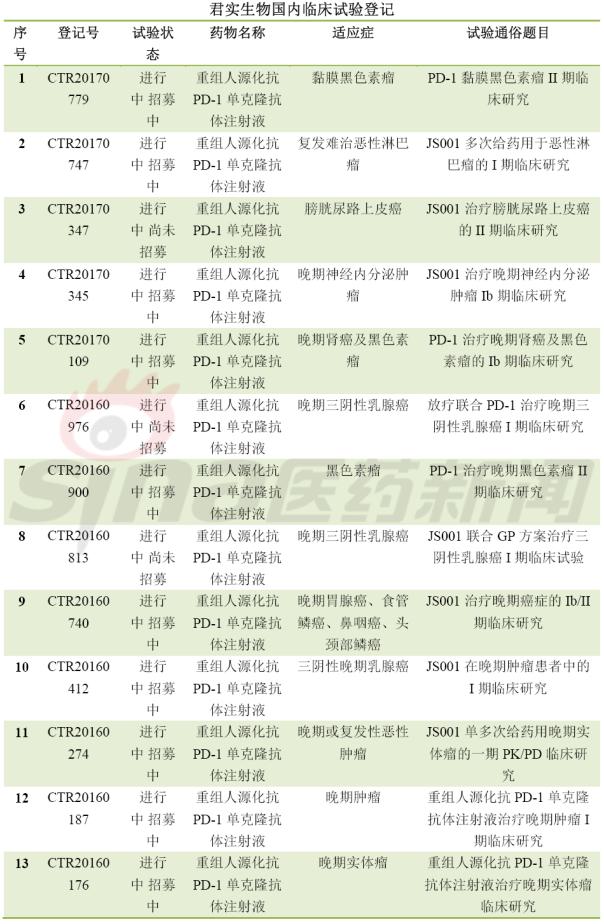
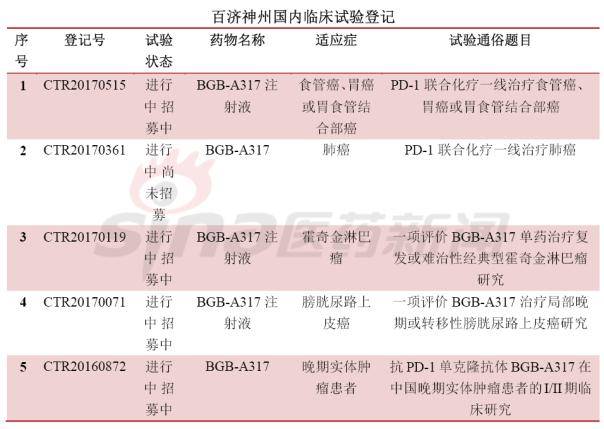
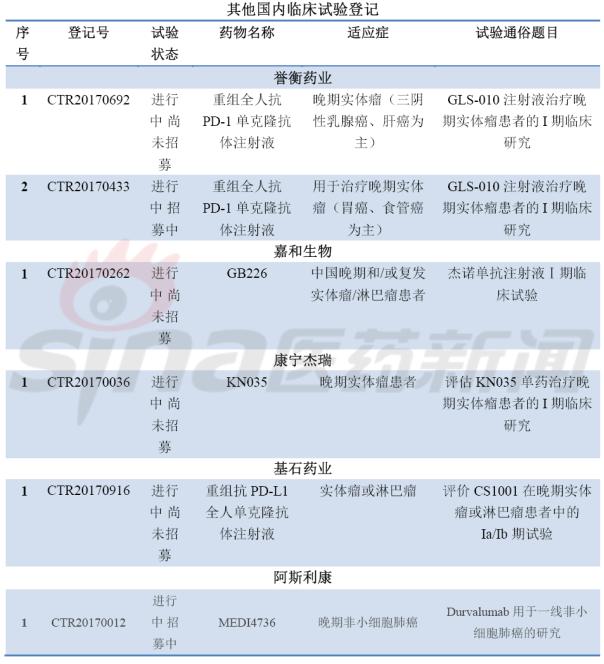
最后,围观国内临床试验备案情况,竞争激烈,临床开发患者招募基本都会遇到问题,要么是进行中尚未招募或进行招募中,很少能够招募完成。甚至外企的临床患者招募都没满,对于患者筛选严格是一方面,另一方面是临床设计的适应症发病率较少或非一线疗法。这可急坏了大药厂啊。肿瘤免疫疗法冰点已来临?

作者:科比crossover
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录





#PD-L1#
74
#招募#
68