年终盘点:2017年肿瘤领域重磅级亮点研究成果
2017-12-18 MedSci MedSci原创
时间总是匆匆,忽然之间就来到了2017年的尾巴。那么在这一年中,我们的科研人员在肿瘤研究和治疗这场攀登中都取得了哪些可圈可点的佳绩?就此,小编筛选出了部分代表性研究加以盘点。当然优秀的研究、优秀的论文是那么多,由于时间有限在此就不一一详述,就请各位看官多多谅解吧。 【1】 FDA: 重磅中的重磅,两款CAR-T疗法获准上市 2017年8月30日,美国F
时间总是匆匆,忽然之间就来到了2017年的尾巴。那么在这一年中,我们的科研人员在肿瘤研究和治疗这场攀登中都取得了哪些可圈可点的佳绩?就此,小编筛选出了部分代表性研究加以盘点。当然优秀的研究、优秀的论文是那么多,由于时间有限在此就不一一详述,就请各位看官多多谅解吧。
【1】 FDA: 重磅中的重磅,两款CAR-T疗法获准上市

2017年8月30日,美国FDA正式批准了诺华制药的CAR-T疗法Kymriah上市,用于治疗复发或难治性儿童B细胞急性淋巴细胞白血病。史上首款CAR-T疗法正式诞生。
2017年10月18日,美国FDA正式批准了Kite Pharma的CAR-T疗法Yescarta,用于治疗在接受至少两种其它治疗方案后无响应或复发性的成人大B细胞淋巴瘤患者及特定类型非霍奇金淋巴瘤患者。
而该领域的另一先行者,Juno Therapeutics的CAR-T疗法JCAR017的种种临床试验证明了其治疗血液肿瘤的有效性及安全性。可以预见的是,第三款CAR-T疗法的上市同样指日可待。
【2】 Science:作为“广谱抗癌药”,PD-1抗体大放异彩
doi: 10.1126/science.aan6733
PD-1及PD-L1抗体自2014年经FDA批准以来,一直作为明星领域备受瞩目,截止现在五种已经上市的PD-1及PD-L1抗体已被批准用于11种肿瘤(黑色素瘤、非小细胞肺癌、肾细胞癌、头颈癌、胃癌、肝癌、经典型霍奇金淋巴瘤、结直肠癌、膀胱癌、默克尔细胞癌以MSI-H/dMMR亚型的实体瘤)的治疗。然而,PD-1及PD-L1抗体的能力并不仅仅局限于这11种肿瘤的治疗中,一项Johns Hopkins大学的研究表明,PD-1抗体对12种MMR缺陷型的不同晚期肿瘤具有显著治疗效果。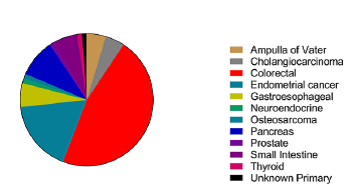
临床试验(样本量为86)结果表明,53%的患者实现了客观缓解,21%的患者实现了完全缓解,77%的患者的病情得到了控制。以上结果表明,PD-1及PD-L1抗体具有成为“广谱抗癌药”的潜能。
【3】 Nature:靶向CD22-CAR-T疗法与靶向CD19-CAR-T疗法相辅相成
doi:10.1038/nm.4441
现已由FDA批准的两款CAR-T疗法均靶向膜蛋白CD19,但是当患者的肿瘤细胞不表达CD19,或低表达CD19以躲避免疫系统时,那么靶向CD19-CAR-T疗法对该类患者就会显示无效。如何克服这一难题?斯坦福大学医学中心与NIC的研究人员发现除了CD19外,CD22同样可以作为靶点。研究者们设计了一种靶向CD22分子的CAR-T疗法,在I期临床实验中,21名B细胞急性淋巴细胞白血病儿童和年轻成人患者在接受了CD22-CAR-T疗法后,73%患者得到了完全缓解,且对该疗法耐受性良好。
【4】 Cell:肿瘤的免疫细胞图谱,让肿瘤免疫治疗更精准
doi.org/10.1016/j.cell
肿瘤细胞毫无节制地生长能力来源于肿瘤细胞与免疫细胞形成的独特微型生态系统。在这种独特微型生态系统中,细胞之间存在着不寻常的联系。研究人员通过绘制免疫细胞图谱(atlases)详细阐述了这种独特生态系统。
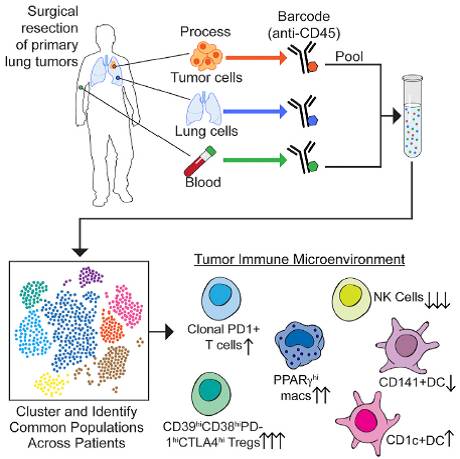
Sloan Kettering Institute的研究人员借助免疫细胞图谱发现,在肿瘤发生的早期,免疫细胞已处于不正常状态,而免疫治疗通常在肿瘤发展的中末期介入,这一研究提示,免疫治疗的介入时期非常重要。研究人员可以通过免疫细胞图谱来精准决策肿瘤免疫治疗的介入时期。
【5】 Oncotarget:正常乳腺组织与乳腺癌组织中菌群的显著差异
doi: 10.18632/oncotarget.21490
一项在克利夫兰医学中心(Cleveland Clinic Lerner College of Medicine)完成的研究表明,女性乳腺癌组织与正常乳腺组织中菌群存在显著不同,研究人员通过比对正常和癌变的乳腺组织中的菌群差异,发现乳腺癌组织富集了甲基杆菌属(Methylobacterium)。除了乳腺组织外,研究人员还对78名乳腺癌患者的口腔以及尿液等部位的菌群进行了分析,发现乳腺癌患者的尿液中革兰氏阳性菌的含量也有所增加(包括葡萄球菌,放线菌等)。因此研究人员创新性地提出,将这些特定细菌作为生物标记物来快速准确地诊断乳腺癌的发生。
然而研究人员的眼光并不仅仅局限于诊断,他们进一步提出“抗癌细菌”这一概念,即在乳腺癌早期使用微生物组学进行预测及诊断,而后应用具有拮抗甲基杆菌属作用的细菌,并借助纳米技术来防治乳腺癌。这项研究有望将乳腺癌的“细菌治疗”向前推进一步。
【6】 Science:肿瘤细胞能食“毒”而生,加速肿瘤细胞增殖
doi: 10.1126/science.aam9305
氨分子作为一种毒性代谢产物,正常情况下经由血液运输到肝脏,经肝脏代谢后进入泌尿系统排出体外。但哈佛医学中心(Harvard Medical School)的研究人员发现,这些氨分子非但对肿瘤细胞没有毒性,反而氨分子的引入加快了多种肿瘤细胞的生长,可以说,肿瘤细胞能够食“毒”而生。研究人员发现乳腺癌细胞能够高效地利用分子氨,将其作为细胞物质的合成基础,合成为谷氨酸及其多种衍生物。
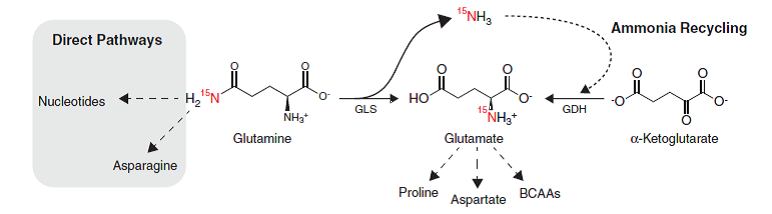
研究人员称,抑制氨分子的回收利用可以作为阻断肿瘤细胞生长的一条新途径。同时,氨分子的生物学功能也需要被重新定义,这能够为研究人员找到阻断肿瘤细胞营养供应来源提供新的思路。
【7】 Science Translational Medicine:靶向FLT3-ITD和BCL-2,或有望根除白血病
doi: 10.1126/scitranslmed.aao1214
急性骨髓性白血病(AML)具有复发易的显著特征,每年造成了大量患者死亡。究其原因,白血病干细胞(LSCs)被认为是AML容易复发的根源,因为这些干细胞能够抵抗化疗药物的杀灭作用,并且即使相当少量的干细胞依然能够增殖并分化成癌细胞。一项由日本理化学研究所研究人员实施的研究表明,同时抑制FLT3-ITD和BCL-2这两个血液细胞中重要的信号通路,可有效地消除AML症状。
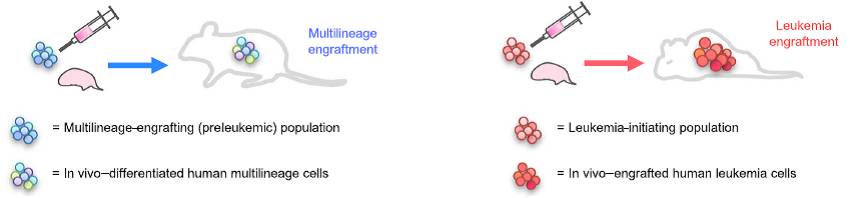
为弄清楚哪些突变与AML的发生是真正相关的,研究人员将不同疾病阶段的AML患者的肿瘤细胞移植到免疫缺陷型的小鼠体内,进而观察这些细胞在骨髓或者脾脏中是否白血病化。利用这种方法发现,FLT3和BCL2基因的突变对于正常骨髓细胞的白血病化起着重要重用,因此靶向这两个信号通路为AML的治疗提供了明确思路。
【8】 Cell:表观遗传药物的联合使用增强了肿瘤免疫疗法的效果
doi.org/10.1016/j.cell.2017.10.022
近日,Johns Hopkins大学的研究人员揭示,去甲基化药物(5-氮杂胞苷)与组蛋白去乙酰化酶抑制剂(HDACis)的联合用药能够抑制原癌基因Myc的作用,进而抑制了肿瘤细胞的增殖。令人意外的是,该种联合用药方案能够促进T细胞向肿瘤细胞的转运,并刺激T细胞对肿瘤细胞进行识别和杀灭。

在动物实验中,5-氮杂胞苷联合givinostat(一种HDACis)治疗非小细胞肺癌患病小鼠时,能够在三个月内取得显著的预防恶性肿瘤发生的效果,与对照组相比,联合用药组同时能够大幅减少良性肺部实体瘤的面积。5-氮杂胞苷联合givinostat与5-氮杂胞苷联合mocetinostat的交替使用也能够显著减少肿瘤细胞转移的发生。
【9】 Science:肺癌细胞居然能远程调控成骨细胞
doi: 10.1126/science.aal5081
在癌症的发生发展过程中,骨骼看似并不会参与其中,毕竟肺癌部位与腿部骨骼的物理距离较远。但最新的一项研究就彻底颠覆了人们现有的认知:肺癌细胞与腿部骨骼中的成骨细胞能够远程相互影响,相互促进。

骨髓是血液细胞制造的主要场所,同时巨噬细胞及中性粒细胞等免疫细胞也于骨髓中生成。研究人员在肺癌模型小鼠中发现,小鼠全身多处骨骼骨密度普遍升高,新骨生成,成骨细胞的数目增多,破骨细胞无显著变化。进一步发现主要是骨钙素(osteocalcin)阳性(OCN+)的成骨细胞发生了变化。清除掉这些OCN+成骨细胞后,肺癌实体的缩小程度高达40%。而OCN+成骨细胞与肺癌细胞是通过何种媒介相互作用的呢?研究人员证明,骨髓中产生的凝集素SiglecF高表达的中性粒细胞在其中起了媒介用。这一发现刷新了肺癌的发生发展机制的认知,为肺癌的治疗提供了新途径。
【10】 Science:如何利用DNA复制叉动力学抑制肿瘤细胞增殖
doi: 10.1126/science.aao3172
细胞,无时无刻不在分裂不在增殖,基因组内DNA的精准复制就是其中的重要一环,DNA的复制速度同时能被细胞所调控以应对细胞代谢的变化,以达到稳态。丹麦哥本哈根大学的研究者揭示了DNA复制叉动力学对细胞代谢变化的响应机制。如果四种核苷酸的产量无法满足DNA复制的需求,那么经活性氧族(ROS)负责传递的化学信号会减慢DNA的复制速率,而核苷酸供应和DNA复制叉动力学之间的通信是由PRDX2介导的。
因为异常的基因组的存在,DNA的复制在肿瘤细胞中是很缓慢的,因而肿瘤细胞的DNA复制需要更多时间去克服种种障碍。研究人员假设,如果将肿瘤细胞DNA缓慢复制基因组的能力抑制后,DNA复制的种种问题无法解决,便无法顺利完成复制,肿瘤细胞便会死亡。该项研究又为肿瘤的治疗提供了新机制。
结语:
2017年,可以说是肿瘤免疫治疗的丰收之年,当然肿瘤研究的其他领域也在大放异彩。相信人们在抗击肿瘤的攀登中,离胜利的顶峰会越来越近。
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#研究成果#
47
#肿瘤领域#
78
肿瘤领域研究成果.
71
2017年肿瘤领域的研究成果.
85
#年终盘点#
56