中科院北京纳米能源所李琳琳团队《自然·通讯》:晶格膨胀提高纳米酶活性和电响应性促进癌症治疗
2024-09-21 BioMed科技 BioMed科技
团队发现晶格间距增大能够提高 Ru 纳米酶的多种类酶活性,并提高其对自供能电刺激的响应性,通过级联催化反应促进癌症治疗,这一规律在Cu等纳米酶上同样适用。
近年来,具有天然蛋白酶催化性质的纳米酶在疾病诊疗中展现出巨大的应用前景。与天然酶相比,纳米酶具有稳定性更高、催化活性可控多样、合成简便、成本低廉等优点。不过,从催化活性上和催化特异性上,纳米酶和天然酶相比仍具有一定的差距。如何调控、提高纳米酶的催化活性仍是目前该领域的难点。对于肿瘤治疗来说,纳米酶能够通过催化肿瘤组织内分子产生毒性物质,如活性氧(ROS),直接或间接导致肿瘤细胞死亡。目前,如何在复杂的肿瘤微环境下调控并提高纳米酶的催化活性从而提高治疗效果仍是一大挑战。

中国科学院北京纳米能源所李琳琳团队前期工作发现,柔性可穿戴/可植入摩擦纳米发电机产生的自供能电刺激能够有效促进纳米酶的活性,提高肿瘤治疗效果(Adv. Mater. 2022, 2109568; Adv. Funct. Mater. 2022, 2209142; Adv. Funct. Mater. 2023, 33, 2305625; Small 2024, 20, 2307087)。最近,团队发现晶格间距增大能够提高 Ru 纳米酶的多种类酶活性,并提高其对自供能电刺激的响应性,通过级联催化反应促进癌症治疗,这一规律在Cu等纳米酶上同样适用。该研究以题为“Lattice expansion in ruthenium nanozymes improves catalytic activity and electro-responsiveness for boosting cancer therapy”的论文发表在《Nature Communications》上。文章的第一作者是中国科学院北京纳米能源与系统研究所的博士生钟颂婧,通讯作者为李琳琳研究员。
该工作通过控制热解温度调控氮碳骨架上Ru 纳米晶体的晶格间距,发现Ru晶格膨胀能够提高其催化产生 ROS、O2 和清除谷胱甘肽(GSH)的活性,还能够提高其对自供能电场的响应性。这意味着内在晶格膨胀和外部电刺激结合可以协同增强催化效果。在自供能电刺激下,晶格膨胀率为 5.99% 的 Ru 纳米酶 (Ru1000)的催化性能和癌症治疗最佳。实验数据和理论计算揭示了晶格膨胀和电刺激均能够调节Ru 的 d 带中心能量,改变底物和中间态吸附能,从而加速催化反应进行。
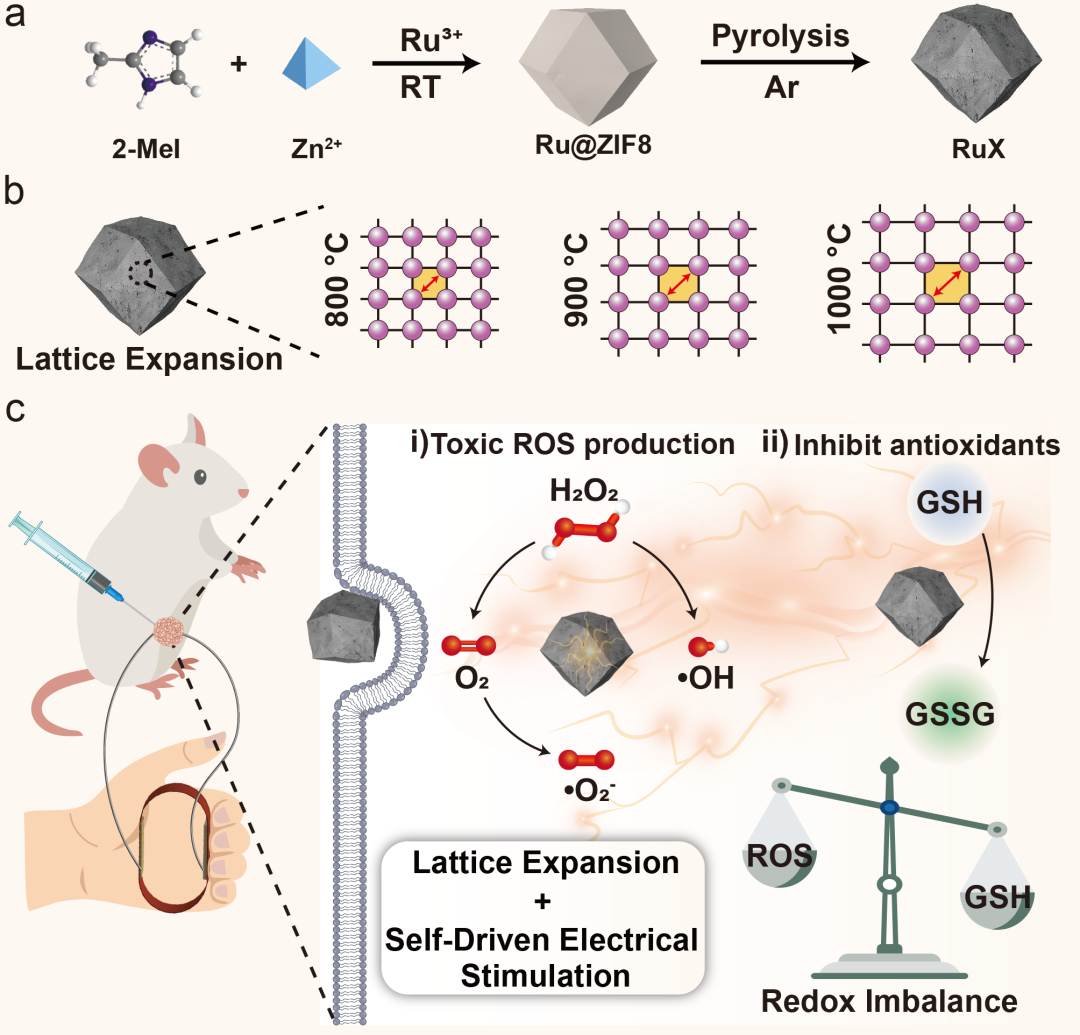
图一. Ru纳米酶合成过程、温度诱导晶格膨胀及肿瘤治疗的示意图.
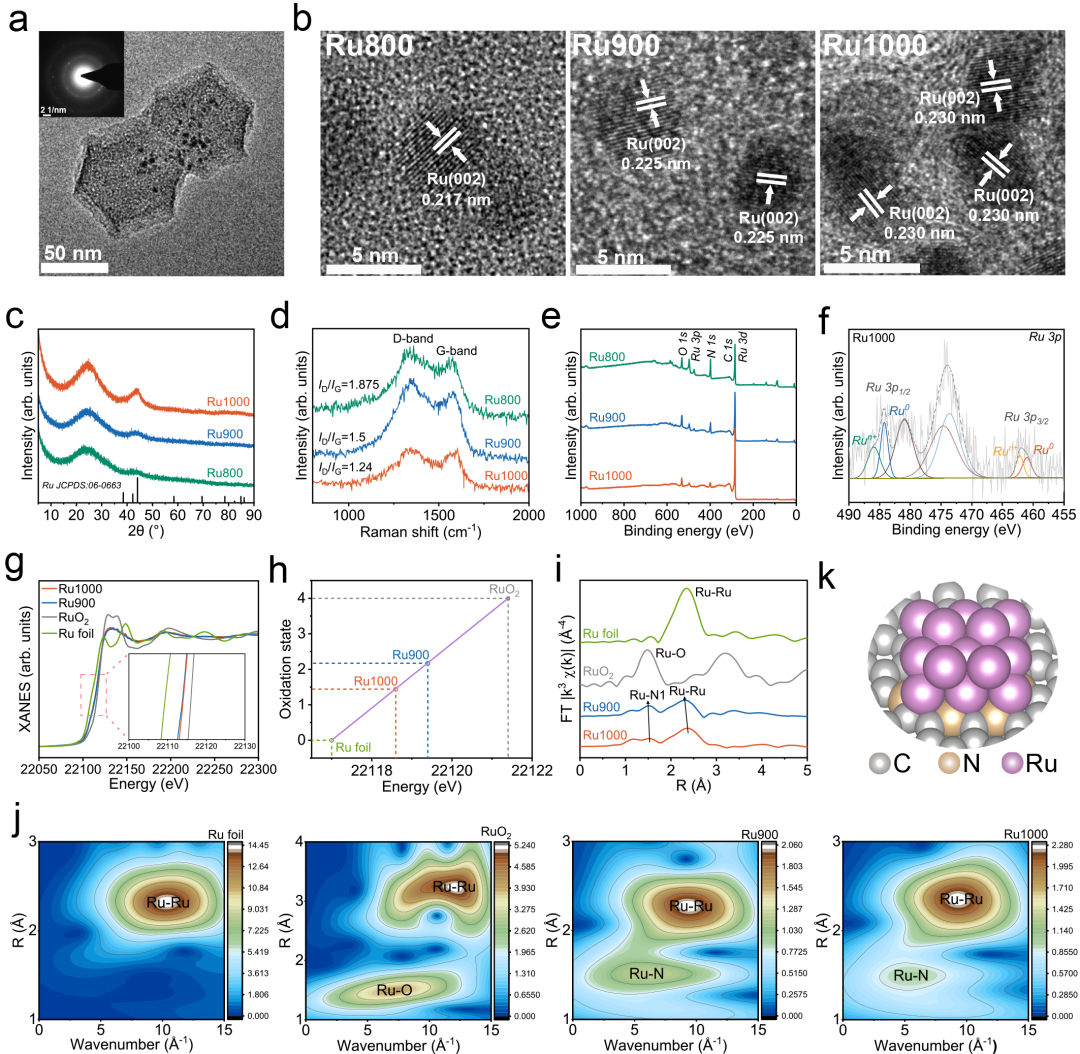
图二. Ru纳米酶的结构表征.
从高分辨率透射电子显微镜 (HRTEM) 图像可以看出,随着热解温度升高,Ru 纳米晶体的晶格间距逐渐均匀扩大,800摄氏度为 0.217 nm (Ru800),900摄氏度为 0.225 nm(Ru900),1000摄氏度为 0.230 nm(Ru1000)。同步辐射 X 射线吸收近边结构 (XANES) 光谱和扩展 X 射线吸收精细结构 (EXAFS) 结果发现,与 Ru900 相比,Ru1000 中Ru-Ru 键长更长,说明Ru晶格膨胀导致 Ru-Ru 键长增加,从而增加了 Ru-Ru键的不饱和度。
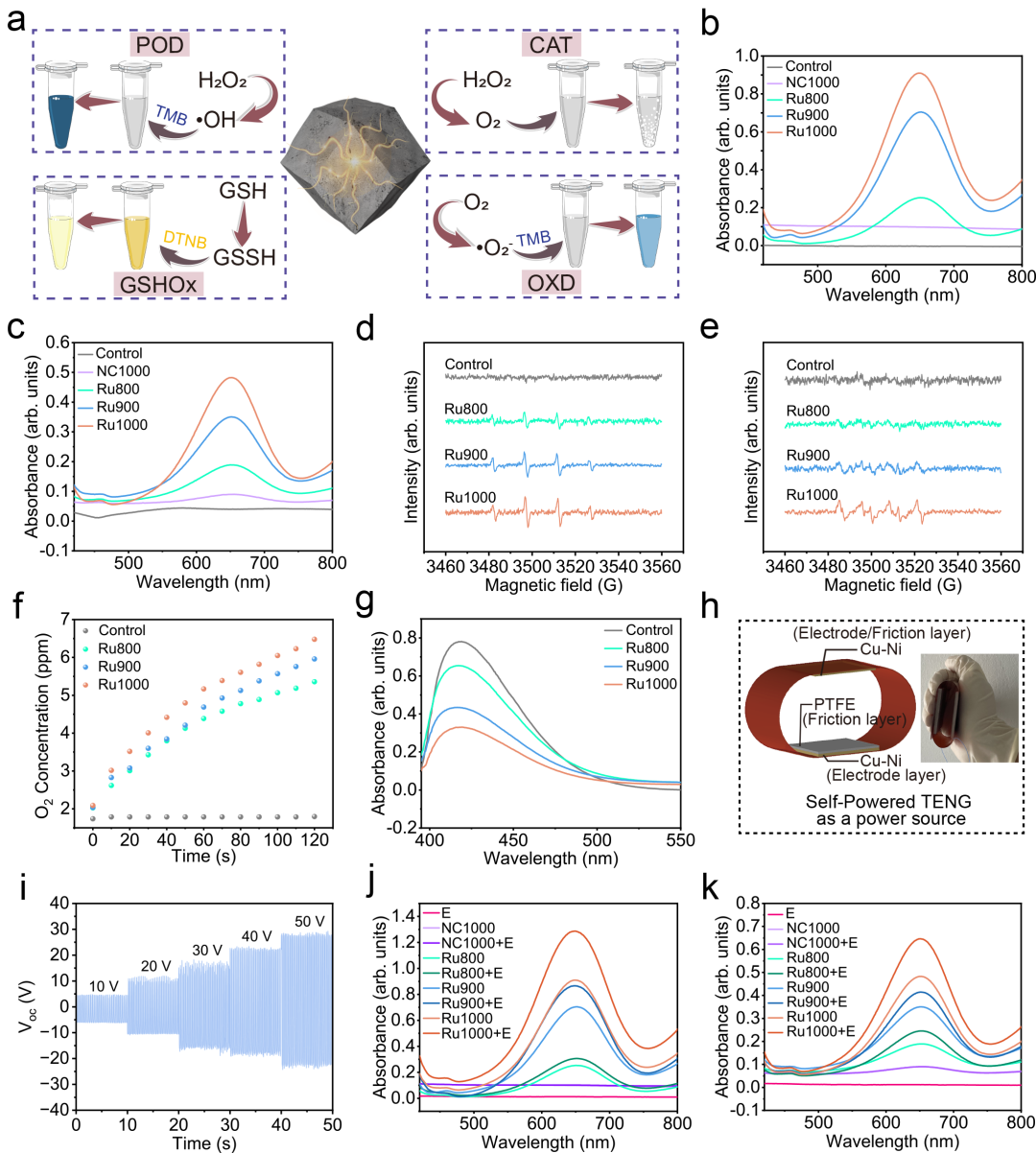
图三. RuX 的催化性能和电响应性.
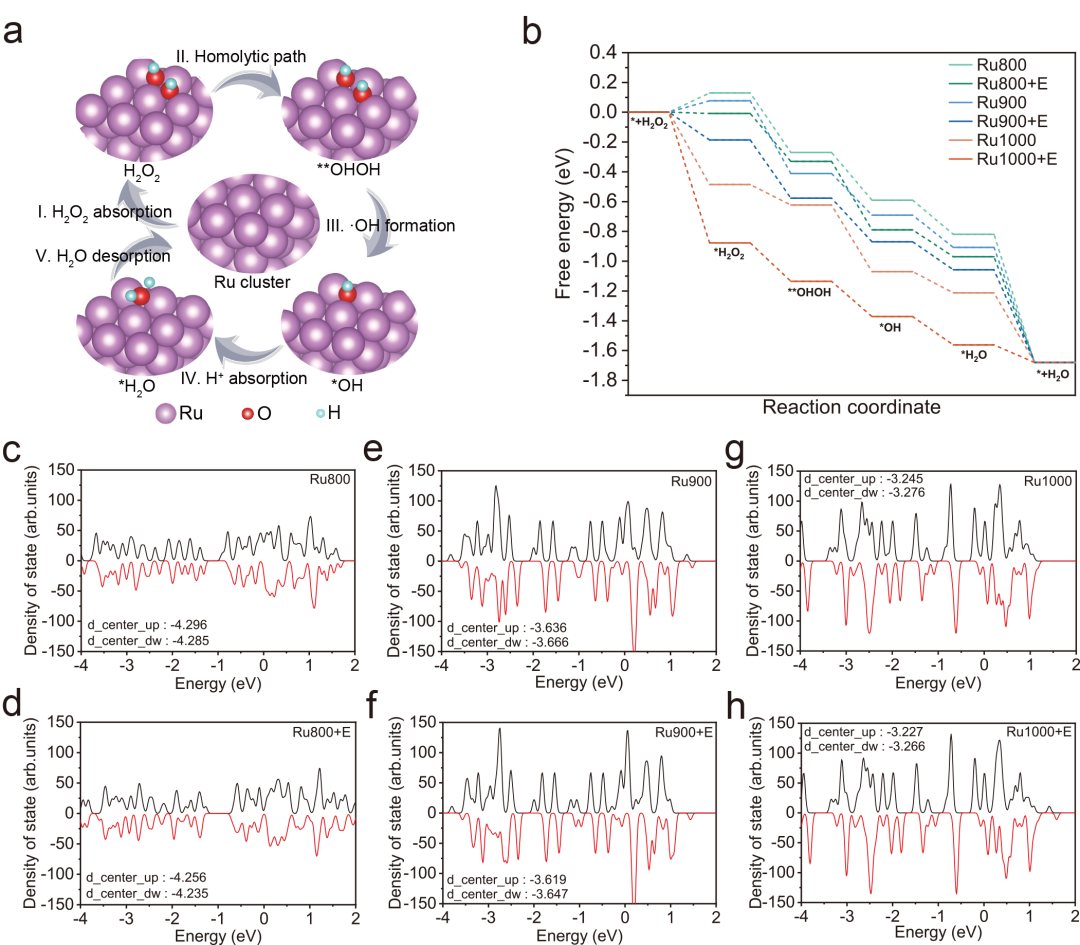
图四. DFT计算验证晶格扩展和电刺激对 RuX 的类POD 活性的促进作用.
对不同晶格间距的Ru纳米酶的催化活性研究发现,晶格间距最大的Ru1000的类过氧化物酶(POD)、氧化酶(OXD)、过氧化氢酶(CAT)和谷胱甘肽氧化酶(GSHOx)四种类酶活性均最佳。此外,在摩擦纳米发电机(TENG)提供的自供能电刺激下Ru纳米酶的催化活性均有所提高,但晶格间距最大的Ru1000提升最为显著。动力学结果初步推测,晶格间距增加促进催化是通过增强活性位点对底物的亲和力来实现的。DFT计算发现,对于Ru800和Ru900来说,由于晶格密度和电子密度较高,H2O2的吸附是限速步骤。而H2O2在Ru1000上的吸附从热力学上是自发的,不需要额外的能量。施加电场后,Ru800、Ru900和Ru1000表面的吸附能均降低,d带中心向费米能级移动。也就是说,晶格膨胀和电刺激都促使Ru电子密度降低,有利于吸附H2O2分子,促进催化。
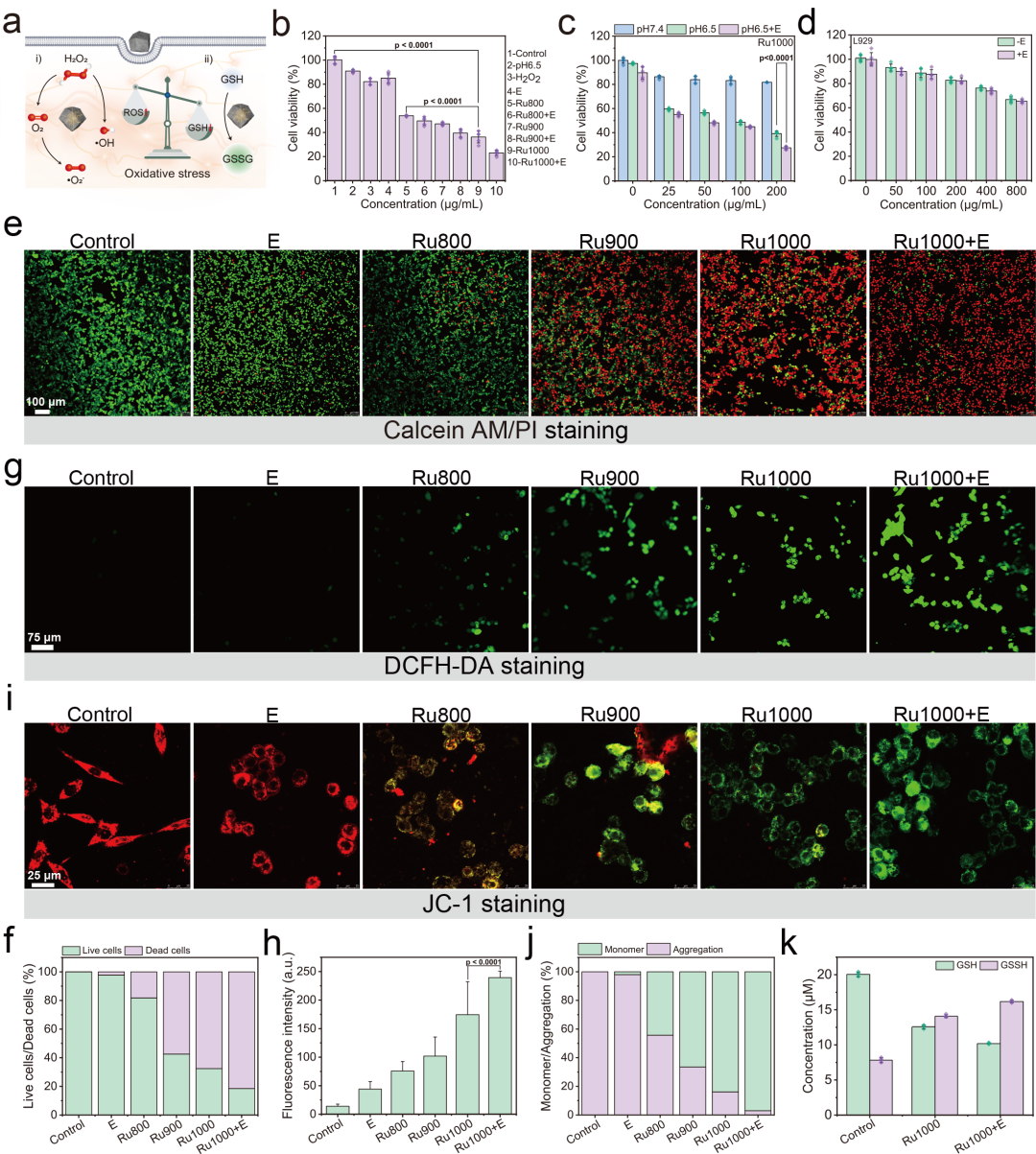
图五. 自驱动电刺激下RuX的体外抗肿瘤作用.
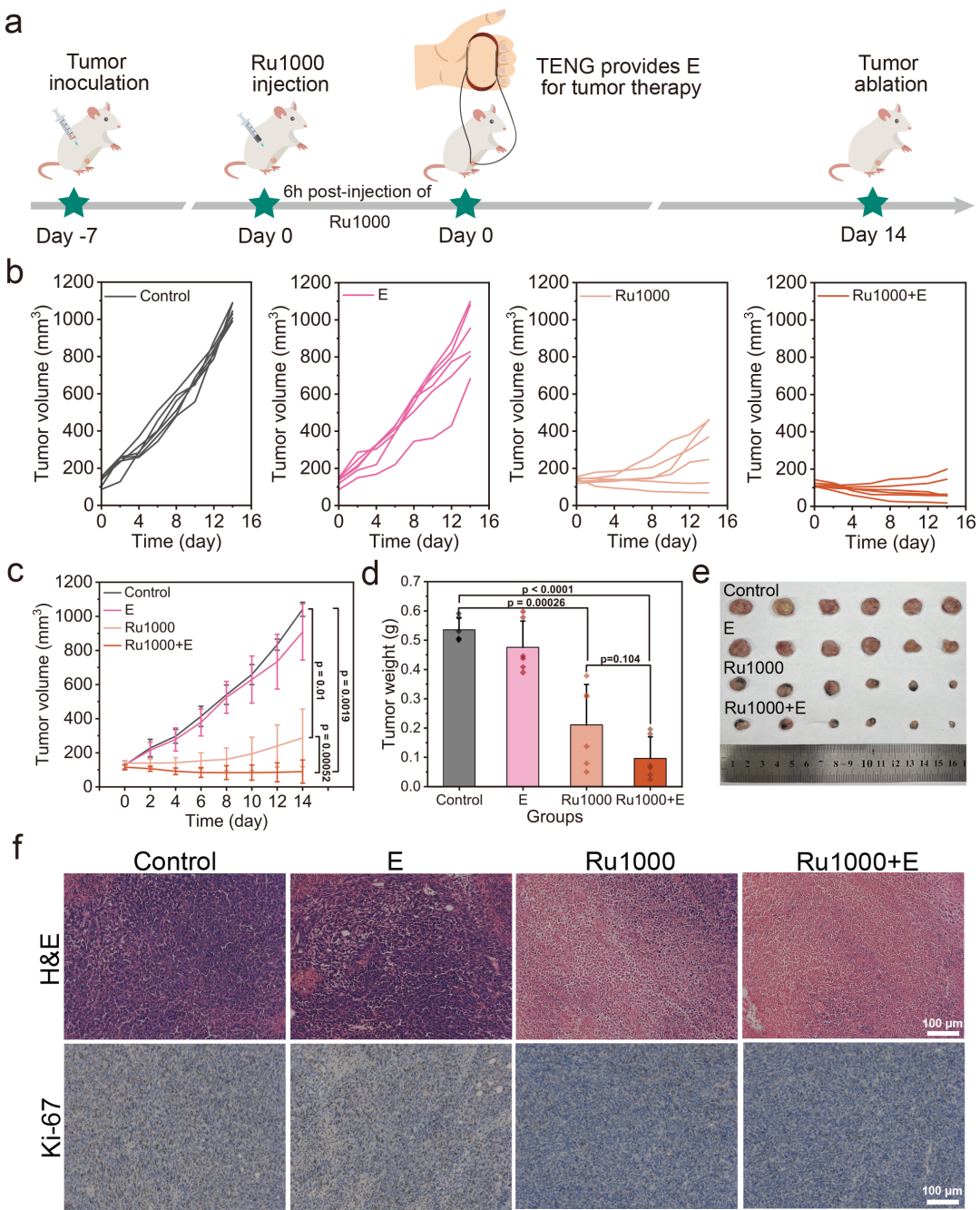
图六. Ru1000的体内抗肿瘤作用.
细胞和动物实验中,Ru纳米酶在体内外均具有良好的生物相容性。Ru1000作用于乳腺癌细胞4T1后,细胞ROS水平提高,GSH/GSSG降低,细胞线粒体损伤,细胞死亡。自供能电刺激进一步提高了肿瘤细胞杀伤和肿瘤抑制(图五、六)。
总之,该工作发现晶格膨胀和外部电刺激均显著增强Ru纳米酶的催化活性,促进癌细胞的氧化损伤和死亡。除了Ru纳米酶,具有类似结构的Cu、Pt等纳米酶也遵循同样的规律。这一规律发现和调控策略为纳米酶的设计提供了新思路。
原文链接:
https://www.nature.com/articles/s41467-024-52277-7
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#癌症治疗# #纳米酶# #晶格膨胀#
21