Cell Res:高福院士揭示PD-L1靶向性肿瘤治疗抗体的作用机制
2016-09-03 佚名 生物探索
近年来,免疫治疗在肿瘤治疗领域取得了一系列重大突破,以PD-1/PD-L1“免疫检查点”抗体阻断疗法为代表的免疫治疗在治疗黑色素瘤、非小细胞肺癌等实体瘤的临床应用中获得了重大成功,显著延长了肿瘤患者的生存期,提高了病人的生活质量,多个抗体药物已经获得美国FDA批准上市或处于多项III期临床试验阶段,然而这些抗体药物的作用机制目前尚不完全清楚。Avelumab是德国Merck公司和美国辉瑞公司联合开
近年来,免疫治疗在肿瘤治疗领域取得了一系列重大突破,以PD-1/PD-L1“免疫检查点”抗体阻断疗法为代表的免疫治疗在治疗黑色素瘤、非小细胞肺癌等实体瘤的临床应用中获得了重大成功,显著延长了肿瘤患者的生存期,提高了病人的生活质量,多个抗体药物已经获得美国FDA批准上市或处于多项III期临床试验阶段,然而这些抗体药物的作用机制目前尚不完全清楚。
Avelumab是德国Merck公司和美国辉瑞公司联合开发的PD-L1靶向抗体药物,能够通过特异性阻断PD-1/PD-L1的相互作用打破肿瘤免疫耐受,恢复肿瘤特异性T细胞对肿瘤细胞的杀伤功能,进而实现肿瘤的清除,目前该抗体正在进行针对非小细胞肺癌、卵巢癌、胃癌及肾细胞癌等的多项III期临床试验。中国科学院微生物研究所高福团队通过结构免疫学平台,成功解析了avelumab抗体与人PD-L1分子的复合物结构,阐明了PD-L1靶向性肿瘤治疗抗体的作用机制。研究发现,avelumab抗体主要通过其重链的三个CDR loop与PD-L1相互作用,而轻链的CDR1和CDR3 loop则贡献了部分相互作用。PD-L1主要通过其C,C’,F和G 折叠片及CC’ loop与avelumab相互作用,其中CC’ loop同时与avelumab的轻链CDR3和重链CDR3相互作用并有多个氢键参与。
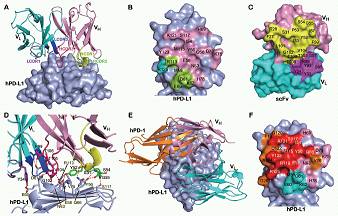
avelumab与PD-1竞争结合PD-L1的结构基础
通过对avelumab抗体与PD-1竞争结合PD-L1机制的分析,发现avelumab主要通过其重链的CDR2与PD-L1的F和G 折叠片结合来竞争PD-1与PD-L1的相互作用,其在PD-L1上的结合区域与PD-1与PD-L1相互作用区域部分重叠。研究还表明,avelumab与PD-L1的亲和力(Kd)为47.2 pM,远高于PD-1与PD-L1相互作用亲和力(0.77-8.2 μM)。因此,高亲和力的avelumab通过其重链CDR2结合PD-L1的F和G折叠片后能够阻止PD-1结合PD-L1,进而阻断PD-1/PD-L1的相互作用。
该项研究成果近期发表在《细胞研究》(Cell Research)杂志上,对设计和改造PD-L1靶向性抗体药物或小分子药物具有重要的指导意义。高福团队在结构免疫学领域深耕多年,在CD8/pMHC (Nature,1997,封面文章等)及TCR/pMHC相互作用机制(Immunity,1999a;Immunity,1999b等)等领域取得了重要成果,近年来在不同物种MHC分子进化及抗原呈递规律(多篇J Immunol, J Virol)、OSCAR(PNAS, 2016)、PILR分子(PNAS, 2014)及ILT家族分子(J Biol Chem, 2011; J Mol Biol, 2009等)等重要免疫分子及其配体相互作用的结构和功能方面进行了系统研究。
原始出处
Kefang Liu, Shuguang Tan, Yan Chai, Danqing Chen, Hao Song, Catherine Wei-Hong Zhang, Yi Shi, Jun Liu, Wenjie Tan, Jianxin Lyu, Shan Gao, Jinghua Yan, Jianxun Qi and George F Gao.Structural basis of anti-PD-L1 monoclonal antibody avelumab for tumor therapy.Cell Research.2016
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#CEL#
24
#Cell#
0
很好,不错,以后会多学习
75
希望科研人员继续努力争取早日成功!早日让患者们用上药!
53
学习了好
60