浙大金建平/裘云庆团队《自然·通讯》:揭示肝癌治疗新靶点——靶向Hippo信号通路的新型调控因子泛素连接酶RNF214
2024-06-20 BioMed科技 BioMed科技
该研究证明了一个鲜有研究的泛素连接酶RNF214是肝癌的原癌蛋白,通过上调YAP-TEAD复合体的转录活性,促进肝癌的发生发展。
原发性肝癌是全球发病率第六的恶性肿瘤,也是癌症相关死亡的第三大原因,其5年生存率仅为18%。在中国,2020年肝癌新发病人数为41万人,死亡人数高达39万人,是严重危害我国国民健康的第二大癌症。肝癌的发病率和死亡率相近,表明肝癌预后极差,患者从现有的治疗手段中获益不佳。因此,寻找治疗肝癌的新靶点及新疗法对提高肝癌患者的总生存率及生存时间尤为重要。泛素化修饰是真核生物蛋白质翻译后修饰的主要过程之一。泛素化是一个特异性过程,其特异性主要由泛素连接酶直接或间接识别底物蛋白所决定。越来越多的研究发现泛素连接酶是肝癌的原癌蛋白,并能作为肝癌的治疗靶点之一,例如MDM2(p53的泛素连接酶)。
2024年6月11日,浙江大学生命科学研究院金建平课题组和浙江大学附属第一医院裘云庆课题组联合在Nature Communications上发表题为“The RNF214-TEAD-YAP signaling axis promotes hepatocellular carcinoma progression via TEAD ubiquitylation”的研究论文。该研究证明了一个鲜有研究的泛素连接酶RNF214是肝癌的原癌蛋白,通过上调YAP-TEAD复合体的转录活性,促进肝癌的发生发展。

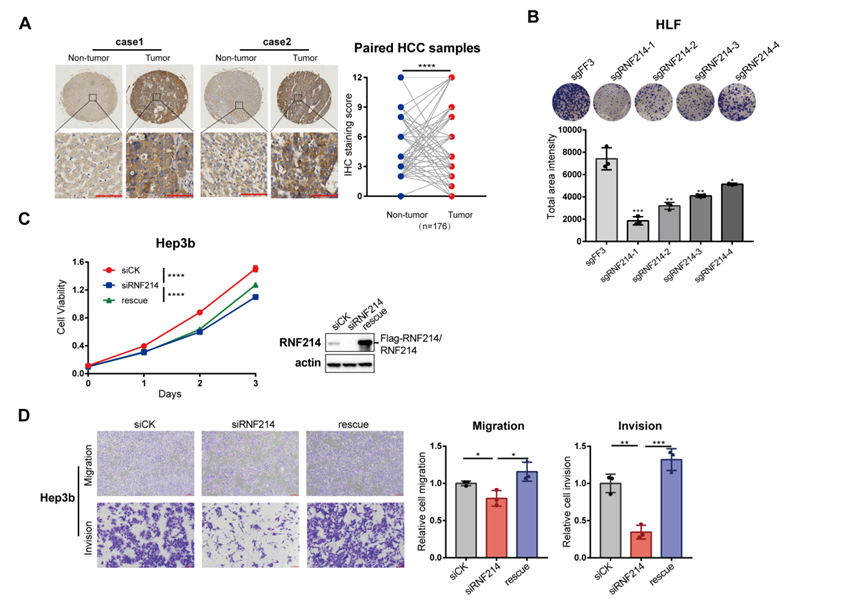
首先,通过对公共数据库的生物信息学分析及175例配对肝癌样本的免疫组化分析,研究团队发现RNF214在肝癌组织中高表达,且与患者不良预后显著相关。在肝癌细胞系中敲低或敲除RNF214,可显著抑制肿瘤细胞增殖、克隆形成、迁徙和侵袭能力。
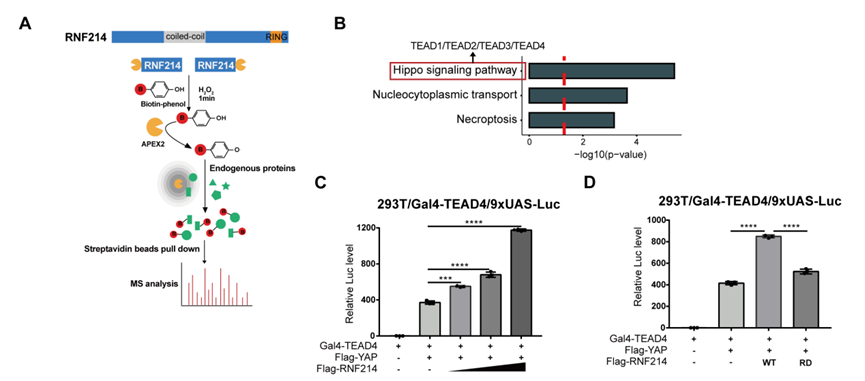
其次,通过APEX2介导的临近标记技术,并结合质谱分析,研究人员发现Hippo信号通路最主要的转录因子TEAD1-4是RNF214潜在的相互作用蛋白;并进一步通过免疫共沉淀实验及体外GST pulldown实验,验证了RNF214与TEAD1-4均存在相互作用。并且,RNF214通过其泛素连接酶活性调控Hippo信号通路的转录活性。通过多种生化实验,研究人员验证了TEADs转录因子是RNF214的底物蛋白;TEAD2羧基端YAP互作结构域的K345位点为RNF214介导的泛素化修饰位点,其泛素化修饰能增强YAP和TEADs之间的相互作用,并促进YAP-TEAD复合体的转录活性。
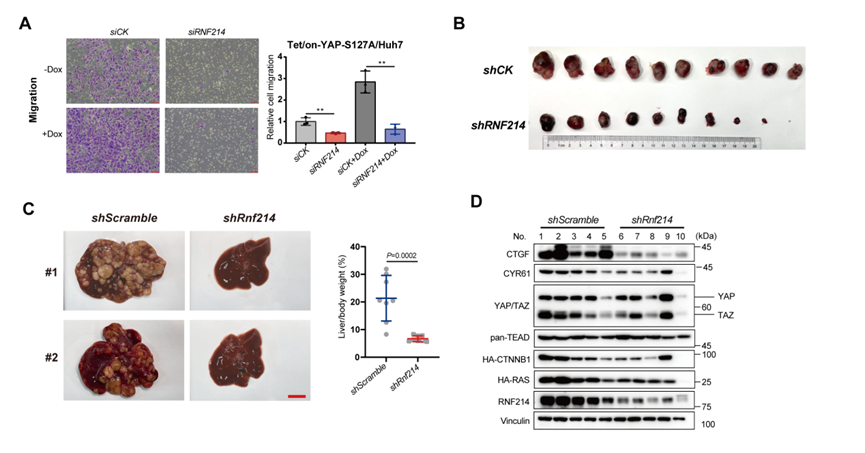
最后,我们在细胞水平验证了RNF214对YAP-TEAD转录复合体致癌作用的重要性;并通过裸鼠皮下成瘤模型和原位肝癌模型验证了抑制RNF214可以显著抑制肝癌的发生发展。
该研究证明了泛素连接酶RNF214在肝癌发生发展中的重要肿瘤学功能,为解析Hippo信号通路在肝癌中的功能研究提供了一个新的视角;本研究表明抑制RNF214泛素连接酶活性可以大大抑制YAP-TEAD转录活性,从而阻止肝癌的发生发展,有望为研发肝癌治疗药物提供新的思路。
金建平实验室博士后林梦佳为本文的第一作者(林梦佳原为金建平实验室和裘云庆实验室的联合培养直博生),金建平教授和裘云庆教授为共同通讯作者,参与本研究的还有郑小恽、严嘉宁、黄飞、陈祎霖、丁冉、万津凯、张磊、汪辰靓、潘金昌、曹晓磊、傅恺怡以及浙一临床药学部楼燕主任。该工作得到了浙江大学生命科学研究院冯新华教授、赵斌教授、姬峻芳教授、沈立教授、复旦大学蓝斐教授、浙江省人民医院病理科何向蕾老师等合作实验室的大力支持,并得到了国家自然科学基金及科技部重大研发项目等的资助。
原文链接:
https://www.nature.com/articles/s41467-024-49045-y
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#肝癌# #RNF214#
5