Microba开始进行炎症性肠病(IBD)治疗的I期临床试验
2023-06-29 网络 网络
首批受试者已经在MAP 315 I期临床试验中成功给药,MAP 315是Microba在炎症性肠病(IBD)方面的主要治疗项目
Microba Life Sciences Limited (ASX: MAP)(以下简称“Microba”或“公司”)今天宣布,首批受试者已在MAP 315(Microba在炎症性肠病(IBD)领域的治疗项目)的I期临床试验中成功完成给药。这一里程碑将Microba的候选药物MAP 315引入临床开发阶段,作为溃疡性结肠炎患者的新潜在治疗方案。
Microba的治疗副总裁Trent Munro教授表示 : “Microba现已发展成为一家临床阶段药物研发公司。我对我们的团队,以及我们在以下方面所做的工作深感自豪:将新型微生物组药物从人类数据引导研发阶段,一直推进到如今已在人类临床试验中给予首剂的口服药物产品。我们在微生物组药物研发领域处于独特的前沿地位,也热切期待MAP 315作为炎症性肠病患者的新治疗方法在未来充分发挥潜在影响。”
该I期临床试验是一项随机、双盲、安慰剂对照研究,旨在通过32名健康成人对MAP 315的安全性、耐受性和药代动力学进行评估。该试验将由澳大利亚墨尔本的Nucleus Network开展,已获得公司人类研究伦理委员会(HREC)的批准,并与其从FDA新药临床研发审批(IND)前的互动中获得的正式反馈保持一致。
MAP 315 I期临床试验详细信息
这项临床试验的标题为“MAP 315的I期随机、双盲、安慰剂对照研究,用于通过健康成人评估其安全性、耐受性和药代动力学”。该研究将招募两组受试者,每组16人,他们将以3:1的比例随机分配,连续14天(2周)接受MAP 315或其相应的安慰剂。预计试验结果将于2023年12月公布。完整的研究详情也可以在澳大利亚新西兰临床试验登记处(ANZCTR)找到,研究ID为:ACTRN12623000291684。
Microba的新型候选药物MAP 315
通过Microba对其大型专有人类数据库的独特分析,MAP 315被确定为一种先前未被充分了解的新型细菌种群,此类种群在健康人群中普遍存在,但在IBD患者体内却一直缺乏。随后通过体外和体内模型对MAP 315进行的临床前研究表明,MAP 315可促进上皮修复和粘膜愈合,这些生物活性对于持续缓解疾病至关重要,但现有疗法并未充分解决这些问题。
MAP 315是一种活性生物治疗产品(LBP),由冻干细菌组成,包裹在肠溶胶囊中口服给药,目前正在作为一种试验产品开发,用于溃疡性结肠炎(UC)的治疗。Microba与领先的微生物组合同药物制造商Bacthera合作,在其位于欧洲的先进设施中大规模生产符合GMP标准的MAP 315,为MAP 315临床试验供应材料。
炎症性肠病——大量未满足的需求和商业机会
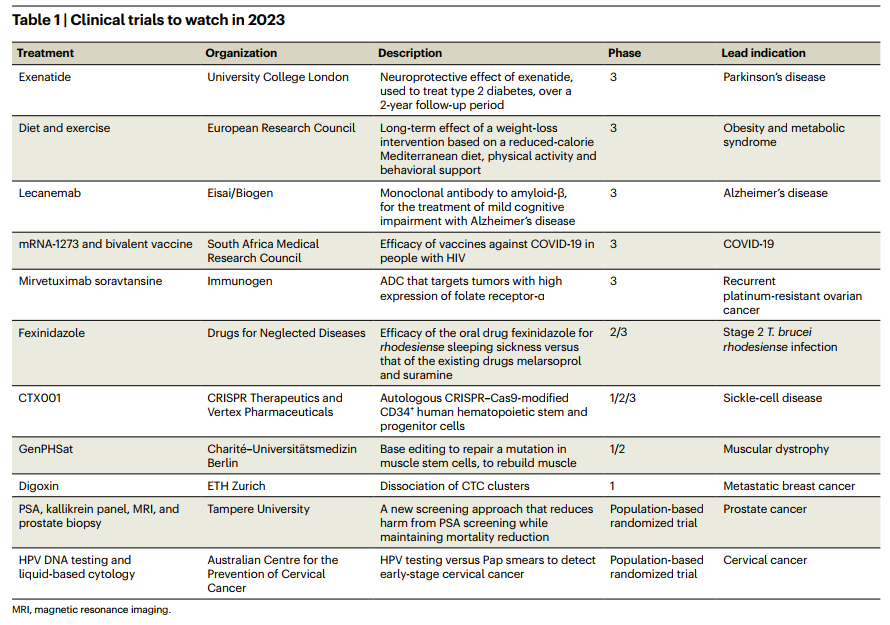
炎症性肠病导致消化道长期发炎,目前全球有超过700万人受此困扰,而且这个数字每年都在增加1。溃疡性结肠炎(UC)是炎症性肠病的两种主要形式之一,它会导致消化道发炎和溃疡(疮),从而引发使人身体虚弱的慢性疾病。目前,患者通常通过抗炎和免疫调节药物治疗以减轻疾病和控制症状,但这往往伴随着明显的副作用。这些现有的治疗方案通常无效,超过50%的患者无法实现持续缓解2,他们经常出现炎症、腹泻、出血和腹痛3,其中多达25%的患者需要住院治疗4。溃疡性结肠炎治疗市场在2020年价值为75亿美元,预计到2030年将增长到108亿美元5。Microba的新型候选药物MAP315为数百万受溃疡性结肠炎困扰的患者改善当前的护理和治疗标准提供了机会。
治疗平台与项目
越来越多的证据表明,肠道微生物组在维持健康和慢性疾病的发展中起着核心作用。目前,基于微生物组的治疗药物已在进行临床开发并首次获得FDA批准,这些新型药物为现有药物无法有效治疗的慢性疾病治疗提供了令人兴奋的新机遇。
Microba凭借其先进的专有宏基因组学技术走在这一领域的前沿,该技术由全球引用率排名前1%的研究人员中的澳大利亚优秀研究人员开发。利用这项技术,Microba建立了一个以人类肠道微生物组为基础的数据驱动型药物研发平台。该平台利用通过公司的微生物组检测服务收集的不断丰富的大规模专有数据存储库,并研发多个强效治疗候选药物来应对慢性疾病。Microba已经建立了涵盖炎症性肠病、免疫肿瘤学和自身免疫性疾病的三个治疗项目,其中首席候选药物MAP 315属于公司的炎症性肠病项目,是首个进入人类临床试验的项目。
关于Microba Life Sciences Limited
Microba Life Sciences是一家致力于改善人类健康的精密微生物组公司。凭借世界领先的人类肠道微生物组测量技术,Microba正在推动重大慢性疾病新型疗法的发现和开发,并在全球范围内向研究人员、临床医生和消费者提供肠道微生物组检测服务。Microba通过与领先组织的合作,正在帮助探索微生物组、健康和疾病之间的新联系,以开发新的健康解决方案。
____________________________
1 https://www.thelancet.com/journals/langas/article/PIIS2468-1253(19)30333-4/fulltext
2 https://www.crohnscolitisfoundation.org/sites/default/files/2019-02/Updated%20IBD%20Factbook.pdf
3 Scribano, M.L. Adverse events of IBD therapies(炎症性肠病疗法的不良事件)。《Inflammatory Bowel Diseases》(2008年)。 https://doi.org/10.1002/ibd.20702。
4Pola, S.等人。Strategies for the care of adults hospitalized for active ulcerative colitis(成人活动性溃疡性结肠炎的住院治疗策略)。《Clinical Gastroenterology and Hepatology》(2012年)。https://doi.org/10.1016/j.cgh.2012.07.006。
5 https://www.nature.com/articles/d41573-021-00194-5、https://www.alliedmarketresearch.com/ulcerative-colitis-market
MAP 315是一种新型活性生物治疗产品,使用Microba的数据驱动型治疗平台研发,用于治疗溃疡性结肠炎。(照片:美国商业资讯)
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言