Cell Metab:王红阳院士团队揭示NAD+代谢调节肿瘤免疫逃逸和增强PD-1/PD-L1治疗敏感性
2021-08-20 和元生物 和元生物
烟酰胺腺嘌呤二核苷酸(NAD
烟酰胺腺嘌呤二核苷酸(NAD+)是能量代谢和信号转导途径的重要中介[1],除了在氧化磷酸化和氧化还原反应中的功能外,NAD+还作为许多酶的底物,并参与许多生物过程,如DNA修复、炎症和蛋白质乙酰化[2]。烟酰胺磷酸核糖基转移酶(NAMPT)是NAD+合成途径的限速酶,NAMPT和NAD+在几种人类恶性肿瘤中经常上调,并在肿瘤的起始、进展和复发中发挥关键作用[3]。然而,NAMPT介导的NAD+代谢在调控肿瘤免疫逃逸中的作用尚不清楚。
近年来,免疫检查点抑制剂在肿瘤免疫治疗方面取得了显著的临床突破。程序性死亡配体1(PD-L1,也称为CD274或B7-H1)在多种癌症中高表达,并通过与活化的T细胞表面的受体PD-1相互作用来调节免疫逃逸,导致T细胞衰竭。PD-1/PD-L1轴抑制剂可显著增强T细胞应答,并在多种晚期癌症中表现出显著的临床应答。
然而,临床试验数据显示,抗PD-1/PD-L1抗体等免疫治疗在实体瘤中的有效率低,仅20%左右。此外,长时间持续性的单一使用免疫检查点抑制剂治疗肿瘤并不能收到预期的疗效,甚至容易引发免疫耐受。因此,寻找行之有效的疗效预测标志和联合治疗是提高肿瘤免疫治疗效果和推进肿瘤精准免疫治疗的重要方法。NAD+代谢与癌症有关。然而,其在免疫检查点调控和免疫逃逸中的作用尚不清楚。
第二军医大学东方肝胆外科医院/国家肝癌科学中心王红阳院士/杨文研究员团队在Cell Metabolism上发表了题为 NAD+ metabolism maintains inducible PD-L1 expression to drive tumor immune evasion 的研究论文,揭示了NAD+代谢通过调节免疫检查点PD-L1的表达,驱动肿瘤免疫逃逸的新机制,并提出了通过补充NAD+前体增强免疫治疗耐受肿瘤对抗PD-1/PD-L1抗体治疗敏感性的新策略[5]。

1 NAD+代谢控制CD8+T细胞依赖性肿瘤抑制作用

图1 NAD+代谢控制CD8+T细胞依赖性肿瘤抑制作用
2 NAD+代谢驱动肿瘤细胞诱导PD-L1表达
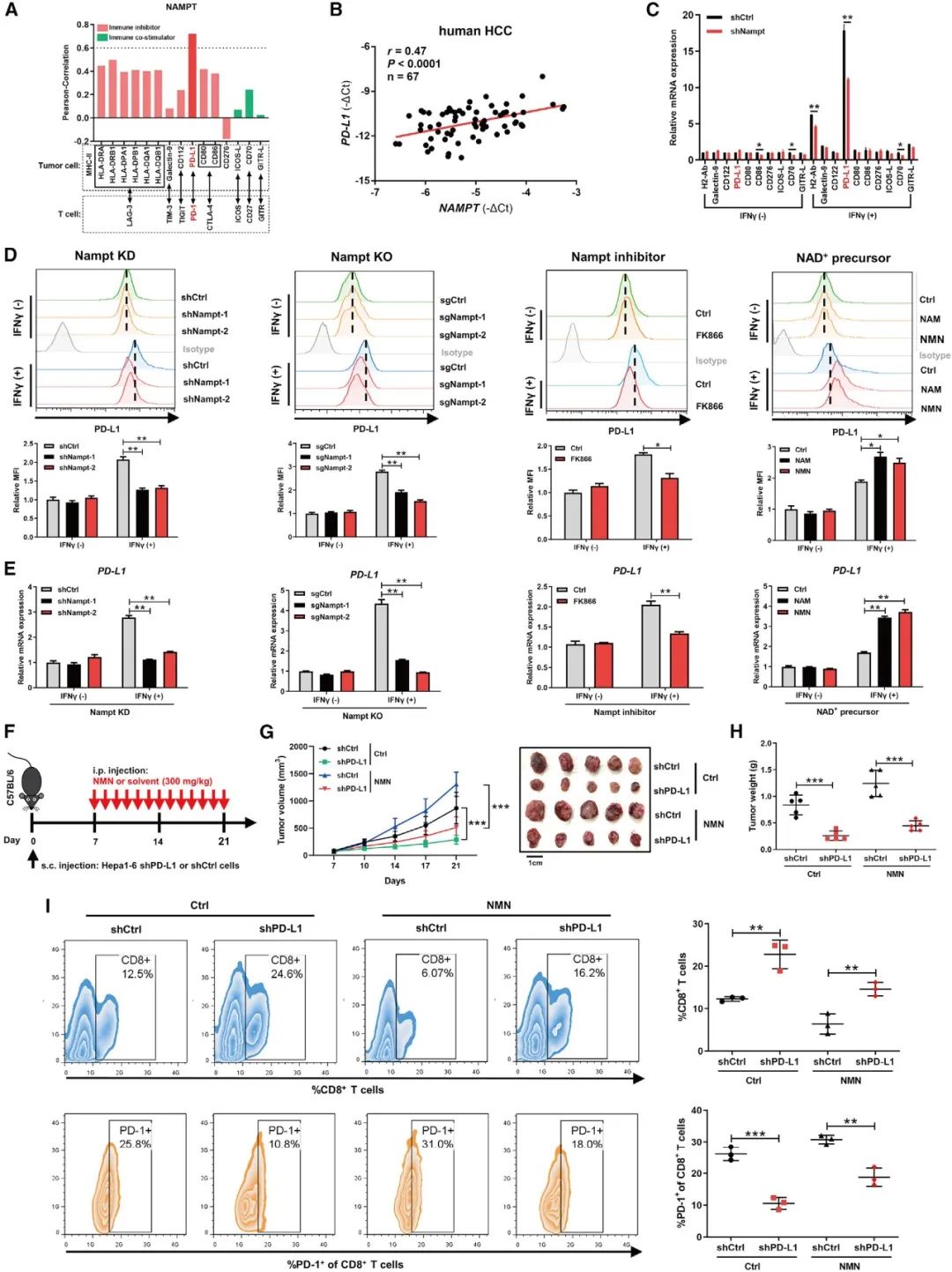
图2 NAD+代谢驱动肿瘤细胞诱导PD-L1表达
3 NAD+代谢通过Stat1依赖的IFNγ信号通路调控PD-L1
基因集富集分析(GSEA)表明,NAMPT和IFNγ信号通路(Jak/Stat pathway)在TCGA介导的肝癌中高度相关。之前研究IFNγ刺激的Jak/Stat/干扰素调节因子-1 (Irf1)信号轴正向介导PD-L1表达,结合WB实验等验证,NAD+代谢调节stat1依赖的IFNγ信号通路在癌症中的PD-L1诱导。

图3 NAD+代谢通过Stat1依赖的IFNγ信号通路调控PD-L1
4 NAD+代谢通过α-KG维持甲基胞嘧啶双加氧酶Tet1的表达和活性
NAD+代谢通过NAD+/NADH氧化还原状态调节线粒体能量生产,通过NAD+依赖的酶活性调节多种生物功能、衰老、疾病和癌症。研究人员通过测序结合质谱分析等实验表明,NAD+代谢通过依赖于α-KG的Tet1调节IFNγ-Stat1-Irf1轴诱导的PD-L1表达。
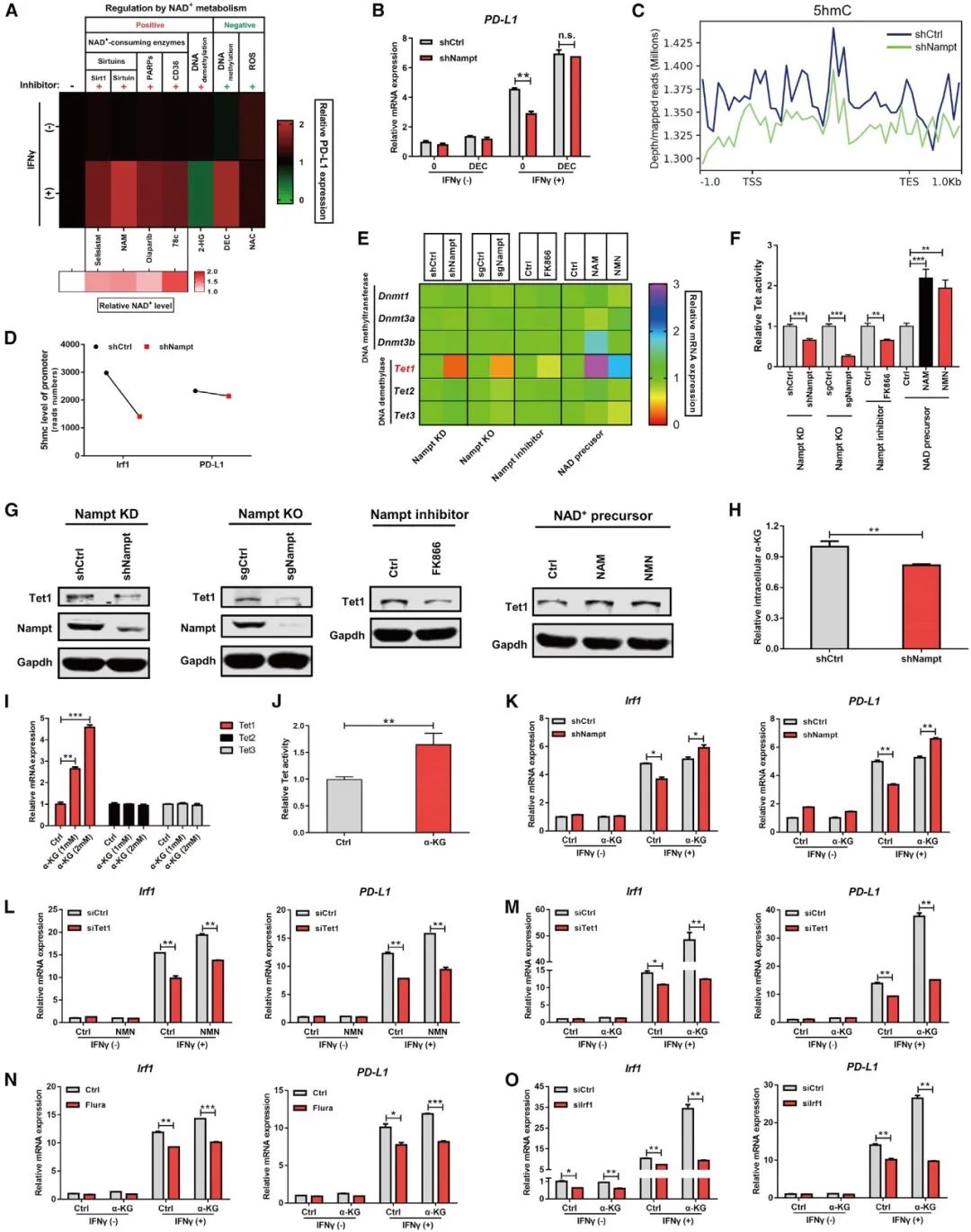
图4 NAD+代谢通过α-KG维持甲基胞嘧啶双加氧酶Tet1的表达和活性
5 IFNγ激活的Stat1招募与Irf1结合的Tet1以调节Irf1去甲基化导致PD-L1表达
研究人员进一步探讨NAD+代谢介导的Tet1如何调控IFNγ信号通路和PD-L1表达,发现,IFNγ激活的Stat1招募与Irf1位点结合的Tet1,促进Irf1去甲基化和转录,诱导下游PD-L1的表达。
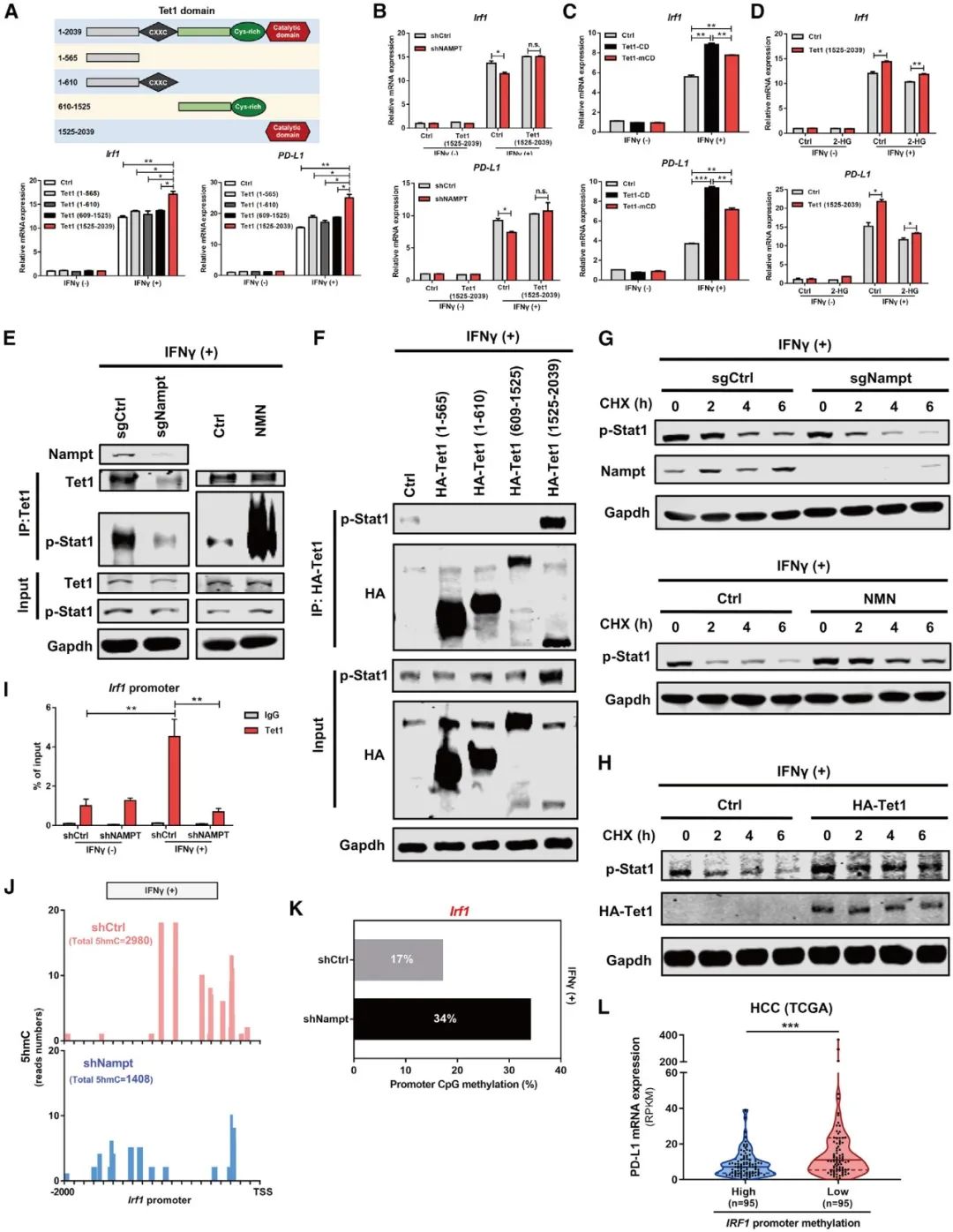
图5 IFNγ激活的Stat1招募与Irf1结合的Tet1以调节Irf1去甲基化导致PD-L1表达
6 NAMPT-TET1-p-STAT1-IRF1-PD-L1轴在人类癌症中激活并预测不良预后
接下来,研究人员检测NAMPT-TET1-p-STAT1-IRF1-PD-L1轴在癌症患者组织中的蛋白表达水平,NAMPT、TET1、p-STAT1、IRF1和PDL1在肝癌中表达明显升高。临床数据分析表明,NAMPT-TET1-p-STAT1-IRF1-PD-L1轴高表达的患者生存率明显较低。
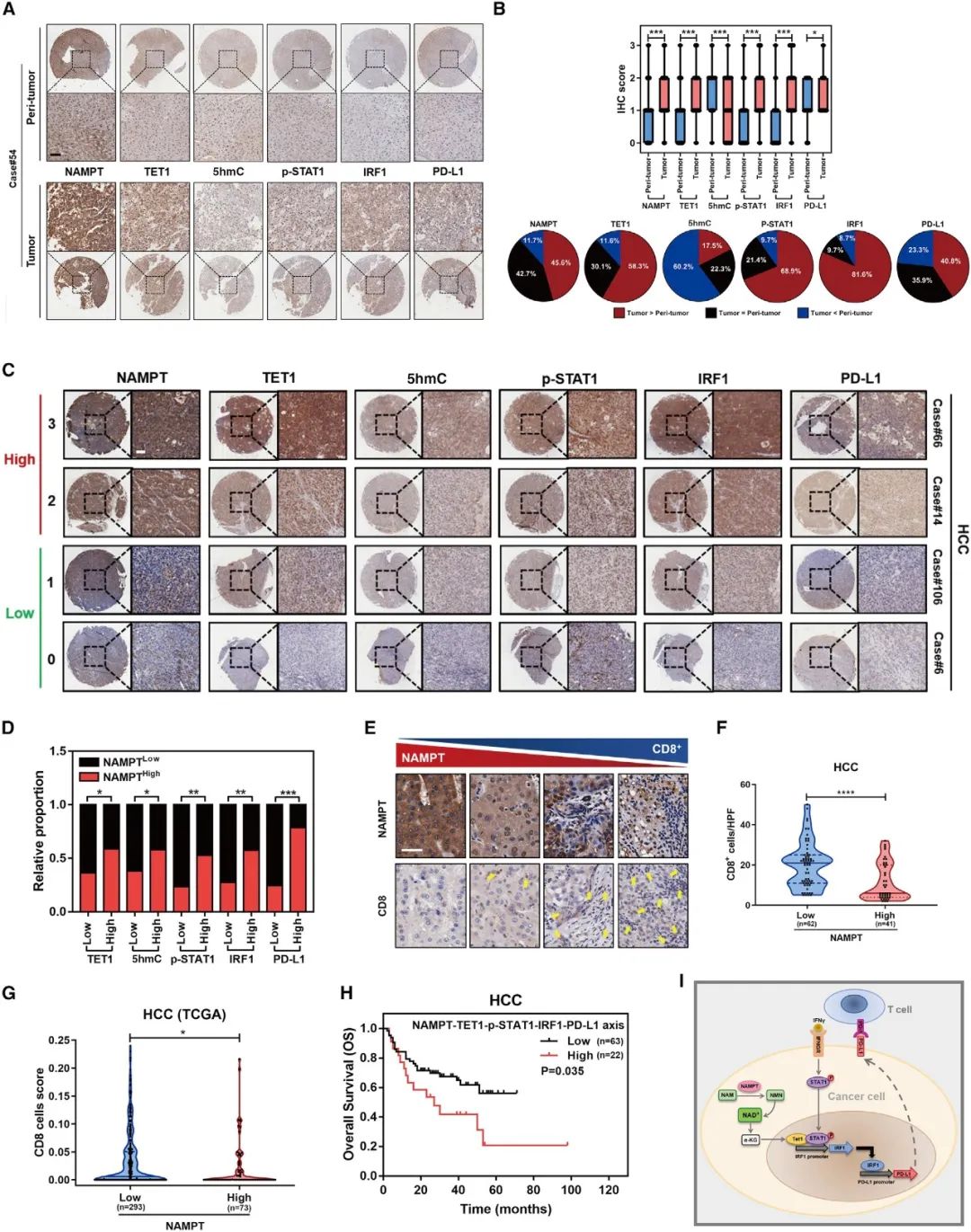
图6 NAMPT-TET1-p-STAT1-IRF1-PD-L1轴在人类癌症中激活并预测不良预后
7 NAMPT预测PD-(L)1检查点阻断和NAD+补充增加抗PD-(L)1的免疫治疗效果
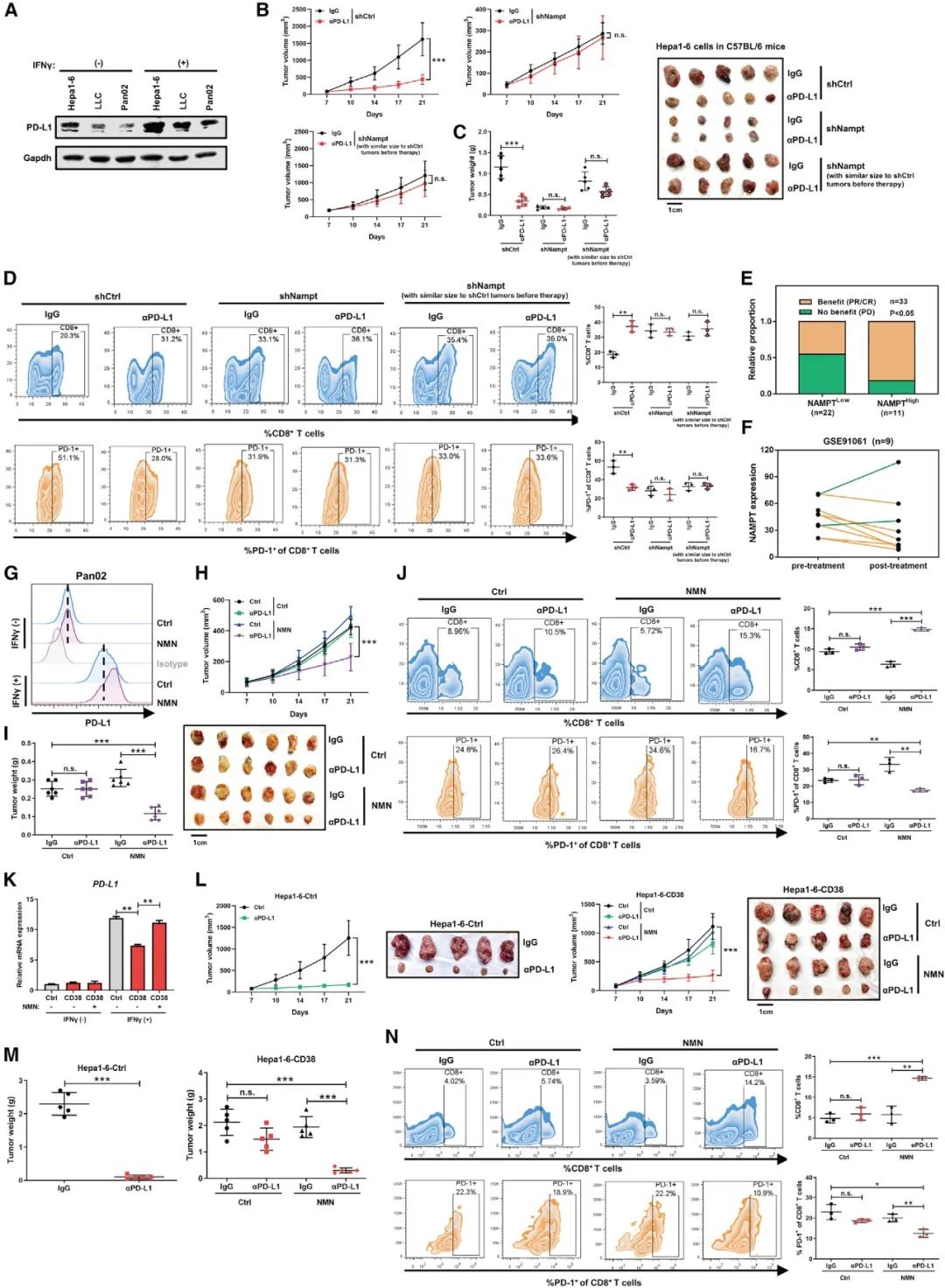
图7 NAMPT预测PD-(L)1检查点阻断和NAD+补充增加抗PD-(L)1的免疫治疗效果
结论:
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#王红阳#
72
#Cell#
68
#CEL#
60
#Meta#
53
#MET#
48