Aging Cell:调节Aβ产生和降解的新途径被发现
2020-11-01 haibei MedSci原创
在体内,没有APP或AICD的小鼠大脑中IDE表达降低,这与人类AD大脑中APP表达水平和IDE表达的显著相关性一致。
目前,全球估计有超过5千万人患有老年痴呆症。老年痴呆症(AD)是一种进行性、不可逆的神经退行性疾病,是老年人最常见的痴呆原因。淀粉样蛋白-β(Aβ)肽在脑组织中过度积累和聚集,导致细胞外衰老斑块的形成,被认为代表了该病以突触丧失和神经元损伤为特征的最初病理过程。
Aβ肽是I型跨膜淀粉样前体蛋白(APP)经β-和γ-分泌酶连续加工的产物,APP是一个保守蛋白家族的成员,包括APP样蛋白1和2(APLP1和APLP2)。除了淀粉样蛋白APP加工途径外,APP可以在主要的α-和γ-分泌酶依赖的非淀粉样蛋白裂解级联中被裂解,排除Aβ肽的生成。

在生理条件下,Aβ的产生和降解之间的紧密平衡是防止病理性Aβ积累的必要条件。最近,研究人员在Aging Cell发文,研究了主要的Aβ降解酶之一的胰岛素降解酶(IDE)是如何被调控的分子机制,以及淀粉样前体蛋白(APP)的处理和Aβ的降解是如何在一个调控循环中被联系起来以实现这种平衡的。
在APP或Presenilin缺失引起的Aβ生成缺失的情况下,IDE介导的Aβ降解减少,伴随着IDE活性、蛋白水平和表达量的降低。在仅表达截短的APP,缺乏APP胞内域(AICD)的细胞中也得到了类似的结果,表明AICD促进IDE的表达。
反过来,APP过度表达介导IDE表达增加,与过度表达C50,代表AICD的截短APP的细胞得到了相似的结果。
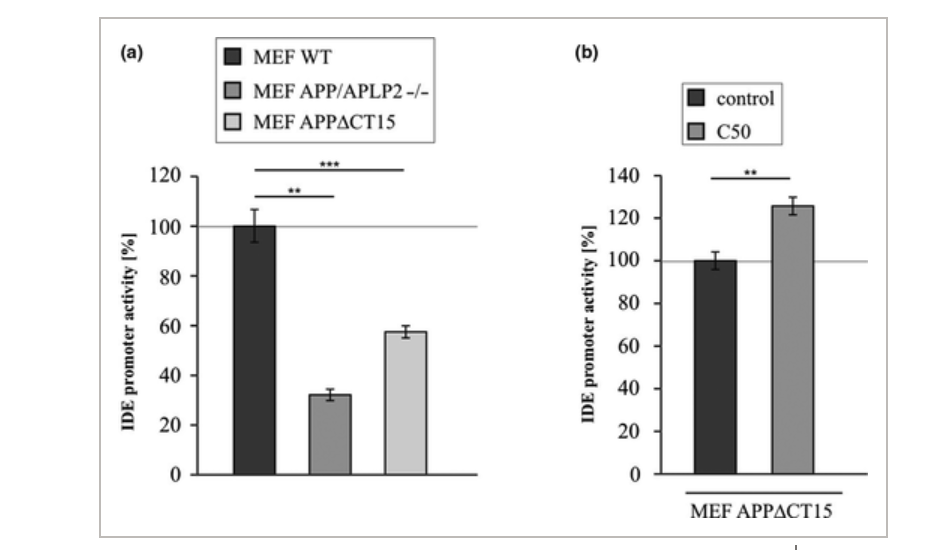
除了这些遗传方法,研究人员还通过AICD肽孵化和γ-分泌酶的药物抑制来调节IDE的表达和启动子活性。这些结果也在利用CRISPR/Cas9 敲除APP和Presenilin的SH-SY5Y细胞中得到证实。
在体内,没有APP或AICD的小鼠大脑中IDE表达降低,这与人类AD大脑中APP表达水平和IDE表达的显著相关性一致。
因此,该研究结果表明,Aβ的产生和Aβ的降解之间形成了紧密的联系,AICD通过IDE促进Aβ的降解,而IDE本身也通过降解AICD限制了自身的产生,形成了一个调节循环。
原始出处:
Anna A. Lauer et al. Regulatory feedback cycle of the insulin‐degrading enzyme and the amyloid precursor protein intracellular domain: Implications for Alzheimer’s disease. Aging Cell (2020). DOI: https://doi.org/10.1111/acel.13264
作者:haibei
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#CEL#
73
#Cell#
89
#新途径#
82
学习了
103
好
126