CELL:TREM2可增强肿瘤抗PD-1免疫治疗效果
2020-08-12 MedSci原创 MedSci原创
检查点免疫疗法的使用实现了T细胞对肿瘤的控制,但该效果会被免疫抑制的髓细胞破坏。
检查点免疫疗法的使用实现了T细胞对肿瘤的控制,但该效果会被免疫抑制的髓细胞破坏。
TREM2是一种髓细胞受体,它负责传递细胞内信号,在阿尔茨海默病期间维持小胶质反应。TREM2也被肿瘤浸润的巨噬细胞表达。

最近,研究人员在CELL发文,报导了Trem2-/-小鼠比野生型小鼠对各种癌症的生长更有抵抗力这一现象,Trem2-/-小鼠也对抗PD-1免疫疗法更有反应。
此外,当与抗PD-1联合使用时,用抗TREM2的单克隆抗体治疗可抑制肿瘤生长,并促进退变。
单细胞测序(scRNA-seq)显示,TREM2缺失和抗TREM2都与肿瘤浸润中稀少的MRC1+和CX3CR1+巨噬细胞有关,与之平行的是表达免疫刺激因子的骨髓亚群的扩张,促进T细胞反应的改善。
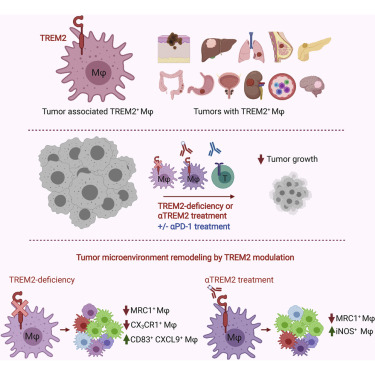
为了挖掘该发现在人类肿瘤中的意义,研究人员首先用IHC分析了来自人类正常和肿瘤标本的巨噬细胞中TREM2蛋白的表达。除了小胶质细胞、MITF+胎盘巨噬细胞、子宫内膜巨噬细胞和肺泡巨噬细胞外,绝大多数外周组织中的巨噬细胞都没有检测到TREM2的表达。
相比之下,通过对包含126个样本的多癌组织芯片的筛选评估,研究人员在75%的来自不同原发部位的肿瘤中观察到TREM2+巨噬细胞。为了规避潜在的肿瘤异质性,研究人员进一步将这一分析扩展到从99个肿瘤样本中获得的完整组织切片,其中包括来自许多部位的肿瘤。研究人员证实了TREM2+巨噬细胞在几乎所有病例中都存在。
接下来,研究人员探索了癌症基因组图谱(The Cancer Genome Atlas,TCGA)数据库中TREM2表达与临床结果之间的相关性。设定75%分位数的阈值后,TREM2表达与CRC队列中更差的总生存期相关。在TNBC队列中,以75%分位数为截止点,TREM2表达也与更差的总生存期和无复发生存期相关。使用TREM2中位数表达也得到了类似的结果。
有趣的是,在TNBC的多变量生存分析中,TREM2具有独立于其他髓系基因的额外生存预后能力,表明其对发病机制有直接贡献。在其他类型的人类肿瘤中也显示出TREM2和巨噬细胞特征基因之间的相关性,但TREM2表达与患者总体或无复发生存期的相关性并不显著,这说明TREM2对肿瘤浸润性巨噬细胞和肿瘤免疫反应的影响可能是特异性的。
因此,TREM2是改变肿瘤骨髓浸润的潜在靶点,并可能增强检查点免疫疗法。
原始出处:
Martina Molgora et al. TREM2 Modulation Remodels the Tumor Myeloid Landscape Enhancing Anti-PD-1 Immunotherapy, CELL (2020). DOI:https://doi.org/10.1016/j.cell.2020.07.013
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#REM#
76
#TREM#
125
#CEL#
57
#Cell#
76
#治疗效果#
66