BMC Med Research Method:进行低风险临床试验前,患者对知情同意书的态度如何?
2017-11-18 佚名 小狗科研
知情同意书(Information Consent Form, ICF)是保护受试者个体权益的重要武器,它既规范临床医疗行为,又约束研究行为的伦理原则。
背景
知情同意书(Information Consent Form, ICF)是保护受试者个体权益的重要武器,它既规范临床医疗行为,又约束研究行为的伦理原则。然而,传统知情同意书的弊端主要在于篇幅冗长且内容过于专业和复杂,使得受试者无法有效获取和理解其中的信息。要求签署书面的知情同意书可能会使得愿意参与的受试者减少,从而影响临床试验的效力,甚至迫使试验提前关闭。近期,BMC Medical Research Methodology报道了一篇来自西班牙的问卷调查研究,旨在探究患者是否支持签署低风险临床随机对照试验的书面ICF。
研究方法
问卷采用了基于横断面调查的2x2析因设计,评估书面ICF和口头/一般性通知(海报、宣传册等)在两种低风险临床试验中患者的接受程度。其中,一种试验是比较两个风险与收益相似的高血压药物,另一个试验是比较早上或晚上服用同一种药物。简单来说就是:
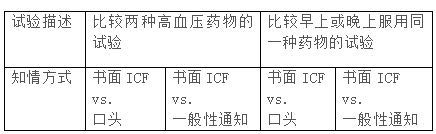
主要结果的指标包括:受访者的个人喜好和他们会推荐研究伦理委员会使用的方式。
研究结果
最终有338名受访者的问卷结果进入了统计。74%的受访者更偏向使用书面ICF,74.3%的受访者表示会和研究伦理委员会推荐书面ICF。然而,相比口头通知,一般性通知更受到患者的支持。
结论
和以往在普通人群中的调查结果相似,患者更认可书面ICF。但一些因素促使我们要考虑在低风险的临床科研中,采用更多样化的书面ICF方式,这些因素包括:
1)很多患者支持一般性通知。
2)美国的数据显示签署书面ICF的受试者如果觉得试验复杂,更容易放弃实验。
3)2016年CIOMS指南中同意在特定条件下豁免知情同意书。
如果更多调查验证了本实验的结果,可以预见的是,通过教育,一般性通知也可能成为一个低风险临床试验进行知情同意的普遍方式。
原始出处:
Rafael Dal-Re, et al. Patients’ beliefs regarding informed consent for low-risk pragmatic trails. BMC Medical Research Methodology. 2017 17:145.
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录






#BMC#
80
#MET#
71
好好好学习学习天天向上
106
#知情同意#
70
#Research#
76