A型血友病,Efanesoctocog alfa被FDA授予“快速通道资格”
2021-02-21 Allan MedSci原创
近日,美国食品药品监督管理局(FDA)已授予efanesoctocog alfa治疗A型血友病的“快速通道资格”(FTD)。
近日,美国食品药品监督管理局(FDA)已授予efanesoctocog alfa治疗A型血友病的“快速通道资格”(FTD)。Efanesoctocog alfa于2017年8月被FDA授予了“孤儿药称号”,并于2019年6月被欧盟委员会授予了“孤儿药称号”。
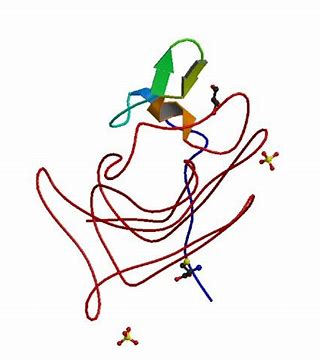
Efanesoctocog alfa是一款治疗A型血友病的新型VIII因子替代疗法。常规VIII因子疗法的半衰期受到von Willebrand因子(VWF)伴侣效应的限制,该效应被认为限制了该VIII因子在体内的停留时间。Efanesoctocog alfa在创新的Fc融合技术的基础上,增加了一个区域von Willebrand因子和XTEN®多肽,以延长其半衰期。
Efanesoctocog alfa有潜力在一周的大部分时间内提供接近正常的流血保护,而半衰期的延长可能会使预防性治疗的给药频率降低至每周一次。
目前,III期XTEND-1研究正在评估Efanesoctocog alfa治疗≥12岁A型血友病患者(n = 150)的安全性和有效性。预防组患者每周接受50 IU / kg剂量的efanesoctocog alfa预防性治疗,持续52周;对照组患者按需接受BIVV001(50 IU / kg),持续26周,然后每周改用efanesoctocog alfa,持续26周。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#血友病#
120
#CTO#
81
#A型血#
69
#ALF#
0
#OCT#
65