Cell:重磅!中国科学家揭秘肝癌发生发展机制!
2019-10-07 佚名 肿瘤资讯
2019年10月3日,国际顶尖期刊《cell》(SCI影响因子 36.216)在线发表了复旦大学附属中山医院樊嘉院士团队、中科院药物所周虎研究员团队、中科院生化与细胞所高大明研究员团队、美国“登月计划”临床蛋白质组肿瘤分析协作组(Clinical Proteomic Tumor Analysis Consortium, CPTAC)与至本医疗科技合作的关于中国乙肝病毒阳性的肝细胞癌(HBV-HCC
2019年10月3日,国际顶尖期刊《cell》(SCI影响因子 36.216)在线发表了复旦大学附属中山医院樊嘉院士团队、中科院药物所周虎研究员团队、中科院生化与细胞所高大明研究员团队、美国“登月计划”临床蛋白质组肿瘤分析协作组(Clinical Proteomic Tumor Analysis Consortium, CPTAC)与至本医疗科技合作的关于中国乙肝病毒阳性的肝细胞癌(HBV-HCC)多维蛋白组学最新研究成果(Integrated Proteogenomic Characterization of HBV-Related Hepatocellular Carcinoma)。这是一篇迄今为止中国肝癌,特别是HBV病毒感染的肝癌的多维基因蛋白质组学的最大的队列研究,也是发表的国际最高影响因子文章, 至本医疗科技作为参与该项研究的主要团队之一,也成为首家荣登国际影响力期刊CELL的中国肿瘤精准医疗公司。
该文绘制了目前全球最大规模的全景式肝癌队列多维蛋白组学图谱,发展机制,为肝癌的精准分型与个体化治疗、疗效监测和预后判断提供了新的思路和策略。
众所周知,中国是一个肝癌大国。据2018年发布的《中国肝癌大数据报告》显示,原发性肝癌全球每年新发病例85.4万,中国46.6万,约占全球的55%,这意味着,全球新发肝癌一半在中国。中国的肝癌发病率居高不下。在男性中,肝癌已是第三大高发的癌症,仅次于肺癌与胃癌。
研究团队提到,肝细胞癌约占原发性肝脏恶性肿瘤的85%-90%,最主要的病因是乙肝病毒(HBV)和丙肝病毒(HCV)的慢性感染,以及酗酒和代谢综合征。数据显示,估计全球有2.92亿人感染乙肝病毒(HBV)。值得注意的是,HBV感染是导致中国肝癌发生的最主要原因,其中约85%的肝癌患者携带HBV感染标志。
在本项研究中,研究人员收集了159例乙肝病毒阳性的肝癌和癌旁样本,运用最先进的组学技术测定了外显子组、转录组、全蛋白组、磷酸化蛋白组数据,开展了肝癌多维蛋白组学研究,通过对庞大基因和蛋白数据的大规模集中扫描,绘制出目前全球最大规模的全景式肝癌队列的基因蛋白组学图谱,多维度地揭示从基因突变到转录以及蛋白质翻译的整个过程。该研究首次结合了多组学整合分析手段,对肝癌发生和发展获得了新的认识,对肝癌的基因蛋白图谱的解析与分子分型,预后和潜在治疗新靶点的发现,以及为提升肝癌的临床治疗水平、改善预后提供了重要的支撑,使得更多的肝癌患者能够获益。
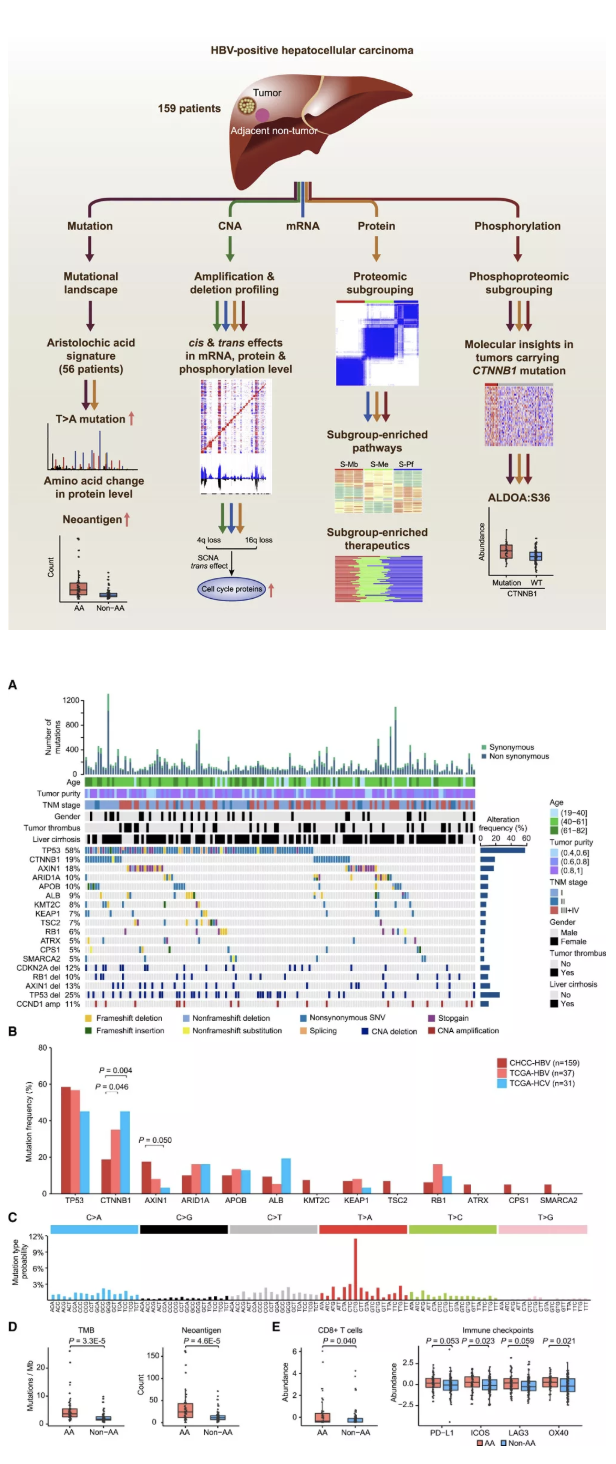
在这项最新的研究中,研究团队首先揭示了中国肝癌突变谱与西方肝癌突变谱的不同之处。其中,AXIN1(18% vs 8%),TSC2(7% vs 0%),SMARCA2(5%vs 0%)等基因在中国HBV肝癌队列的突变频率显著高于TCGA HBV肝癌队列,而CTNNB1(19%vs 35%),ARID1A(10%vs 16%)等基因则与TCGA的数据相比突变频率较低。
值得关注的是,该研究中发现超过三分之一的肝癌样本含有由马兜铃酸诱导产生的“突变特征谱”,同样在蛋白质谱数据上也检测到了由马兜铃酸引起的突变所编码的蛋白突变肽段。马兜铃酸曾在肝癌领域长期引发广泛关注及争议,被世界卫生组织(WHO)于2012年列为I类致癌物。本次研究发现,马兜铃酸“突变特征谱”与肿瘤突变负荷(TMB)、肿瘤新抗原(Neoantigen)、肿瘤微环境免疫耐受(CD8+T细胞浸润, PD-L1等免疫检查点丰度)等的临床指标显著相关。这些发现提示了免疫治疗可能会对这类肝癌产生疗效,同时,也充分反映出利用中国人肝癌数据开展临床转化研究的重要性。
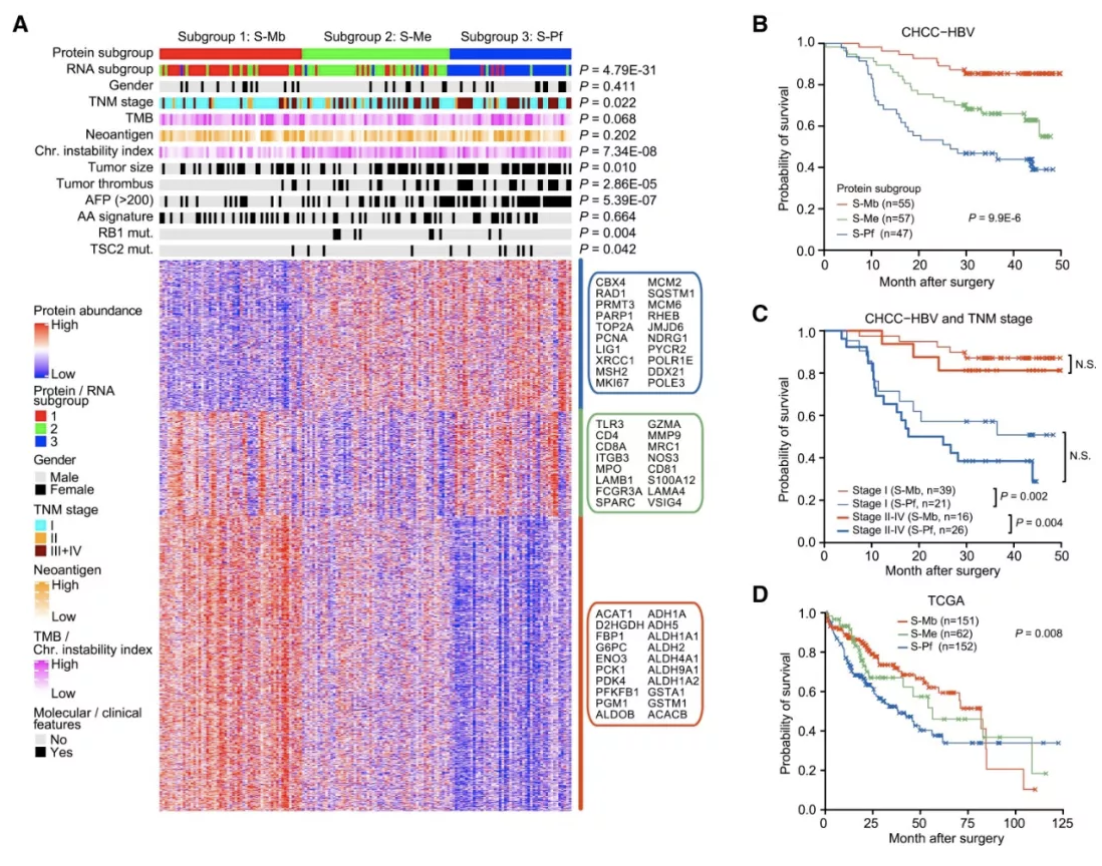
其次,肝癌患者的蛋白质组数据整体上可以分为三类亚型,它们分别是代谢驱动型(metabolism subgroup,S-Mb)、微环境失调型(Microenvironment dysregulated subgroup, S-Me)和增殖驱动型(Proliferation subgroup, S-Pf)。我们发现这三类蛋白亚型与基因组稳定性与基因突变、TNM分期、肿瘤大小、癌栓有无、甲胎蛋白(AFP)及等临床特征都存在显著相关。研究还发现,这三类亚型患者的预后具有极其显著的差别,这将为肝癌的临床预后判别,以及肝癌的个性化治疗起到重要的指导作用。
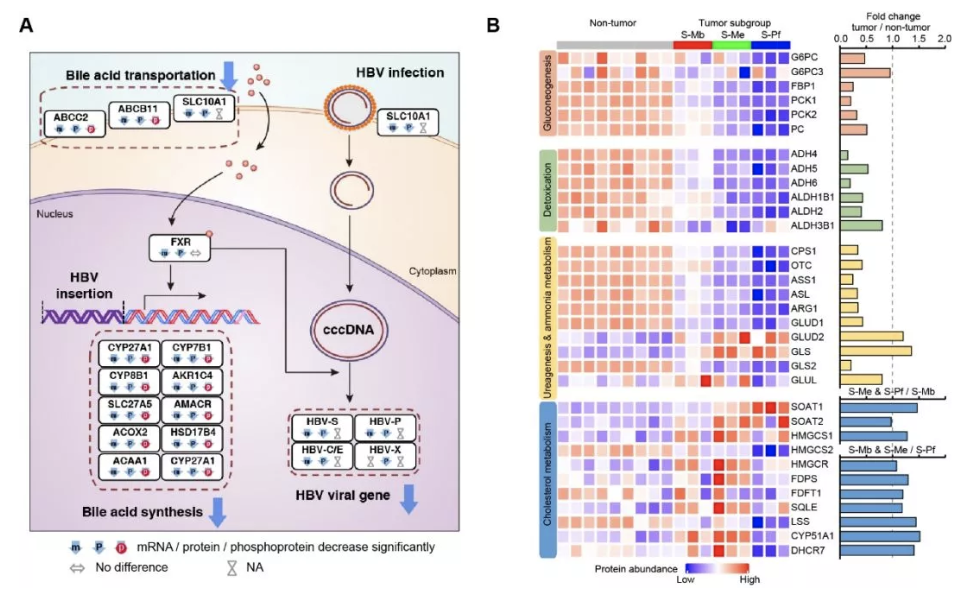
最后,本研究从多组学角度系统性地揭示了肝特异性代谢通路异常在HBV相关的肝癌中起到重要作用。我们发现超过80%的肝脏特异性基因在肝癌中呈现蛋白表达下调,而且肝特异性代谢途径中的大多数蛋白(如糖异生,解毒和尿素-氨代谢)在肝肿瘤中显著减弱,然而胆固醇代谢的关键酶(SOAT1,SOAT2,HMGCR等)和谷氨酰胺代谢相关蛋白(GLS和GLUD2)在肿瘤中表达显著上调。这些数据表明在HBV相关的肝癌中,肝特异性代谢途径发生了重编程。
作为本文的共同第一作者之一,至本医疗科技的计算肿瘤学部副总裁施巍炜博士表示,“多维组学的优势和意义,在于它可以全面地获取肿瘤不同维度的信息,利用组学间的交叉互补,探索彼此之间的内在关联,从很大程度上弥补了单一组学的不足。至本很荣幸在这个项目中承担了肝癌多维基因蛋白质组数据的主要生物信息分析和肝癌临床样本病理部分的工作,我们希望未来和临床更紧密的结合,为每一位癌症病人提供全面、准确的分子水平信息,推动癌症治疗的革新。”
原始出处:
Qiang Gao, Hongwen Zhu, et al. Integrated Proteogenomic Characterization of HBV-Related Hepatocellular Carcinoma. Cell. Oct 2019.
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#中国科学#
81
#CEL#
67
#发生发展#
67
樊院士,赞。努力学习
107
#Cell#
68