I期临床表明,iNKT细胞疗法安全性优异,并能缓解晚期黑色素瘤患者疾病进展,延长患者生存期
2024-02-26 公众号:基因启明 公众号:基因启明
据统计,全球每年黑色素瘤新发病例约324600例,死亡病例约57000例。手术切除对早期黑色素瘤有效,一旦发生远处转移预后极差,中位生存时间仅6~9个月,5年生存率为30%~40%。
亮点
1.iNKT细胞治疗对晚期黑色素瘤患者是安全且耐受性良好的。在任何入选患者中均未观察到严重不良事件;
2. 自体扩增的iNKT细胞被输注入晚期黑色素瘤患者体内后,能够产生大量IFNγ等细胞因子,并能够刺激其它免疫细胞活化,上调免疫细胞数量,进而实现抗肿瘤效果;
3.iNKT细胞疗法能够延缓晚期黑色素瘤患者疾病进展,延长生存期。
黑色素瘤起源于黑色素细胞,是恶性程度最高的皮肤肿瘤。近年来黑色素瘤发病率呈上升趋势,以每年3%~5%的速度增长。据统计,全球每年黑色素瘤新发病例约324600例,死亡病例约57000例。手术切除对早期黑色素瘤有效,一旦发生远处转移预后极差,中位生存时间仅6~9个月,5年生存率为30%~40%。
近年来,免疫疗法在黑色素瘤治疗中取得突破性进展。其中,恒定自然杀伤T(iNKT)细胞在肿瘤免疫治疗的应用潜能日益凸显。iNKT细胞在胸腺中发育,聚集在肝脏中,其次分布在脾、骨髓、淋巴结、皮肤粘膜和外周血等其他部位。其高度特异性天然糖脂配体——α-半乳糖神经酰胺(α-GalCer)有助于激活iNKT细胞产生大量的免疫调节因子,活化的iNKT细胞能通过凋亡信号转导途径,释放穿孔素、颗粒酶B和肿瘤坏死因子(TNF-α)等方式杀伤肿瘤。
近期,一项题为Adoptive Transfer of Invariant NKT Cells as Immunotherapy for Advanced Melanoma: a Phase 1 Clinical Trial的研究表明,自体体外扩增的iNKT细胞是一种可行且安全的免疫疗法,能够在体内扩增并产生IFNγ,具有提高抗肿瘤活性的潜力,且疗效安全,无重大不良反应。

首先,研究人员从9名晚期黑色素瘤患者体内成功分离并体外培养了iNKT细胞,体外扩增后iNKT细胞的纯度为13-87%(中位数为66%),其中4名患者扩增后iNKT细胞纯度与扩增前相比增加,1例患者降低,3例患者无变化;扩增后的iNKT细胞总数从1.1×107至1.26×109不等。随后,研究人员将这些iNKT细胞再次输注至患者体内,每个周期输注的iNKT细胞数量为4–217×106(中位数7.3×106)。所有患者都接受了3次iNKT输注,每次间隔2周。
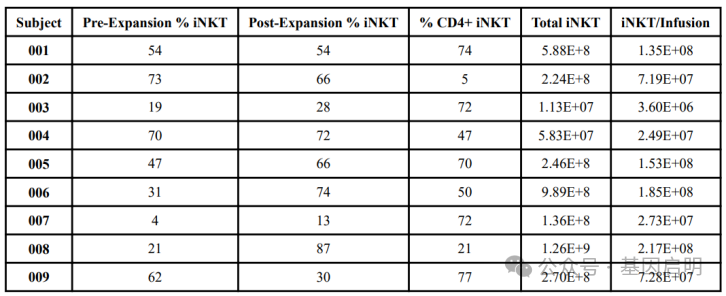
iNKT细胞扩增前和扩增后的回收率和纯度
进一步的,研究人员评估了体外扩增后iNKT细胞的细胞因子产生情况,发现体外扩增的iNKT细胞同样具有功能性,并产生与健康供体iNKT细胞相当水平的IFNγ和IL-4。
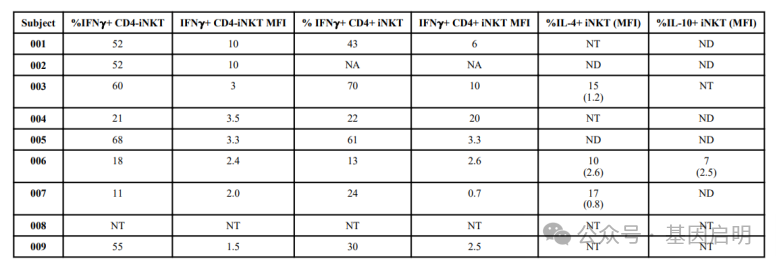
iNKT产品的功能活性
那么iNKT细胞输注后是否会影响其它免疫细胞呢?研究人员通过流式细胞术对体内免疫细胞进行了表征,他们发现免疫细胞对iNKT输注产生响应,其数量和激活状态都会发生变化,活化的单核细胞数量也普遍增加。这种改变在输注后持续1周或2周,然后恢复至基线水平。如:CD4T细胞的瞬时激活标志物——CD69的表达对每个输注周期都有响应,且大多数患者CD4T细胞的峰值均高于基线0.5-1%,并在治疗周期内返回基线。
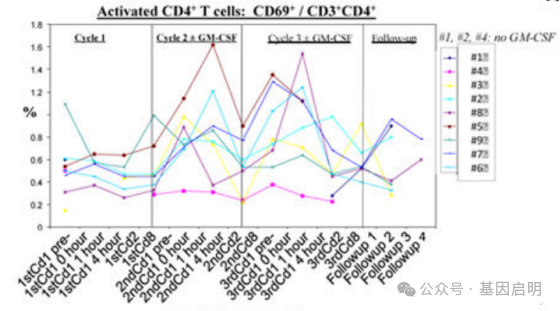
免疫细胞在输注iNKT细胞后的体内含量变化
这个发现令大家十分兴奋,他们随即评估了体内iNKT细胞的功能。
在基线和治疗完成后(第3次输注后至少一个月),研究人员用α-GalCer刺激患者,随后检测循环中IFNγ、IL-4和IL-10含量。有趣的是,他们发现经iNKT细胞治疗后,超一半的患者体内IFNγ水平升高;不论是治疗前或治疗后,注射α-GalCer均会在一定程度上刺激患者体内IL-4生成,甚至有患者在治疗后表现出更强的IL-4生成;在大多数患者中,基线IL-10的产生也相当,部分患者在治疗后表现出更强的IL-10生成。总之,研究人员认为,治疗后患者体内iNKT细胞功能增强,Th1细胞因子含量大幅度增加。
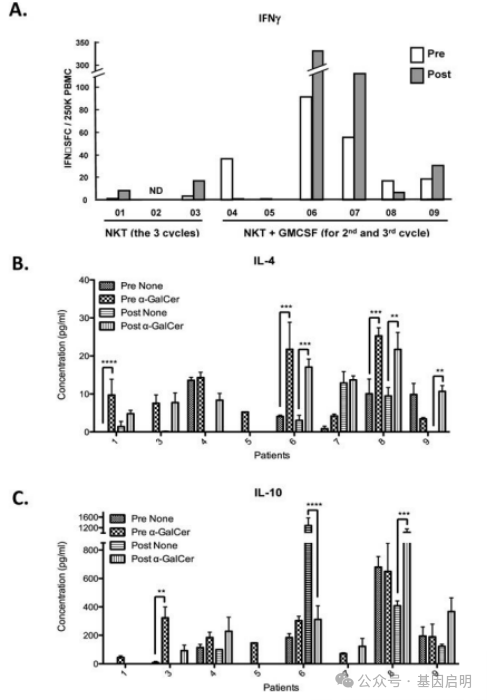
患者治疗前和治疗后iNKT细胞因子含量
那么,最关键的问题来了,输注iNKT细胞真的能够缓解病症、延长患者的生存期吗?
研究人员首先评估了iNKT细胞疗法的安全性,尽管一些患者在输注后会发生低热,但在整个疗程中依然表现出良好的耐受性。随后他们对9名患者的病情进展和生存期进行了评估,在整个随访期间,3例患者死亡,3例患者在53个月、60个月和65个月时无疾病进展,3例患者接受进一步治疗,在61个月、81个月和85个月时存活。
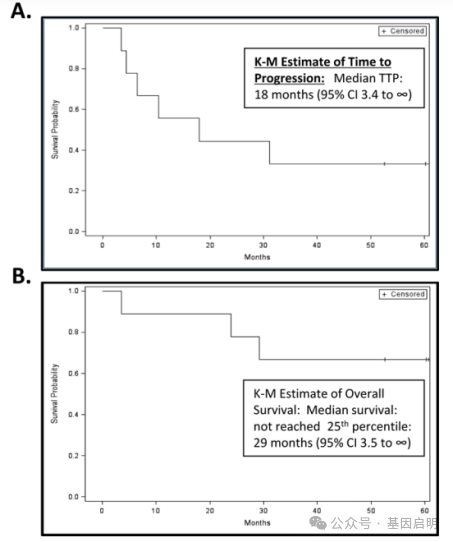
患者进展时间和总生存期数据
综上,这项I期临床试验结果表明,自体体外扩增的iNKT细胞在治疗晚期黑色素瘤方面是可行且安全的,它输注回体内能够增强iNKT细胞活性并随后激活其他免疫细胞,进而延缓患者疾病进展,延长生存期,具有极好的抗肿瘤潜力。
来源:
微信公众号:基因启明
参考文献:
Exley MA, Friedlander P, Alatrakchi N, Vriend L, Yue S, Sasada T, Zeng W, Mizukami Y, Clark J, Nemer D, LeClair K, Canning C, Daley H, Dranoff G, Giobbie-Hurder A, Hodi FS, Ritz J, Balk SP. Adoptive Transfer of Invariant NKT Cells as Immunotherapy for Advanced Melanoma: A Phase I Clinical Trial. Clin Cancer Res. 2017 Jul 15;23(14):3510-3519. doi: 10.1158/1078-0432.CCR-16-0600. Epub 2017 Feb 13. PMID: 28193627; PMCID: PMC5511564.
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#黑色素瘤# #iNKT细胞疗法#
9