Best of ECCO 2023:一文了解维得利珠单抗治疗IBD最新进展
2023-04-02 消化界 消化界
本文截取ECCO会议中关于维得利珠单抗(VDZ)治疗IBD最新进展供大家学习前沿进展。
欧洲克罗恩病和结肠炎组织(ECCO)是目前世界上最大的非营利性炎症性肠病(IBD)专家组织,每年都吸引着全球IBD学者的关注。第18届ECCO大会于3月1-4日在哥本哈根举行,主题为“Sequencing in IBD”。会议期间,热点纷呈,各国专家为IBD疾病负担、并发症管理、疾病监测和治疗目标及治疗策略提供最新的观点。
那么,会议中有哪些值得关注的IBD新进展呢?3月31日一场汇聚我国IBD领域顶级专家的学术盛会,将为大家一一解读ECCO会议中的重要进展。
本文截取ECCO会议中关于维得利珠单抗(VDZ)治疗IBD最新进展供大家学习前沿进展。
VDZ联合全肠内营养(EEN)治疗中至重度CD患者(摘要号:P677)1
研究背景:
克罗恩病(CD)是一种无法治愈的慢性肠道炎症性疾病,其导致严重的胃肠道和肠外并发症,还会引起并发症增多、生活质量变差和卫生费用增加。尽管越来越多的随机对照试验研究已证实生物制剂(包括VDZ)在活动性CD成人患者中的疗效前景,但在真实世界研究中仍有60%的患者难以达到临床和内镜缓解。该研究了评估了VDZ联合EEN治疗中-重度活动性CD的疗效。
研究方法:
该研究回顾性入组了武汉大学人民医院(又名湖北省人民医院)IBD医学中心接受VDZ治疗的28例中-重度活动性CD患者。所有患者均接受VDZ标准诱导治疗,同时接受16周EEN治疗。评估短期(第16周)和中期(第32周和第48周)临床应答、临床缓解和粪钙卫蛋白(FC),第16周和第48周时评估内镜应答和黏膜愈合。
研究结果:
患者接受VDZ静脉给药诱导和16周EEN治疗后,第16周时71.4%(20/28)达到临床缓解,73.1%(19/26)达到内镜应答,71.4%(20/28)FC正常化。第32周时的中期评估,当前治疗可持续保持79.2%(19/24)患者发生临床应答、62.5%(15/24)临床缓解和66.7%(16/24)FC正常化;第48周时超过60%患者观察到临床应答(68.2%,15/22)和黏膜愈合(63.6%,14/22)(图)。
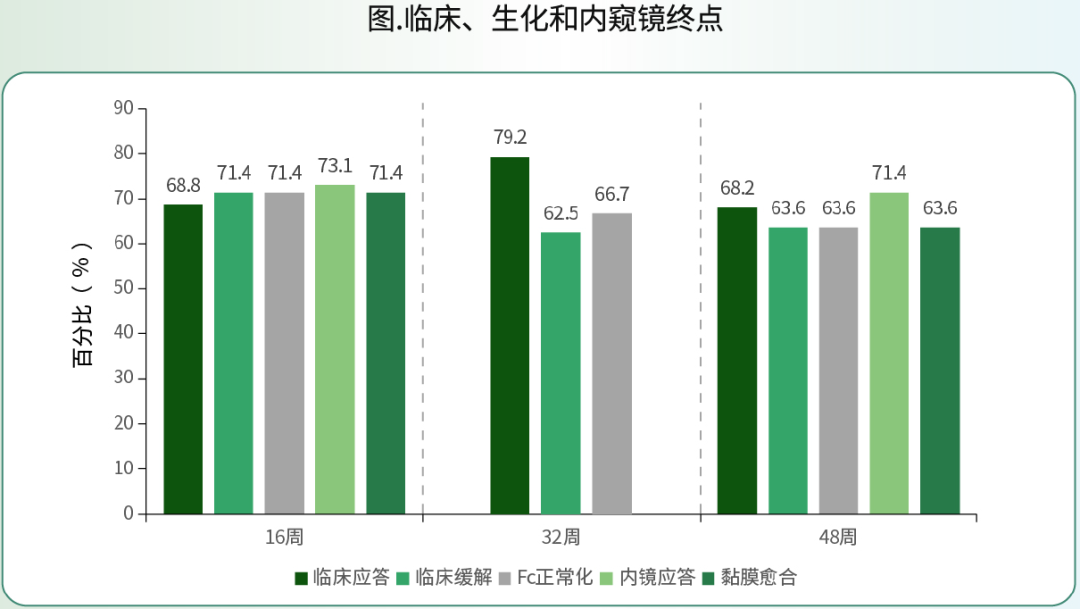
研究结论:
VDZ联合16周EEN可改善中-重度CD患者的短期和中期临床及内镜结局。
VDZ与乌司奴单抗在生物制剂初治的CD患者中的真实世界疗效和安全性比较:EVOLVE扩展研究结果(摘要号:P636)2
研究背景:
该研究对比了VDZ和乌司奴单抗作为CD患者一线生物制剂治疗的真实世界疗效和安全性。
研究方法:
EVOLVE扩展研究(NCT05056441)是一项2016年-2021年在澳大利亚、比利时或瑞士的生物制剂初治CD患者(≥18岁)中使用VDZ或乌司奴单抗治疗的多中心、观察性、回顾性队列研究。收集从治疗开始至病历提取开始的死亡或失访数据(以先发生者为准)。使用Kaplan-Meier法分析至事件发生时间,并估计12、24和36个月内的临床应答、临床缓解、黏膜愈合和治疗持续性的累积发生率。
研究结果:
研究共纳入来自31家研究中心的623例生物制剂初治的CD患者(VDZ 347例,乌司奴单抗276例)。VDZ和乌司奴单抗治疗患者在36个月内临床应答(VDZ 82.0%,乌司奴单抗 84.1%;p=0.87)和临床缓解(VDZ 88.3%,乌司奴单抗88.5%;p=0.67)的累积发生率相似。VDZ治疗患者的黏膜愈合率显著高于乌司奴单抗组(VDZ 91.3%,乌司奴单抗 87.4%,p=0.02),乌司奴单抗治疗患者在36个月内的治疗持续性更高(VDZ 70.6%,乌司奴单抗80.3%;p=0.03)。VDZ与乌司奴单抗治疗患者之间CD恶化(HR 1.01;95% CI,0.68-1.49;p=0.98)和CD相关手术(HR 1.80;95% CI,0.69-4.73;p=0.23)的风险无显著差异。
表1. 生物制剂初治CD患者接受VDZ或UST治疗在12、24和36个月的累积临床结局
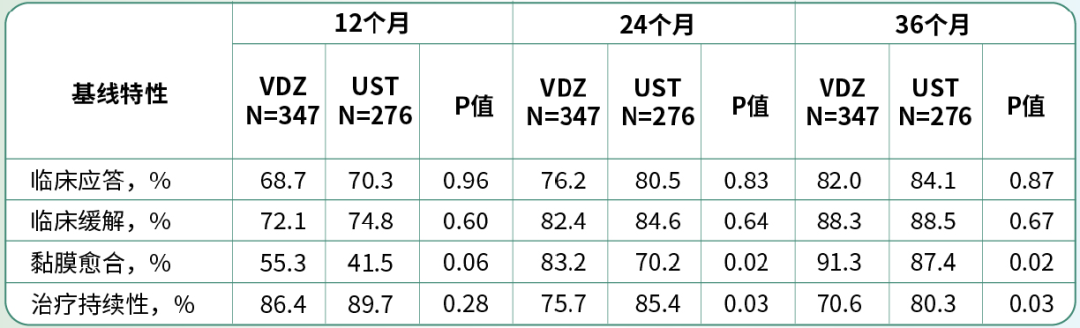
研究结论:
在真实世界环境中,VDZ与乌司奴单抗在生物制剂初治CD患者中的临床应答和临床缓解相似。在36个月内,VDZ治疗患者的黏膜愈合率较高,乌司奴单抗治疗患者的治疗持续性较高。
VDZ与英夫利西单抗和阿达木单抗在UC和CD中的实际持久性,荟萃分析(摘要号:P564)3
研究背景:
VARSITY研究显示,VDZ比阿达木单抗治疗UC的疗效更好。然而,真实世界中VDZ相较于阿达木单抗、英夫利西单抗在UC和CD患者中的有效性尚不清楚。药物持久性测量从用药开始到停止治疗的持续时间,是一种综合了治疗效果、安全性和耐受性的替代标志物。该荟萃分析比较了VDZ与TNF-α抑制剂(阿达木单抗和英夫利西单抗)在UC和CD中的药物持久性。
研究方法:
系统评价和荟萃分析检索了电子数据库——EMBASE和PubMed中2017年至2022年7月的观察性研究以及最近胃肠病学会议——2022年圣地亚哥消化疾病周中筛选的摘要。6项评估了诊断为IBD的>18岁受试者中VDZ与TNF-α抑制剂(阿达木单抗和英夫利西单抗)的治疗持久性的观察性研究符合纳入标准,并被纳入。
研究结果:
总体而言,VDZ的1年持续治疗率在UC中为71.2%,在CD中为76%,显著高于英夫利西单抗(UC为56.4%,CD为53.7%)和阿达木单抗(UC为53.7%,CD为55.6%)。(图1)头对头比较显示RR为1.15(95%CI 1.12-1.19),有利于VDZ。
从4项研究中汇总了2年的持续治疗率。VDZ在UC中的2年持续治疗率为66%,在CD中的持续治疗率为61%,优于英夫利西单抗(UC为49.7%,CD为59.1%)和阿达木单抗(UC为31.4%,CD为56%)。(图2)头对头比较的荟萃分析继续显示,VDZ与TNF-α抑制剂持续2年的差异有统计学意义(RR为1.12,95%CI 1.01-1.25)。对于UC患者,VDZ显著优于阿达木单抗和英夫利西单抗,RR分别为1.41(95%CI 1.14-1.74)和1.15(95%CI 1.06-1.25)。对于CD患者,VDZ的1年持续治疗率略高于TNF-α抑制剂(RR 1.10 95%CI 1.02-1.19)。

研究结论:
与阿达木单抗和英夫利西单抗相比,在未接受过生物制剂治疗的患者中,VDZ在UC和CD中均实现了更高的1年和2年持续治疗率。VDZ相对于TNF-α抑制剂的获益在UC中比CD更明显。
开始VDZ或其他生物制剂治疗的UC或CD患者的疲劳变化:来自比利时登记研究患者的数据(摘要号:P573)4
研究背景:
UC和CD患者的疲劳与生活质量下降相关。该研究旨在分析启用VDZ或其他生物制剂治疗的患者疲劳的发生情况,并识别与疲劳消失时间或1年时疲劳持续存在相关的因素。
研究方法:
对一项前瞻性真实世界安全性研究(PASS; NCT02674308)中随访的比利时患者的疲劳登记研究数据进行事后分析。纳入开始VDZ或其他生物制剂治疗且既往未使用VDZ的≥18岁UC或CD患者。患者完成慢性疾病治疗功能性评估-疲劳(FACIT-F)量表,医生在基线时和随后每间隔6个月(共4.5年随访)收集疾病特征。疲劳持续性定义为连续2次FACIT-F评分<40,疲劳消失(基线疲劳患者)定义为FACIT-F评分>40。使用多元回归评估与至疲劳消失时间和1年时疲劳持续相关的因素。
研究结果:
该分析纳入465例在登记研究入组时开始VDZ(n=259)或其他生物制剂治疗(n=206)的UC(n=174)或CD(n=291)患者(基线特征见表1)。所有患者的FACIT-F评分变化显示,治疗开始的初始6个月内疲劳改善,然后在研究剩余时间内稳定。至疲劳消失时间的Kaplan-Meier估计值表明,在6、12和24个月时,分别有2.1%、6.2%和14.2%的基线疲劳患者疲劳消失(OR 0.31, 0.16-0.6)。UC患者与CD患者(HR 1.53, 1.07-2.21)达到与未达到临床缓解的患者(HR 2.02,1.18-3.48)相比,每单位时间内疲劳消失的概率较高,基线时有肠外表现的患者与无肠外表现的患者相比较低(HR 0.62, 0.39-0.99)。未观察到疲劳持续/消失与治疗组、人口统计学、疾病持续时间、治疗史、其他药物使用、瘘管病史或活动性瘘管、IBD手术或临床应答之间存在相关性。
表1. 开始VDZ或其他生物制剂治疗得患者基线人口统计学和特征

a 从初次IBD诊断至指示日期的持续时间
研究结论:
这些真实世界结果表明,开始VDZ或其他生物制剂治疗UC或CD的患者的疲劳在治疗初始6个月改善,然后随时间稳定。临床缓解与疲劳持续存在的可能性较低和至疲劳消失的时间较短相关。
参考文献
1. Abstract citation ID: jjac190.0807. P677 Combination of vedolizumab and exclusive enteral nutrition in patients with moderate to severe Crohn’s Disease.
2. Abstract citation ID: jjac190.0766. P636 Real-world clinical effectiveness and safety of vedolizumab and ustekinumab in biologic-naïve patients with Crohn’s disease: Results from the EVOLVE Expansion study.
3. Abstract citation ID: jjac190.0694. P564 vedolizumab versus infliximab and adalimumab in the real-world persistence in Ulcerative Colitis and Crohn’s disease – a meta-analysis.
4. Abstract citation ID: jjac190.0703. P573 Change in fatigue in patients with Ulcerative Colitis or Crohn’s disease initiating vedolizumab or other biologic therapy: Data from Belgian registry patients.
作者:消化界
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言